Phasenselektion von Calciumcarbonat durch die Chiralität adsorbierter Aminosäuren†
Stephan E. Wolf
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorNiklas Loges
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorBernd Mathiasch Dr.
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorMartin Panthöfer Dr.
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorIngo Mey
Institut für Physikalische Chemie, Welderweg 11, 55099 Mainz, Deutschland
Search for more papers by this authorAndreas Janshoff Prof. Dr.
Institut für Physikalische Chemie, Welderweg 11, 55099 Mainz, Deutschland
Search for more papers by this authorWolfgang Tremel Prof. Dr.
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorStephan E. Wolf
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorNiklas Loges
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorBernd Mathiasch Dr.
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorMartin Panthöfer Dr.
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorIngo Mey
Institut für Physikalische Chemie, Welderweg 11, 55099 Mainz, Deutschland
Search for more papers by this authorAndreas Janshoff Prof. Dr.
Institut für Physikalische Chemie, Welderweg 11, 55099 Mainz, Deutschland
Search for more papers by this authorWolfgang Tremel Prof. Dr.
Institut für Anorganische Chemie und Analytische Chemie, Johannes-Gutenberg-Universität Mainz, Duesbergweg 10–14, 55099 Mainz, Deutschland, Fax: (+49) 6131-392-5605
Search for more papers by this authorDiese Arbeit wurde durch die Deutsche Forschungsgemeinschaft (DFG) im Rahmen des Schwerpunktprogramms “Prinzipien der Biomineralisation” unterstützt. S.E.W. ist Stipendiat der Konrad-Adenauer-Stiftung. Wir bedanken uns bei Dr. Ute Kolb für die Bereitsstellung der Software MS Modeling (Accelrys Software Inc.) sowie bei Prof. Dr. W. Hofmeister für den Zugang zu den REM-Einrichtungen.
Graphical Abstract
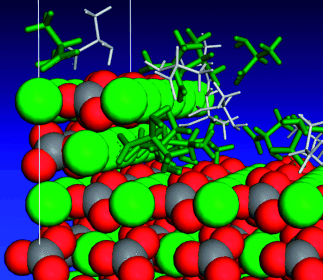
Auch Aminosäuren haben Lieblingsplätze: Die Phasenselektion von Calciumcarbonat (Kugeln: C grau, Ca grün, O rot) ist bestimmt durch chirale Aminosäuren (Stabmodelle), die während der Kristallisation anwesend sind. Das Wechselspiel zwischen Kristalloberfläche und Additiven führt zu einer enantiospezifischen Adsorption der D- und L-Aminosäuren auf chiralen Stufen des Kristallwachstums. Die resultierende Oberflächenpassivierung erzeugt eine kinetische Barriere, welche die Phasenselektion steuert.
Supporting Information
Supporting information for this article is available on the WWW under http://www.wiley-vch.de/contents/jc_2001/2007/z700010_s.pdf or from the author.
Please note: The publisher is not responsible for the content or functionality of any supporting information supplied by the authors. Any queries (other than missing content) should be directed to the corresponding author for the article.
References
- 1L. Perez-Garcia, D. B. Amabilino, Chem. Soc. Rev. 2002, 31, 342–356.
- 2
- 2aW. A. Bonner, Chirality 2000, 12, 114–126;
10.1002/(SICI)1520-636X(2000)12:3<114::AID-CHIR3>3.0.CO;2-N CAS PubMed Web of Science® Google Scholar
- 2bM. P. Bernstein, J. P. Dworkin, S. A. Sandford, G. W. Cooper, L. J. Allamandola, Nature 2002, 416, 401–403;
- 2cD. Y. Sumner, Am. J. Sci. 1997, 297, 455–487.
- 3
- 3aD. P. E. Smith, J. Vac. Sci. Technol. B 1991, 9, 1119–1125;
- 3bS. J. Sowerby, W. M. Heckl, G. B. Petersen, J. Mol. Evol. 1996, 43, 419–424;
- 3cJ. V. Barth, J. Weckesser, G. Trimarchi, M. Vladimirova, A. De Vita, C. Cai, H. Brune, P. Günter, K. Kern, J. Am. Chem. Soc. 2002, 124, 7991–7995;
- 3dH. Spillmann, A. Dmitriev, N. Lin, P. Messina, J. V. Barth, K. Kern, J. Am. Chem. Soc. 2003, 125, 10725–10728;
- 3eC. B. France, B. Parkinson, J. Am. Chem. Soc. 2003, 125, 12712–12713.
- 4
- 4aM. Ortega Lorenzo, S. Haq, T. Bertrams, P. Murray, R. Raval, C. J. Baddeley, J. Phys. Chem. B 1999, 103, 10661–10669;
- 4bM. Ortega Lorenzo, C. J. Baddeley, C. Muryn, R. Raval, Nature 2000, 404, 376–379;
- 4cR. Humblot, S. M. Barlow, R. Raval, Prog. Surf. Sci. 2004, 76, 1–19;
- 4dS. Romer, B. Behzadi, R. Fasel, K.-H. Ernst, Chem. Eur. J. 2005, 11, 4149–4154;
- 4eA. Kühnle, T. R. Linderoth, B. Hammer, F. Besenbacher, Nature 2002, 415, 891–893;
- 4fQ. Chen, R. V. Richardson, Nat. Mater. 2003, 2, 324–328.
- 5C. A. Orme, A. Noy, A. Wierzbicki, M. T. McBride, M. Grantham, H. H. Teng, P. M. Dove, J. J. DeYoreo, Nature 2001, 411, 775–779.
- 6R. M. Hazen, T. R. Filley, G. A. Goodfriend, Proc. Natl. Acad. Sci. USA 2001, 98, 5487–5490.
- 7
- 7aL. Addadi, S. Weiner, Proc. Natl. Acad. Sci. USA 1985, 82, 4110–4114;
- 7bS. Mann, Struct. Bonding (Berlin) 1983, 54, 125–174.
- 8H. A. Lowenstam, S. Weiner, On Biomineralization, Oxford University Press, New York, 1989.
10.1093/oso/9780195049770.001.0001 Google Scholar
- 9
- 9aS. Weiner, L. Addadi, J. Mater. Chem. 1997, 7, 689–702;
- 9bS. Mann, Biomineralization—Principles and Concepts in Biomaterials Chemistry, Oxford University Press, Oxford, 2001;
- 9cF. C. Meldrum, Int. Mater. Rev. 2003, 48, 187–224;
- 9dE. Bäuerlein, Biomineralization, Wiley-VCH, Weinheim, 2004;
10.1002/3527604138 Google Scholar
- 9eA. A. Berman, L. Addadi S. Weiner, Nature 1988, 331, 546–548;
- 9fG. Falini, S. Albeck, S. Weiner, L. Addadi, Science 1996, 271, 67–69;
- 9gN. Nassif, N. Pinna, N. Gehrke, M. Antonietti, C. Jäger, H. Cölfen, Proc. Natl. Acad. Sci. USA 2005, 102, 12653–12655.
- 10
- 10aI. Weißbuch, L. Addadi, M. Lahav, L. Leiserowitz, Science 1991, 253, 637–645;
- 10bD. Jaquemain, S. G. Wolf, F. Leveiller, M. Deutsch, K. Kjaer, J. Als-Nielsen, M. Lahav, L. Leiserowitz, Angew. Chem. 1992, 104, 134–158;
10.1002/ange.19921040205 Google ScholarAngew. Chem. Int. Ed. Engl. 1992, 31, 130–152;
- 10cI. Weißbuch, R. Popovitz-Biro, M. Lahav, L. Leiserowitz, Acta Crystallogr. Sect. B 1995, 51, 115–148.
- 11
- 11aS. Mann, B. R. Heywood, S. Rajam, J. D. Birchall, Nature 1988, 334, 692–695;
- 11bS. Mann, D. D. Archibald, J. M. Didymus, T. Doughlus, B. R. Heywood, F. C. Meldrum, M. J. Reeves, Science 1993, 261, 1286–1292;
- 11cJ. J. M. Donners, R. J. M. Nolte, N. A. J. M. Sommerdijk, J. Am. Chem. Soc. 2002, 124, 9700–9701;
- 11dA. M. Travaille, L. Kaptijn, P. Verwer, B. Huisgen, J. A. A. W. Elemans, R. J. M. Nolte, H. van Kempten, J. Am. Chem. Soc. 2003, 125, 11571–11577;
- 11eS. Cavalli, D. C. Popescu, E. E. Tellers, M. R. J. Vos, B. C. Pichon, M. Overhead, H. Rapaport, N. A. J. M. Somerdijk, A. Kros, Angew. Chem. 2006, 118, 753–758;
10.1002/ange.200501654 Google ScholarAngew. Chem. Int. Ed. 2006, 45, 739–744.
- 12
- 12aT. N. Thomas, T. A. Land, J. J. De Yoreo, W. H. Casey, Langmuir 2004, 20, 7643–7652;
- 12bK. J. Davis, P. M. Dove, L. E. Wasylenki, J. J. De Yoreo, Am. Mineral. 2004, 89, 714–720;
- 12cK. J. Davis, P. M. Dove, J. J. De Yoreo, Science 2000, 290, 1134–1137.
- 13J. B. Thompson, G. T. Paloczi, J. H. Kindt, M. Michenfelder, B. L. Smith, G. Stucky, D. E. Morse, P. K. Hansma, Biophys. J. 2000, 37 0, 3308–3312.
- 14
- 14aJ. Küther, W. Tremel, Chem. Commun. 1997, 2029–2030;
- 14bJ. Küther, R. Seshadri, W. Knoll, W. Tremel, J. Mater. Chem. 1998, 8, 641–650;
- 14cJ. Küther, G. Nelles, R. Seshadri, M. Schaub, H.-J. Butt, W. Tremel, Chem. Eur. J. 1998, 4, 1834–1841;
10.1002/(SICI)1521-3765(19980904)4:9<1834::AID-CHEM1834>3.0.CO;2-6 CAS Web of Science® Google Scholar
- 14dJ. Küther, R. Seshadri, W. Tremel, Angew. Chem. 1998, 110, 3196–3199;
10.1002/(SICI)1521-3757(19981102)110:21<3196::AID-ANGE3196>3.0.CO;2-E Google ScholarAngew. Chem. Int. Ed. 1998, 37, 3044–3047;10.1002/(SICI)1521-3773(19981116)37:21<3044::AID-ANIE3044>3.0.CO;2-0 CAS Web of Science® Google Scholar
- 14eJ. Küther, R. Seshadri, G. Nelles, H.-J. Butt, W. Knoll, W. Tremel, Adv. Mater. 1998, 10, 401–404;
- 14fM. Balz, H. A. Therese, J. Li, J. S. Gutmann, M. Kappl, L. Nasdala, W. Hofmeister, H.-J. Butt, W. Tremel, Adv. Funct. Mater. 2005, 15, 683–688;
- 14gM. Balz, H. A. Therese, M. Kappl, L. Nasdala, W. Hofmeister, H.-J. Butt, W. Tremel, Langmuir 2005, 21, 3981–3986;
- 14hV. Pipich, M. Balz, W. Tremel, D. Schwahn, 9th International Symposium on Biomineralization, Extended Conference Proceedings, Pucon/Chile, 6.–9. Dezember 2005;
- 14iN. Loges, K. Graf, L. Nasdala, Langmuir 2006, 22, 3073–3080;
- 14jW. Tremel, J. Küther, M. Balz, N. Loges, S. E. Wolf in Handbook of Biomineralization, Vol. 2 (Hrsg.: ), Wiley-VCH, Weinheim, 2007, S. 207–232.
- 15
- 15aW. Hou, Q. Feng, J. Cryst. Growth 2005, 282, 214–219;
- 15bC. Shivkumara, P. Singh, A. Gupta, M. S. Hegde, Mater. Res. Bull. 2006, 41, 1455–1460.
- 16Die scheinbare Überbestimmung von [Ca2+] im Vergleich zum Sollgehalt von 10 mmol der Mutterlösung ist darauf zurückzuführen, dass die Ca2+-empfindliche Elektrode ebenso auf H+ und NH4+ anspricht.
- 17Match 1.4c, Crystal Impact, Bonn, 2006; PDF-2, Release 2004, JCPDS-International Centre for Diffraction Data, Newtown Square, PA 19073-3273, USA.
- 18Um zu überprüfen, ob die Mehrzähnigkeit der Aminosäuren der ausschlaggebende Faktor ist, wurde die achirale Aminosäure β-Alanin als Additiv eingesetzt. Abweichend von Vergleichsexperimenten mit Glycin zeigte sich im Falle des β-Alanins die bevorzugte Bildung von Aragonit (siehe die Hintergrundinformationen).
- 19
- 19aMaterials Studio 4.0, Accelrys Inc., San Diego, CA, 2006;
- 19bH. Sun, J. Phys. Chem. B 1998, 102, 7338–7364.
- 20
- 20aJ. R. Cronin, S. Pizzarello, Science 1997, 275, 951–955;
- 20bS. Pizzarello, J. R. Cronin, Geochim. Cosmochim. Acta 2000, 64, 329–338;
- 20cJ. Bailey, A. Chrysostomou, J. H. Hough, T. M. Gledhill, A. McCall, S. Clark, F. Menard, M. Tamura, Science 1998, 281, 672–674;
- 20dR. M. Hazen, T. R. Filley, G. A. Goodfriend, Proc. Natl. Acad. Sci. USA 2001, 98, 5487–5490.
- 21R. T. Downs, R. M. Hazen, J. Mol. Catal. A 2004, 216, 273–285.
- 22
- 22aV. A. Avetisov, V. I. Goldanskii, V. V. Kuz'min, Phys. Today 1991, 44, 33–41;
- 22bG. Ertem, J. P. Ferris, J. Am. Chem. Soc. 1997, 119, 7197–7201.
- 23
- 23aD. H. Lee, K. Severin, Y. Yokobayashi, M. R. Ghadiri, Nature 1997, 390, 591–594;
- 23bS. Yao, I. Ghosh, R. Zutshi, J. Chimielewski, Nature 1998, 396, 447–450.
- 24
- 24aC. Chyba, C. Sagan, Nature 1992, 355, 125–132;
- 24bD. P. Glavin, J. L. Bada, K. F. Brinton, G. McDonald, Proc. Natl. Acad. Sci. USA 1997, 94, 8835–8838.
- 25W. L. Marshall, Geochim. Cosmochim. Acta 1994, 58, 2099–2106.
- 26P. Cintas, Angew. Chem. 2002, 114, 1187–1193;
10.1002/1521-3757(20020402)114:7<1187::AID-ANGE1187>3.0.CO;2-S Google ScholarAngew. Chem. Int. Ed. 2002, 41, 1139–1145.10.1002/1521-3773(20020402)41:7<1139::AID-ANIE1139>3.0.CO;2-9 CAS PubMed Web of Science® Google Scholar
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.