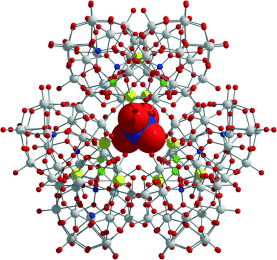
PO43−-vermittelter Aufbau eines Polyoxometallat-Superclusters†
Xikui Fang Dr.
Ames Laboratory, Iowa State University, Ames, Iowa 50011 (USA)
Search for more papers by this authorPaul Kögerler Prof. Dr.
Ames Laboratory, Iowa State University, Ames, Iowa 50011 (USA)
Institut für Anorganische Chemie, RWTH Aachen, 52074 Aachen (Deutschland)
Search for more papers by this authorXikui Fang Dr.
Ames Laboratory, Iowa State University, Ames, Iowa 50011 (USA)
Search for more papers by this authorPaul Kögerler Prof. Dr.
Ames Laboratory, Iowa State University, Ames, Iowa 50011 (USA)
Institut für Anorganische Chemie, RWTH Aachen, 52074 Aachen (Deutschland)
Search for more papers by this authorWir danken Gordon Miller für den gewährten Zugang zu einem Röntgendiffraktometer. Ames Laboratory wird von der Iowa State University für das U.S. Department of Energy betrieben (DE-AC02-07CH11358).
Graphical Abstract
Kleines Anion, große Wirkung: Der Aufbau eines heterochiralen Polyoxometallat-Aggregats aus zehn molekularen Komponenten (siehe Struktur; W grau, Mn grün, Ce gelb, P blau, O rot) wird durch den Templateffekt eines einzigen Phosphations gesteuert. In der Synthese werden drei dimere magnetische Dawson-Bausteine durch Koordinationszahlkontrolle zusammengefügt.
Supporting Information
Supporting information for this article is available on the WWW under http://www.wiley-vch.de/contents/jc_2001/2008/z802491_s.pdf or from the author.
Please note: The publisher is not responsible for the content or functionality of any supporting information supplied by the authors. Any queries (other than missing content) should be directed to the corresponding author for the article.
References
- 1 Comprehensive Coordination Chemistry II, Vol. 7 (Hrsg.: ), Elsevier, Oxford, 2004.
- 2
- 2aM. E. Davis, Nature 2002, 417, 813;
- 2bP.-G. Lassahn, V. Lozan, G. A. Timco, P. Christian, C. Janiak, R. E. P. Winpenny, J. Catal. 2004, 222, 260.
- 3
- 3aV. K. Yachandra, K. Sauer, M. P. Klein, Chem. Rev. 1996, 96, 2927;
- 3bR. Manchanda, G. W. Brudvig, R. H. Crabtreee, Coord. Chem. Rev. 1995, 144, 1.
- 4
- 4aM. W. Cooke, G. S. Hanan, Chem. Soc. Rev. 2007, 36, 1466;
- 4bD. Gatteschi, R. Sessoli, J. Villain, Molecular Nanomagnets, Oxford University Press, New York, 2006.
- 5R. E. P. Winpenny, Adv. Inorg. Chem. 2001, 52, 1.
- 6
- 6aR. W. Saalfrank, I. Bernt, E. Uller, F. Hampel, Angew. Chem. 1997, 109, 2596;
10.1002/ange.19971092225 Google ScholarAngew. Chem. Int. Ed. Engl. 1997, 36, 2482;
- 6bB. Hasenknopf, J.-M. Lehn, N. Boumediene, A. Dupont-Gervais, A. Van Dorsselaer, B. Kneisel, D. Fenske, J. Am. Chem. Soc. 1997, 119, 10956;
- 6cJ. S. Fleming, K. L. V. Mann, C.-A. Carraz, E. Psillakis, J. C. Jefferey, J. A. McCleverty, M. D. Ward, Angew. Chem. 1998, 110, 1315;
10.1002/(SICI)1521-3757(19980504)110:9<1315::AID-ANGE1315>3.0.CO;2-2 Google ScholarAngew. Chem. Int. Ed. 1998, 37, 1279;10.1002/(SICI)1521-3773(19980518)37:9<1279::AID-ANIE1279>3.0.CO;2-Q CAS PubMed Web of Science® Google Scholar
- 6dR. Wang, Z. Zheng, T. Jin, R. J. Staples, Angew. Chem. 1999, 111, 1929;
10.1002/(SICI)1521-3757(19990614)111:12<1929::AID-ANGE1929>3.0.CO;2-F Web of Science® Google ScholarAngew. Chem. Int. Ed. 1999, 38, 1813;10.1002/(SICI)1521-3773(19990614)38:12<1813::AID-ANIE1813>3.0.CO;2-3 CAS PubMed Web of Science® Google Scholar
- 6eX. Lin, D. M. J. Doble, A. J. Blake, A. Harrison, C. Wilson, M. Schröder, J. Am. Chem. Soc. 2003, 125, 9476;
- 6fA. J. Tasiopoulos, W. Wernsdorfer, B. Moulton, M. J. Zaworotko, G. Christou, J. Am. Chem. Soc. 2003, 125, 15274;
- 6gG. J. T. Cooper, G. N. Newton, P. Kögerler, D.-L. Long, L. Engelhardt, M. Luban, L. Cronin, Angew. Chem. 2007, 119, 1362;
10.1002/ange.200603870 Google ScholarAngew. Chem. Int. Ed. 2007, 46, 1340.
- 7
- 7aP. D. Beer, P. A. Gale, Angew. Chem. 2001, 113, 502;
10.1002/1521-3757(20010202)113:3<502::AID-ANGE502>3.0.CO;2-A Google ScholarAngew. Chem. Int. Ed. 2001, 40, 486;10.1002/1521-3773(20010202)40:3<486::AID-ANIE486>3.0.CO;2-P CAS PubMed Web of Science® Google Scholar
- 7bR. Vilar, Angew. Chem. 2003, 115, 1498; Angew. Chem. Int. Ed. 2003, 42, 1460.
- 8
- 8aD. H. Busch, A. L. Vance, A. G. Kolchinski in Comprehensive Supramolecular Chemistry, Vol. 9 (Hrsg.: ), Pergamon, New York, 1996, S. 1–42;
- 8bG. Seeber, B. E. F. Tiedemann, K. N. Raymond, Top. Curr. Chem. 2006, 265, 147.
- 9A. Müller, H. Reuter, S. Dillinger, Angew. Chem. 1995, 107, 2505; Angew. Chem. Int. Ed. Engl. 1995, 34, 2328.
- 10E. Cadot, F. Sécheresse, Chem. Commun. 2003, 2189, zit. Lit.
- 11P. Mialane, A. Dolbecq, J. Marrot, E. Rivière, F, Sécheresse, Angew. Chem. 2003, 115, 3647;
10.1002/ange.200351486 Google ScholarAngew. Chem. Int. Ed. 2003, 42, 3523.
- 12X. Fang, P. Kögerler, Chem. Commun. 2008, 3396.
- 13
- 13aA. J. Tasiopoulos, T. A. O'Brien, K. A. Abboud, G. Christou, Angew. Chem. 2004, 116, 349;
10.1002/ange.200352898 Google ScholarAngew. Chem. Int. Ed. 2004, 43, 345;
- 13bA. J. Tasiopoulos, P. L. Milligan, Jr., K. A. Abboud, T. A. O'Brien, G. Christou, Inorg. Chem. 2007, 46, 9678.
- 14Röntgenstrukturdaten für K36Na111⋅106 H2O: H224Ce9K36Mn6Na11O468P13W90, T=173(2) K, M=27914.11 g mol−1, monoklin, Raumgruppe C2/c, a=23.516(4), b=41.631(7), c=44.508(8) Å, V=43166(13) Å3, Z=4, μ(MoKα) = 25.499 mm−1, 135 264 Reflexe, 31 135 unabhängig (Rint=0.1141). Max./min. Elektronenrestdichten: 5.53/−3.79 e Å−3. Die Verfeinerung konvergierte zu R(Fo)=0.0782, wR(
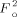 )=0.1721 und GOF=1.088 mit I>2σ(I). Weitere Einzelheiten zur Kristallstrukturuntersuchung können beim Fachinformationszentrum Karlsruhe, 76344 Eggenstein-Leopoldshafen (Fax: (+49) 7247-808-666; E-mail: [email protected]), unter der Hinterlegungsnummer CSD-419470 angefordert werden.
)=0.1721 und GOF=1.088 mit I>2σ(I). Weitere Einzelheiten zur Kristallstrukturuntersuchung können beim Fachinformationszentrum Karlsruhe, 76344 Eggenstein-Leopoldshafen (Fax: (+49) 7247-808-666; E-mail: [email protected]), unter der Hinterlegungsnummer CSD-419470 angefordert werden.
- 15
- 15aDie Reinheit des eingesetzten Polyoxowolframats Na12[α-P2W15O56]⋅18 H2O beträgt nur ca. 90 %, die genaue Identität und Zusammensetzung der Verunreinigungen sind nicht bekannt, siehe: B. J. Hornstein, R. G. Finke, Inorg. Chem. 2002, 41, 2720;
- 15bfolgender einfacher Test zeigte uns, dass Phosphat tatsächlich als Verunreinigung vorliegt: Zugabe von Na12[α-P2W15O56]⋅18 H2O zu einer verdünnten CaCl2-Lösung führt zur sofortigen Ausfällung von Ca3(PO4)2. Dagegen bewirkt die Zugabe des als Reinstoff isolierbaren monolakunaren Derivats K10[α2-P2W17O61]⋅20 H2O keinen Niederschlag, entsprechende Lösungen bleiben auch nach Wochen klar. Diese Ergebnisse deuten auch darauf hin, dass die lakunaren Phosphowolframat-Liganden wahrscheinlich keine Quelle für freie PO43−-Ionen sind.
- 16Bindungsvalenzsummen wurden zur Bestimmung der Protonierungsgrade (Oxo, OH oder OH2) der Sauerstoffgruppen und der Oxidationszahlen der Ce- und Mn-Zentren in 1 genutzt, siehe die Hintergrundinformationen.
- 17Für einen detaillierten strukturellen Vergleich der {Ce3Mn2}-Kerne in 2 und 1 siehe die Hintergrundinformationen.
- 18Die für die Dimerbausteine in 1 gewählten Chiralitätsbezeichnungen folgen den IUAC-Konventionen für Tris-Chelatkomplexe, wo Enantiomere durch die Präfixe Λ und Δ unterschieden werden. Entlang der zweizähligen Achsen betrachtet werden die Pseudodimere nach dem Drehsinn der beiden gewinkelten Polyoxoanion-Liganden als Δ (im Uhrzeigersinn) und Λ (gegen den Uhrzeigersinn) bezeichnet (siehe die Hintergrundinformationen).
- 19R. Contant, Inorg. Synth. 1990, 27, 106.
10.1002/9780470132586.ch18 Google Scholar
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.