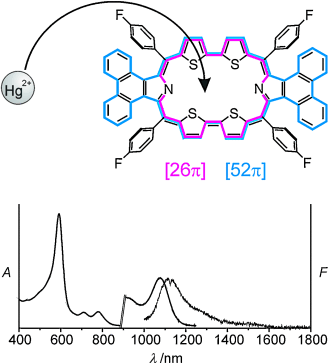
Ein kernmodifiziertes Rubyrin mit meso-Aryl-Subsituenten und Phenanthren-anellierten Pyrrolringen als hoch konjugierter NIR-Farbstoff und Hg2+-Sonde†
Di Wu Dr.
State Key Laboratory of Coordination Chemistry, Nanjing University-Jinchuan Group Ltd. Joint Laboratory of Metal Chemistry, Nanjing University, Nanjing, 210093, China, Fax: (+86) 25-8331-4502
Search for more papers by this authorAna B. Descalzo Dr.
Bundesanstalt für Materialforschung und -prüfung (BAM), Richard-Willstätter-Straße 11, 12489 Berlin, Deutschland, Fax: (+49) 30-8104-5005
Search for more papers by this authorFritz Weik Dr.
Max-Born-Institut für Nichtlineare Optik und Kurzzeitspektroskopie, Max-Born-Straße 2A, 12489 Berlin, Deutschland
Search for more papers by this authorFranziska Emmerling Dr.
Bundesanstalt für Materialforschung und -prüfung (BAM), Richard-Willstätter-Straße 11, 12489 Berlin, Deutschland, Fax: (+49) 30-8104-5005
Search for more papers by this authorZhen Shen Prof.
State Key Laboratory of Coordination Chemistry, Nanjing University-Jinchuan Group Ltd. Joint Laboratory of Metal Chemistry, Nanjing University, Nanjing, 210093, China, Fax: (+86) 25-8331-4502
Search for more papers by this authorXiao-Zeng You Prof.
State Key Laboratory of Coordination Chemistry, Nanjing University-Jinchuan Group Ltd. Joint Laboratory of Metal Chemistry, Nanjing University, Nanjing, 210093, China, Fax: (+86) 25-8331-4502
Search for more papers by this authorKnut Rurack Dr.
Bundesanstalt für Materialforschung und -prüfung (BAM), Richard-Willstätter-Straße 11, 12489 Berlin, Deutschland, Fax: (+49) 30-8104-5005
Search for more papers by this authorDi Wu Dr.
State Key Laboratory of Coordination Chemistry, Nanjing University-Jinchuan Group Ltd. Joint Laboratory of Metal Chemistry, Nanjing University, Nanjing, 210093, China, Fax: (+86) 25-8331-4502
Search for more papers by this authorAna B. Descalzo Dr.
Bundesanstalt für Materialforschung und -prüfung (BAM), Richard-Willstätter-Straße 11, 12489 Berlin, Deutschland, Fax: (+49) 30-8104-5005
Search for more papers by this authorFritz Weik Dr.
Max-Born-Institut für Nichtlineare Optik und Kurzzeitspektroskopie, Max-Born-Straße 2A, 12489 Berlin, Deutschland
Search for more papers by this authorFranziska Emmerling Dr.
Bundesanstalt für Materialforschung und -prüfung (BAM), Richard-Willstätter-Straße 11, 12489 Berlin, Deutschland, Fax: (+49) 30-8104-5005
Search for more papers by this authorZhen Shen Prof.
State Key Laboratory of Coordination Chemistry, Nanjing University-Jinchuan Group Ltd. Joint Laboratory of Metal Chemistry, Nanjing University, Nanjing, 210093, China, Fax: (+86) 25-8331-4502
Search for more papers by this authorXiao-Zeng You Prof.
State Key Laboratory of Coordination Chemistry, Nanjing University-Jinchuan Group Ltd. Joint Laboratory of Metal Chemistry, Nanjing University, Nanjing, 210093, China, Fax: (+86) 25-8331-4502
Search for more papers by this authorKnut Rurack Dr.
Bundesanstalt für Materialforschung und -prüfung (BAM), Richard-Willstätter-Straße 11, 12489 Berlin, Deutschland, Fax: (+49) 30-8104-5005
Search for more papers by this authorWir danken dem National Basic Research Program of China (No. 2006CB806104, 2007CB925103), der National Natural Science Foundation of China (No. 20401009), der Fok Ying Tung Education Foundation (No. 104013), der Alexander von Humboldt-Stiftung und der Europäischen Kommission (Marie-Curie-Stipendium) für finanzielle Unterstützung sowie Dr. T. Okujima und Prof. N. Ono (Ehime University) für MALDI-TOF-MS-, Dr. A. Jakob (Bruker) für HRMS-, Dr. J. P. Lei (Nanjing University) für CV- und Dr. K. Hoffmann (BAM) für CLSM-Messungen, Dr. J. W. Tomm (MBI) für Zugang zum FT-IR-Spektrometer und Dr. N. Dantan (BAM) für die Bereitstellung von D4.
Graphical Abstract
„Am anderen Ende der Leitung“ ist das erste kernmodifizierte expandierte Porphyrin, an dessen Pyrrolringe polycyclische aromatische Substituenten anelliert sind, das bis weit ins nahe Infrarot hinein absorbiert und im Bereich des zweiten optischen Telekommunikationsfensters fluoresziert. Die Einbettung des Farbstoffs in eine Polyurethanmembran ergibt einen Teststreifen zum Hg2+-Nachweis.
Supporting Information
Supporting information for this article is available on the WWW under http://www.wiley-vch.de/contents/jc_2001/2008/z702854_s.pdf or from the author.
Please note: The publisher is not responsible for the content or functionality of any supporting information supplied by the authors. Any queries (other than missing content) should be directed to the corresponding author for the article.
References
- 1J. L. Sessler, D. Seidel, Angew. Chem. 2003, 115, 5292–5333;
10.1002/ange.200200561 Google ScholarAngew. Chem. Int. Ed. 2003, 42, 5134–5175; S. Shimizu, N. Aratani, A. Osuka, Chem. Eur. J. 2006, 12, 4909–4918; J. L. Sessler, D.-G. Cho, M. Stepien, V. Lynch, J. Waluk, Z. S. Yoon, D. Kim, J. Am. Chem. Soc. 2006, 128, 12640–12641; R. Misra, R. Kumar, T. K. Chandrashekar, B. S. Joshi, J. Org. Chem. 2007, 72, 1153–1160.
- 2H. Rath, J. Sankar, V. PrabhuRaja, T. K. Chandrashekar, A. Nag, D. Goswami, J. Am. Chem. Soc. 2005, 127, 11608–11609; C. Comuzzi, S. Cogoi, M. Overhand, G. A. van der Marel, H. S. Overkleeft, L. E. Xodo, J. Med. Chem. 2006, 49, 196–204; J. Ramos, M. Sirisawad, R. Miller, L. Naumovski, Mol. Cancer Ther. 2006, 5, 1176–1182.
- 3S. Shimizu, A. Osuka, Eur. J. Inorg. Chem. 2006, 1319–1335; J. L. Sessler, E. Tomat, Acc. Chem. Res. 2007, 40, 371–379.
- 4M. R. Kumar, T. K. Chandrashekar, J. Inclusion Phenom. Mol. Recognit. Chem. 1999, 35, 553–582; J. L. Sessler, S. Camiolo, P. A. Gale, Coord. Chem. Rev. 2003, 240, 17–55.
- 5H. Furuta, M. J. Cyr, J. L. Sessler, J. Am. Chem. Soc. 1991, 113, 6677–6678; J. Nishimoto, T. Yamada, M. Tabata, Anal. Chim. Acta 2001, 428, 201–208; J. M. Lintuluoto, K. Nakayama, J. Setsune, Chem. Commun. 2006, 3492–3494.
- 6A. Srinivasan, V. R. G. Anand, S. K. Pushpan, T. K. Chandrashekar, K. Sugiura, Y. Sakata, J. Chem. Soc. Perkin Trans. 2 2000, 1788–1793.
- 7
- 7aS. J. Weghorn, J. L. Sessler, V. Lynch, T. F. Baumann, J. W. Sibert, Inorg. Chem. 1996, 35, 1089–1090;
- 7bS. J. Narayanan, B. Sridevi, T. K. Chandrashekar, U. Englich, K. Ruhlandt-Senge, Inorg. Chem. 2001, 40, 1637–1645.
- 8J. H. Kwon, T. K. Ahn, M.-C. Yoon, D. Y. Kim, M. K. Koh, D. Kim, H. Furuta, M. Suzuki, A. Osuka, J. Phys. Chem. B 2006, 110, 11683–11690.
- 9X.-J. Zhu, S.-T. Fu, W.-K. Wong, J.-P. Guo, W.-Y. Wong, Angew. Chem. 2006, 118, 3222–3226; Angew. Chem. Int. Ed. 2006, 45, 3150–3154.
- 10K. Rurack, M. Kollmannsberger, U. Resch-Genger, J. Daub, J. Am. Chem. Soc. 2000, 122, 968–969; J. V. Ros-Lis, R. Martínez-Máñez, K. Rurack, F. Sancenón, J. Soto, M. Spieles, Inorg. Chem. 2004, 43, 5183–5185.
- 11Z. Shen, H. Röhr, K. Rurack, H. Uno, M. Spieles, B. Schulz, G. Reck, N. Ono, Chem. Eur. J. 2004, 10, 4853–4871; Y.-H. Yu, A. B. Descalzo, Z. Shen, H. Röhr, Q. Liu, Y.-W. Wang, M. Spieles, Y.-Z. Li, K. Rurack, X.-Z. You, Chem. Asian J. 2006, 1, 176–187.
- 12Gemäß dem Prinzip von harten und weichen Säuren und Basen (HSAB): R. G. Pearson, J. Am. Chem. Soc. 1963, 85, 3533–3539.
- 13A. Srinivasan, V. M. Reddy, S. J. Narayanan, B. Sridevi, S. K. Pushpan, M. Ravikumar, T. K. Chandrashekar, Angew. Chem. 1997, 109, 2710–2713;
10.1002/ange.19971092308 Google ScholarAngew. Chem. Int. Ed. Engl. 1997, 36, 2598–2601.
- 14A. Srinivasan, S. K. Pushpan, M. Ravikumar, T. K. Chandrashekar, R. Roy, Tetrahedron 1999, 55, 6671–6680.
- 15T. D. Lash, J. Porphyrins Phthalocyanines 2001, 5, 267–288.
- 16Es sind nur wenige solche expandierte Porphyrine bekannt:
- 16aJ.-Y. Shin, H. Furuta, A. Osuka, Angew. Chem. 2001, 113, 639–641;
Angew. Chem. Int. Ed. 2001, 40, 619–621;
10.1002/1521-3773(20010202)40:3<619::AID-ANIE619>3.0.CO;2-X CAS PubMed Web of Science® Google Scholar
- 16bH. Hata, H. Shinokubo, A. Osuka, Angew. Chem. 2005, 117, 954–957;
10.1002/ange.200462231 Google ScholarAngew. Chem. Int. Ed. 2005, 44, 932–935;
- 16cY. Inokuma, T. Matsunari, N. Ono, H. Uno, A. Osuka, Angew. Chem. 2005, 117, 1890–1894;
10.1002/ange.200462815 Google ScholarAngew. Chem. Int. Ed. 2005, 44, 1856–1860;
- 16dP. K. Panda, Y.-J. Kang, C.-H. Lee, Angew. Chem. 2005, 117, 4121–4123;
10.1002/ange.200500944 Google ScholarAngew. Chem. Int. Ed. 2005, 44, 4053–4055;
- 16eW. Maes, J. Vanderhaeghen, W. Dehaen, Chem. Commun. 2005, 2612–2614.
- 17K. M. Hossain, T. Kameyama, T. Shibata, K. Takagi, Bull. Chem. Soc. Jpn. 2001, 74, 2415–2420.
- 18A. Ulman, J. Manassen, J. Am. Chem. Soc. 1975, 97, 6540–6544.
- 19Röntgenstrukturanalyse von 1: C76H40F4S4N2⋅4 CHCl3, Mr=1662.938, Kristallgröße 0.10>0.08>0.07 mm3, monoklin C2/c (No. 15), a=26.880(5), b=25.710(5), c=20.240(5) Å, β=119.23(0)°, V=12 206(34) Å3, Z=8, ρber.=1.54 g cm−3, T=293(2) K, 23 066 gemessene Reflexe, 6555 Reflexe mit [I>2σ(I)]. R=0.0550, RW=0.0972, GOF=0.881. CCDC-659352 enthält die ausführlichen kristallographischen Daten zu dieser Veröffentlichung. Die Daten sind kostenlos beim Cambridge Crystallographic Data Centre über www.ccdc.cam.ac.uk/data_request/cif erhältlich.
- 20S. Shimizu, R. Taniguchi, A. Osuka, Angew. Chem. 2005, 117, 2265–2269; Angew. Chem. Int. Ed. 2005, 44, 2225–2229.
- 21M. Meot-Ner, A. D. Adler, J. Am. Chem. Soc. 1975, 97, 5107–5111; L. R. Milgrom, J. P. Hill, S. Bone, Adv. Mater. Opt. Electron. 1993, 2, 143–147.
- 22J. L. Sessler, T. Morishima, V. Lynch, Angew. Chem. 1991, 103, 1018–1020; Angew. Chem. Int. Ed. Engl. 1991, 30, 977–980.
- 23J. D. Spence, T. D. Lash, J. Org. Chem. 2000, 65, 1530–1539.
- 24Z. S. Yoon, J. H. Kwon, M.-C. Yoon, M. K. Koh, S. B. Noh, J. L. Sessler, J. T. Lee, D. Seidel, A. Aguilar, S. Shimizu, M. Suzuki, A. Osuka, D. Kim, J. Am. Chem. Soc. 2006, 128, 14128–14134. Über das Spektrum des Dikations von 6 wurde dort nicht berichtet.
- 25H.-J. Xu, Z. Shen, T. Okujima, N. Ono, X.-Z. You, Tetrahedron Lett. 2006, 47, 931–934.
- 26M. Suzuki, M.-C. Yoon, D. Y. Kim, J. H. Kwon, H. Furuta, D. Kim, A. Osuka, Chem. Eur. J. 2006, 12, 1754–1759.
- 27T. K. Ahn, J. H. Kwon, D. Y. Kim, D. W. Cho, D. H. Jeong, S. K. Kim, M. Suzuki, S. Shimizu, A. Osuka, D. Kim, J. Am. Chem. Soc. 2005, 127, 12856–12861.
- 28Von uns wurde hier keine kürzerwellige Fluoreszenz gefunden, wie sie für 7 in Lit. [30] und in J.-H. Ha, G. Y. Jung, M.-S. Kim, Y. H. Lee, K. Shin, Y.-R. Kim, Bull. Korean Chem. Soc. 2001, 22, 63–67 beschrieben wurde.
- 29J. Mack, Y. Asano, N. Kobayashi, M. J. Stillman, J. Am. Chem. Soc. 2005, 127, 17697–17711.
- 30A. Srinivasan, M. R. Kumar, R. P. Pandian, S. Mahajan, K. S. Pushpan, B. Sridevi, S. J. Narayanan, T. K. Chandrashekar, J. Porphyrins Phthalocyanines 1998, 2, 305–314.
10.1002/(SICI)1099-1409(199807/10)2:4/5<305::AID-JPP72>3.0.CO;2-R CAS Web of Science® Google Scholar
- 31F. Zahir, S. J. Rizwi, S. K. Haq, R. H. Khan, Environ. Toxicol. Pharmacol. 2005, 20, 351–360; L. D. Hylander, M. Meili, Crit. Rev. Environ. Sci. Technol. 2005, 35, 1–36.
- 32J. V. Ros-Lis, M. D. Marcos, R. Martínez-Máñez, K. Rurack, J. Soto, Angew. Chem. 2005, 117, 4479–4482;
10.1002/ange.200500583 Google ScholarAngew. Chem. Int. Ed. 2005, 44, 4405–4407.
- 33P. Pallavicini, Y. A. Diaz-Fernandez, F. Foti, C. Mangano, S. Patroni, Chem. Eur. J. 2007, 13, 178–187; L. Feng, Z. Chen, Sens. Actuators B 2007, 122, 600–604; E. M. Nolan, S. J. Lippard, J. Am. Chem. Soc. 2007, 129, 5910–5918; weitere Beispiele sind in den Hintergrundinformationen aufgeführt..
- 34I. Oehme, O. S. Wolfbeis, Mikrochim. Acta 1997, 126, 177–192; C.-L. Hea, F.-L. Ren, X.-B. Zhang, Z.-X. Han, Talanta 2006, 70, 364–369; C. Cano-Raya, M. D. Fernández-Ramos, J. Gómez-Sánchez, L. F. Capitán-Vallvey, Sens. Actuators B 2006, 117, 135–142.
- 35B. M. Weidgans, C. Krause, I. Klimant, O. S. Wolfbeis, Analyst 2004, 129, 645–650; experimentelle Details sind in den Hintergrundinformationen enthalten.
- 361 ist ebenfalls photostabil und zeigt nach 15 min Bestrahlung mit 10.1 mW (bestrahlte Fläche von 0.5 cm2) bei 532 nm keine Zersetzung.
- 37K. Umezawa, K. Tohda, X. M. Lin, J. L. Sessler, Y. Umezawa, Anal. Chim. Acta 2001, 426, 19–32; J. L. Sessler, J. M. Davis, V. Král, T. Kimbrough, V. Lynch, Org. Biomol. Chem. 2003, 1, 4113–4123.
- 38R. Kumar, R. Misra, T. K. Chandrashekar, Org. Lett. 2006, 8, 4847–4850.
- 39Beide Merkmale sind entscheidend: die Hückel-[4n+2]-Aromatizität des [26]Chromophors und die zusätzlichen π-Elektronen entlang der [52]Trajektorie. Zudem können die nahezu in der Ebene liegenden meso-Substituenten ebenfalls wechselwirken. Wenn der [26]Kern durch Reduktion in einen [28]Kern umgewandelt wird, geht die Aromatizität verloren, was sich in drastischen hypso- und hypochromen Verschiebungen widerspiegelt (siehe die Hintergrundinformationen).
- 40RCA Electro-Optics Handbook, RCA Commercial Engineering, Harrison, NJ, 1974, S. 61–63.
- 41ITU-T Recommendations, Series G: Transmission Systems and Media, Digital Systems and Networks, Optical system design and engineering, Supplement 39, International Telecommunication Union (ITU), Genf, 2006, S. 5.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.