Rückgrat-verknüpfte Liganden erhöhen die Vielfalt in heteroleptischen Koordinationskäfigen
Abstract
Die Kombination von formkomplementären, bis-monodentaten Liganden LA und LB mit PdII-Kationen erlaubt das Selbstsortieren heteroleptischer Käfige der Formel cis-[Pd2LA2LB2]. Wir berichten, wie solche Gebilde durch die Einführung kovalenter Brücken zwischen den Rückgraten zweier LA-Einheiten diversifiziert werden können. Durch Lösungsmittel- und Gasteffekte wird gezeigt, dass die Flexibilität dieser Brücken die Zahl an Metallionen und Hohlräumen sowie die Topologie von vier Produkten bestimmt. Der Ligand LA1 mit flexiblem Linker reagiert in CH3CN mit seinem LB-Pendant zu einem vierkernigen Dimer (D1). In DMSO wird ein dreikerniger Pseudotetraeder T1 gebildet. Das Produkt von starrem LA2 mit LB ähnelt D1, jedoch mit rotierter Ligandanordnung (D2). In Gegenwart eines Gastes wandelt sich D2 in Prisma P2 um. Wir zeigen, wie die Steuerung des Koordinationsmodus eines Liganden strukturelle Differenzierung auslösen und somit die Komplexität in der Metall-vermittelten Selbstassemblierung erhöhen kann.
Multivalente Interaktionen, die die gleichzeitige Bindung eines größeren Moleküls an ein anderes über mehrere Kontaktstellen beschreiben, spielen in biologischen Systemen eine bedeutende Rolle.1 Die synthetische supramolekulare Chemie untersucht und nutzt multivalente Interaktionen, um große, selbstassemblierte Strukturen zu stabilisieren. In den letzten Jahrzehnten wurde über viele Beispiele solcher Systeme berichtet. Die meisten dieser Architekturen weisen hohe Symmetrien auf, die oft auf den Platonischen oder Archimedischen Körpern beruhen. Während die Natur Strukturen mit ähnlicher, modular aufgebauter Form hervorgebracht hat (z. B. Viruskapside und Eisenspeicherproteine), sind die meisten multivalenten Gebilde biologischen Ursprungs von eher geringer Symmetrie und gewöhnlich heteromultimer. Die Nachahmung solcher asymmetrischer biologischer Systeme durch künstliche Supramoleküle stellt eine Herausforderung für herkömmliche Assemblierungsstrategien dar.2 Rationales Design und Synthese von metallo-supramolekularen Produkten mit niedriger Symmetrie stehen in jüngster Zeit im Fokus mehrerer Forschungsgruppen. Dabei werden verschiedene, aber geometrisch zusammenpassende Liganden entwickelt, die über geeignete Metallionen miteinander verbunden werden. Die Schwierigkeit liegt in dem Ziel, eine einzige, integrativ selbstsortierte Spezies zu bilden, statt statistische Mischungen zu erzeugen oder narzisstische Trennung zu erleiden.3
In Bezug auf Koordinationskäfige bieten solche Ansätze das Potenzial, nanometergroße Objekte mit wohldefinierter Form, Größe und Ausstattung an funktionellen Gruppen zu konstruieren. Diese bieten die Möglichkeit, Substrate in ihrem Inneren selektiv zu erkennen und umzuwandeln. Die Bildung von Koordinationskäfigen mit asymmetrischem Hohlraum wurde kürzlich in einer Vielzahl von Studien vorangetrieben. Zum Beispiel berichtete Nitschke über den Aufbau heteroleptischer Architekturen, indem er starke π-Wechselwirkungen zwischen Liganden einsetzte.4 Yoshizawa5 und Fujita6 berichteten die exklusive Bildung heteroleptischer Wirt-Gast-Konstrukte auf Basis von Fullerenderivaten und großen aromatischen Ligandsystemen unter Verwendung spezifischer π-π-Interaktionen.
Andere Arbeiten zeigten, dass die Einführung subtiler Modifikationen an den Donorgruppen zur ausschließlichen Bildung heteroleptischer Gebilde mit zugänglichen Hohlräumen führen kann. Wir schlagen vor, diesen Ansatz “coordination-sphere engineering” zu nennen.7 So nutzte Crowley zum Beispiel Wasserstoffbrücken als sekundäre Wechselwirkungen zwischen Aminogruppen benachbarter Ligandeinheiten, um den Aufbau heteroleptischer Käfige zu steuern.8 Stang verwendete einen Ansatz zur Ladungstrennung, um heteroleptische PtII-basierte Systeme zu erhalten.9 Während Fujita Pionierarbeit bei der Installation von sterisch anspruchsvollen Methylsubstituenten an Arylliganden L des weit verbreiteten cis-[Pd(Ethylendiamin)L2]-Motivs leistete, haben wir kürzlich den Anwendungsbereich dieser Strategie erweitert. Dazu gruppierten wir vier Liganden vom Picolin-Typ mit abwechselnder Methylgruppenorientierung um “nackte” PdII-Kationen, um so heteroleptische cis-[Pd2L2L′2]-Strukturen zusammenzusetzen.10
Als besonders vielseitige Strategie für den Zusammenbau heteroleptischer Käfige hat sich die so genannte “Formkomplementarität” herausgestellt, wie Fujita,11 Mukherjee,3c Zhou,12 Stang,13 Chand14 und wir gezeigt haben.15 Diese Strategie nutzt die geometrische Passgenauigkeit von Liganden in Mehrkomponentensystemen, um den integrativen, sich selbst sortierenden Aufbau heteroleptischer Supramoleküle zu erlauben.
Mitglieder dieser neuen Klasse von Koordinationskäfigen, die aus mindestens zwei Ligandtypen aufgebaut sind, besitzen einen einzigen Hohlraum, der oft eine eher geringe Symmetrie aufweist. Da uns die Natur zeigt, dass viele biologische Wirte, z. B. Enzyme, mehrere Bindungstaschen enthalten (z. B. eine Substratbindungsstelle und einen Rezeptor für die allosterische Modulation), begannen wir uns für die Konstruktion von Systemen mit mehreren Kavitäten zu interessieren. Bisher können zwei Hauptstrategien unterschieden werden:16 Die erste verwendet multitope Liganden, z. B. tris- oder sogar tetrakis-monodentate Brücken, die mit geeigneten Metallen, z. B. quadratisch-planaren PdII-Kationen, zusammengefügt werden, um Konstrukte zu erhalten, die aus zwei oder mehr linear oder kreisförmig angeordneten Kavitäten gleicher Form und Größe bestehen. Beispiele für diese Art von Mehrfachkäfigsystemen wurden von Chand,17 Crowley,18 Yoshizawa19 und uns berichtet.20 Die andere Strategie beruht auf der Catenierung von Einzelkäfigen, um sich durchdringende Dimere oder Aggregate höherer Ordnung zu erhalten, die drei oder mehr Kavitäten von üblicherweise recht kleinem Volumen enthalten.20b, 21 Es wurden hingegen nur wenige Beispiele von Koordinationskäfigen berichtet, die mehrere Kavitäten unterschiedlicher Größe enthalten.22 Da solche Strukturen die Differenzierung von Gastspezies ermöglichen, z. B. im Rahmen kooperativ-heterotroper Rezeptoren, stimuli-responsiver Katalysatoren und logischer Gatter, besteht ein wachsendes Interesse an deren Konstruktion.23 Erst kürzlich berichtete Chand über eine Reihe neuartiger “Conjoined-Cages” mit mehreren, unterschiedlich großen Hohlräumen durch die periphere Dekoration einer zentralen, dreikernigen [Pd3L6]-Einheit mit einem, zwei und drei [Pd2L4]-Substituenten.24
Hier berichten wir über den Aufbau einer Familie von heteroleptischen Multikavität-Systemen durch Kombination von Formkomplementarität mit kovalenter Rücken-zu-Rücken-Verbrückung zweier Liganden.25 Zunächst zeigen wir, dass die Kombination des bananenförmigen, Carbazol-basierten Liganden LA mit dem vom Fluoren abgeleiteten Liganden LB einen neuen, heteroleptischen, cis-konfigurierten [Pd2LA2LB2]-Käfig C bildet (Hintergrundinformationen, Abbildungen S5–S11). Daraufhin entwarfen wir zwei Liganden LA1 und LA2, in welchen je ein Paar von LA-Einheiten über ihre Rückgrat-Stickstoffpositionen mit zwei verschiedenen Linkertypen verbunden sind. LA1 wurde durch Verwendung einer flexiblen Hexylenkette erhalten, und LA2 enthält einen starren Phenylenlinker. Überraschenderweise führte die Änderung der Flexibilität des Linkers dazu, dass die Größe, Form und Hohlraumanzahl der gebildeten, heteroleptischen Strukturen viel stärkere Variationen aufweist als erwartet (Abbildung 1).
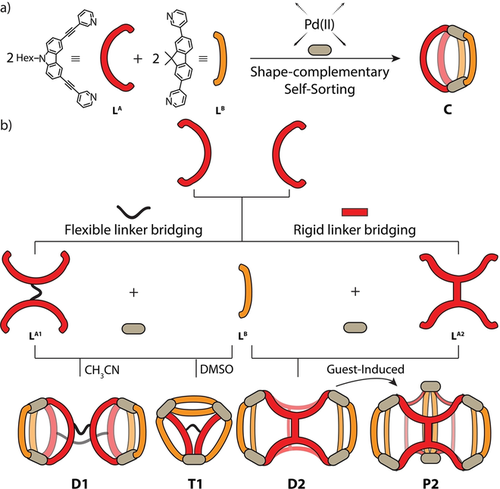
Heteroleptische Käfige mit unterschiedlichem Grad an struktureller Komplexität. a) Formkomplementäre Bildung eines cis-konfigurierten [Pd2LA2LB2]-Käfigs C; b) Einführung von Rückgratbrücken, kombiniert mit Formkomplementarität, ergibt eine Vielzahl von Mehrkavitäten-Systemen, deren Bildung durch ein Zusammenspiel von Brückenflexibilität, Lösungsmittel und anionischen Gästen kontrolliert wird.
Die Liganden LA1 und LA2 wurden durch vierfache Sonogashira-Kreuzkupplungsreaktionen ausgehend von entsprechenden tetra-iodierten Vorläufern synthetisiert (Abbildungen S1–S4). Zunächst wurde LA1 für die homoleptische Käfiganordnung mit [Pd(CH3CN)4](BF4)2 in DMSO[D6] bei Raumtemperatur getestet, was zur quantitativen Bildung einer einzelnen Spezies führte, wie durch 1H-NMR- und DOSY-Spektroskopie angezeigt (Abbildungen S12–S15). Die HR-ESI-Massenspektrometrie zeigte die Bildung eines zweikernigen Käfigs [Pd2(LA1)2] (C1), der höchstwahrscheinlich seinem nicht-verbrückten Vorgänger [Pd2(LA)4]26 ähnelt, aber mit jeweils kovalent verknüpften Paaren benachbarter, bis-monodentater Liganden (Abbildungen S16 und S46). Als nächstes untersuchten wir LB auf homoleptische Assemblierung in DMSO[D6] und erhielten eine 1:1-Mischung aus einem 3-gliedrigen Ring [Pd3(LB)6] (R) und einem [Pd4(LB)8]-Tetraeder (T),27 welche durch 1H-NMR und HR-ESI-MS identifiziert werden konnten (Abbildungen S17–S21). Dann kombinierten wir den verbrückten Liganden LA1 mit seinem formkomplementären Pendant LB,28 um die Bildung heteroleptischer Strukturen zu untersuchen. Unsere ersten Experimente mit CD3CN ergaben ein relativ kompliziertes NMR-Spektrum, was auf die Bildung einer Mischung aus mehreren Spezies hinweist. HR-ESI-MS deckte die Existenz von mindestens fünf Komponenten unterschiedlicher Ligandzusammensetzung auf, [Pd3(LB)6], [Pd4(LB)8], [Pd2(LA1)(LB)2], [Pd4(LA1)2(LB)4] und [Pd3(LA1)(LB)4], was höchstwahrscheinlich auf die hohe strukturelle Flexibilität von LA1 zurückzuführen ist (Abbildungen S22 und S23). Bemerkenswerterweise waren wir in der Lage, eine einzelne Spezies aus dieser Mischung durch Gasphasendiffusion von Ethylether in die CD3CN-Lösung zu kristallisieren. Die Struktur dieser Verbindung D1, die der Formel [Pd4(LA1)2(LB)4] entspricht, kann formal als ein Dimer der heteroleptischen Käfigmonomere C beschrieben werden, die durch zwei kettenförmige Verbindungsglieder Rücken-an-Rücken verbunden sind.29 Sie kristallisierte in der monoklinen Raumgruppe C2/c, ist von C2-Symmetrie und enthält nur die Hälfte des Dimers in der asymmetrischen Einheit. Der Pd⋅⋅⋅Pd-Abstand von 13.6 Å in jedem Käfigmonomer ist fast derselbe wie im heteroleptischen Mutterkäfig C (Abbildungen 4 a und S45). Neben den beiden C-ähnlichen Hohlräumen, die mit Acetonitril-Molekülen und BF4− Anionen besetzt sind, entsteht durch die enge Verbindung der beiden Käfigeinheiten ein weiterer, keilförmiger Raum, der von den Carbazolliganden beider Käfigeinheiten flankiert wird. Während dieser Hohlraum in erster Linie durch zwei koplanare aromatische Ligandpanele in etwa 6.8 Å Abstand definiert wird, konnten im Festkörper oder in Lösung keine eingelagerten Gäste gefunden werden (Abbildung S51).
Da Lösungsmitteleffekte eine bedeutende Rolle für den Ausgang einer supramolekularen Bildungsreaktion spielen können,30 waren wir daran interessiert herauszufinden, ob die Kombination von LA1 mit LB bei Verwendung von DMSO[D6] als Lösungsmittel zu einem anderen Produkt führt. Die 1H-NMR-Analyse ergab ein sehr kompliziertes, aber gut aufgelöstes Spektrum mit insgesamt 42 Signalen im Bereich δ=6.9–10.4 ppm (Abbildung 2 b). HR-ESI-MS zeigt eine Reihe von Signalen, die den Spezies [Pd3(LA1)(LB)4+n BF4](6−n)+ (n=0–4; Abbildung 3 a) zugeordnet werden konnten. Die DFT-basierte Modellierung legt nahe, dass zwei isomere, heteroleptische Strukturen der Formel [Pd3(LA1)(LB)4] mit völlig unterschiedlichen Topologien postuliert werden können (Abbildung S47). Im einen Fall würden beide Carbazolreste von LA1 dieselbe Kante eines 3-gliedrigen Rings R1 überspannen (beide anderen Kanten bestehen aus einem Paar von Liganden LB), während sich im anderen Fall eine Struktur T1 ergeben würde, bei der eine Kante durch ein Ligandenpaar LB verbunden wäre und zwei Kanten eine Kombination aus einem LB und einer bis-monodentaten Hälfte von LA1 aufweisen würden. Da dort die flexible Hexylenschleife von LA1 Platz auf einer Fläche der dreieckigen Basis einnehmen würde, die aus den verbundenen Liganden gebildet wird, nimmt die gesamte Struktur T1 eine pseudotetraedrische Form an. Eine sorgfältige Analyse der NMR-Aufspaltungsmuster und indikativer NOESY-Kreuzpeaks erlaubte es uns, die R1-Topologie auszuschließen (Abbildung 2 b, 4 c). Es gelang uns, alle 1H-NMR-Signale aus 2D-Spektren zuzuordnen (Abbildungen S26 und S27). Alle von LB stammenden Protonensignale sind in vier Sätze aufgeteilt, während sich für LA1 zwei Signalsätze ergeben. Die ausschließliche Bildung von T1 wurde durch ein 1H-DOSY-NMR-Spektrum verifiziert, welches zeigte, dass alle 42 Signale im aromatischen Bereich dem gleichen Diffusionskoeffizienten entsprechen, wobei der berechnete hydrodynamische Radius von 13.9 Å mit den Dimensionen der modellierten Struktur vergleichbar ist. Leider scheiterten alle Versuche, Einkristalle für T1 zu erhalten. Das DFT-Modell erwies sich jedoch als geeignet, die unterschiedlichen NMR-Signalaufspaltungen zu erklären, die für LA1 und LB beobachtet wurden. Das Modell zeigt, dass für den Liganden LA1 die oberen Hälften (braune Farbe) und die unteren Hälften (rote Farbe) aufgrund ihrer Anordnung entlang der Basis des 3-gliedrigen Rings unterschiedliche chemische Umgebungen ausgemacht werden können, was zu zwei Sätzen von NMR-Signalen führt (Abbildung 2 b, 4 b). Die Liganden LB, kombiniert mit den LA1-Einheiten an diesen Kanten, sind ebenfalls in zwei Hälften (blaue und violette Farbe) aufgeteilt. Darüber hinaus hat die Kante, die von zwei LB überspannt wird, unterscheidbare Ober- und Unterseiten (gelb und grün). Zusammengenommen können vier verschiedene chemische Umgebungen für LB erwartet werden, genau wie im experimentellen NMR-Spektrum beobachtet.
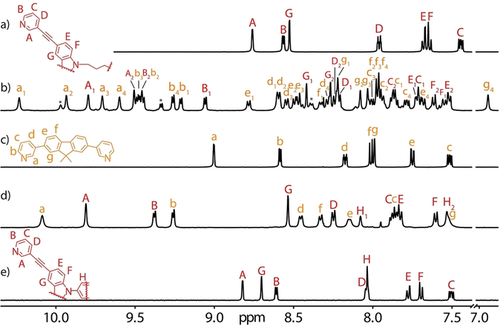
Partielle 1H-NMR-Spektren (500 MHz/DMSO[D6], 298 K) des heteroleptischen Pseudotetraeders [Pd3(LA1)(LB)4]6+ (T1) und Käfigdimers [Pd4(LA2)2(LB)4]8+ (D2) nebst freien Liganden. a) LA1; b) T1 (*=[Pd3(LB)6]6+ Ring R); c) LB; d) D2, erhalten durch Erhitzen einer 1:2:2-Mischung aus LA2, LB und PdII; e) LA2.
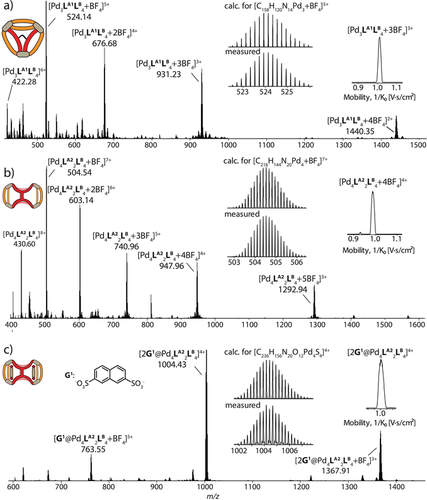
HR-ESI-Massenspektren von a) Pseudotetraeder T1; b) Käfigdimer D2 und c) Wirt-Gast-Komplex 2G1@D2. Die Einschübe zeigen Ionenmobilitätsspektren.
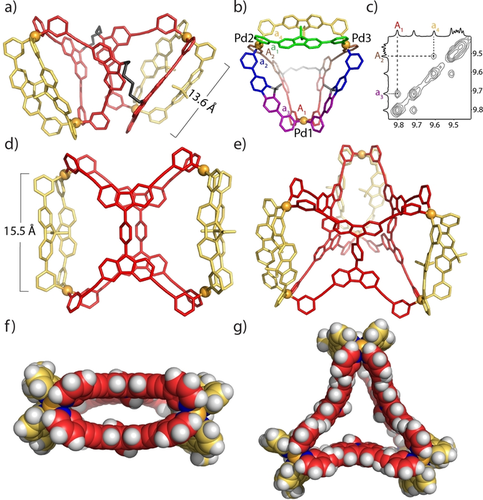
a) Röntgenstruktur von D1;34 b) DFT-optimiertes Modell von T1 (Farben zeigen unterschiedliche Ligandumgebungen); c) NOESY-NMR-Details zur Unterstützung der T1-Struktur; d) Seiten- und f) Draufsicht der Röntgenstrukturen von D234 und e) und g) von P2[34]; (G1, BF4−-Anionen und Lösungsmittelmoleküle wurden weggelassen).
Zusätzlich setzten wir die “Trapped Ion Mobility Spectrometry” in Verbindung mit hochauflösender ESI-TOF-Massenspektrometrie (ESI-TIMS-TOF) ein, um einen besseren Einblick in die Gasphasendimensionen der Struktur zu erhalten.31 Wir fanden heraus, dass die experimentell bestimmten Kollisionsquerschnitte (eCCS) tatsächlich besser zu den berechneten, theoretischen Werten (tCCS) der modellierten T1-Struktur passen als zu R1 (Tabelle S2). Eine solche heteroleptische, pseudotetraedrische Struktur ist nach unserem besten Wissen noch nie berichtet worden.
Anschließend untersuchten wir den Einsatz des Liganden LA2, mit starrem Phenylenlinker, für die Käfigmontage. Zunächst wurde die Bildung homoleptischer Spezies untersucht, was zu extrem verbreiterten NMR-Spektren in verschiedenen Lösungsmitteln führte. Dies ist ein Hinweis auf die Bildung polymerer Spezies, was angesichts der divergierenden Natur des starren, tetra-monodentaten Liganden nicht überraschend ist. Anschließend setzten wir die Liganden LA2 und LB mit PdII in einer 1:2:2-Mischung in DMSO[D6] oder DMF[D7] bei 80 °C für 8 h um, wobei wir nur einen Satz klarer Signale erhielten, die alle LA2 und LB zugeordnet werden konnten (Abbildung 2 d). Die Pyridylprotonensignale neben den Stickstoffdonoren auf beiden Liganden (HA, HB und Ha, Hb) haben sich im Vergleich zu den freien Liganden signifikant in den Tieffeldbereich bewegt, was auf PdII-Koordination hindeutet. 1H-DOSY bestätigte, dass alle Protonensignale zum gleichen Diffusionskoeffizienten gehören, mit einem hydrodynamischen Radius von 17.2 Å (Abbildung S34). Im NOESY-Spektrum wurden deutliche Kreuzpeaks zwischen den Protonen Ha und HA sowie zwischen Hb und HB beobachtet, was weiter zeigt, dass sowohl der Ligand LA2 als auch LB integrale Bestandteile der gleichen Struktur D2 sind (Abbildung S33). Die NMR-Integration der Protonensignale für HA, HB, Ha und Hb zeigt ein Verhältnis von 1:1:1:1. Interessanterweise sind die Protonensignale für den Phenylenlinker (HH1 und HH2) nicht mehr äquivalent.
HR-ESI-MS ergab eine Formel [Pd4(LA2)2(LB)4+n BF4](8−n)+ (n=1, 2) mit prominenten Peaks bei m/z 504.54 und 603.14 (Abbildung 3 b). Außerdem konnten wir durch langsame Gasphasendiffusion von Isopropylether in eine Lösung in DMF Einkristalle erhalten, die für die Röntgenstrukturanalyse geeignet waren. Die Verbindung D2 kristallisiert in der monoklinen Raumgruppe C2/m, wobei die asymmetrische Einheit nur ein Viertel der diskreten metallo-supramolekularen Anordnung enthält. Während die anfängliche visuelle Inspektion der Struktur eine hohe Ähnlichkeit von D2 mit D1 vermuten lässt, gibt es bei genauerem Hinsehen einen auffälligen Unterschied: Während Ligand LA1 in D1 die LB-Gegenstücke in der gleichen Weise bindet, wie es im zugrunde liegenden Käfig C beobachtet wurde, ist Ligand LA2 formal um 90° in seiner Hauptebene gedreht, wobei nun jeweils die Pyridin-Donor-Arme der beiden Rücken-an-Rücken verbundenen Teile des Liganden LA2 an LB binden (Abbildung 4 d). Der Abstand der Pd⋅⋅⋅Pd-Kationen, die an die gleichen LB-Liganden binden, beträgt für D2 15.5 Å im Vergleich zu 13.6 Å für D1, was auf die unterschiedlichen, formkomplementären Bindungsmodi zurückzuführen ist. Beide Einheiten von LA2 sind koplanar orientiert, und ihre zentralen Phenylengruppen drehen sich leicht relativ zu den Carbazol-Ebenen, um sterische Hinderung zu minimieren. Von jeder Phenylengruppe zeigt eine Kante in den zentralen Hohlraum und eine nach außen (Abbildung 4 f), was höchstwahrscheinlich zu der erwähnten NMR-Signalaufspaltung führt. Für jeden der beiden äußeren Teile der Struktur zeigt die geminale Dimethylgruppe an einem Liganden LB nach außen, während die andere Dimethylgruppe auf das Fluorenrückgrat des gegenüberliegenden LB zeigt, um CH⋅⋅⋅π-Interaktionen zu ermöglichen (ca. 2.9–3.3 Å).
Interessanterweise sind vier DMF-Lösungsmittelmoleküle in den beiden äußeren Hohlräumen verkapselt und interagieren mit den Pd-Komplexen über CH⋅⋅⋅O Wasserstoffbrücken zwischen der Carbonylgruppe des DMF und den Pyridin-C-H-Gruppen von D2 (Abbildung S55). Dies inspirierte uns dazu, die Wirt-Gast-Eigenschaften von D2 zu untersuchen, indem wir Gäste mit der Fähigkeit wählten, als Akzeptor von Wasserstoffbrücken zu fungieren. In Übereinstimmung mit unseren früheren Studien15a wurde 2,7-Naphthalindisulfonat (G1) welches der Form der äußeren Hohlräume ähnelt, als Gast aufgenommen. Tatsächlich ergab die NMR-Titration, dass sich mit zunehmender Menge an Gast die nach innen gerichteten Protonensignale HA und Ha signifikant ins Tieffeld verschieben, was eine Verkapselung von G1 in beiden Kavitäten von D2 impliziert (Abbildung S41). Die Signalverschiebung endete nach der Zugabe von 2 Äquivalenten an Gast (Δδ=0.36 bzw. 0.69), was auf ein gesättigtes Gleichgewicht mit einem Wirt/Gast-Verhältnis von 1:2 schließen lässt. Dies wurde durch das HR-ESI-MS-Spektrum verifiziert, in dem der auffälligste Peak bei m/z 1004.43 2G1@D2 zugeordnet werden konnte (Abbildung 3 c). Die Assoziationskonstanten wurden mit K1=(2.08±0.08)×103 und K2=(2.11±0.28)×103 m−1 für das erste bzw. das zweite Bindungsereignis berechnet (1H-NMR-Integration gemittelt über drei verschiedene Wirt/Gast-Verhältnisse).32 Der Kooperativitätsparameter α=4 K2/K1=4 deutet auf eine positiv-kooperative Bindung hin, was angesichts der Tatsache, dass der erste bis-anionische Gast die positive Gesamtladung des Komplexes reduziert, überraschend ist (Tabelle S1).33 Bei einem Versuch, Einkristalle des Wirt-Gast-Komplexes zu züchten, erhielten wir stattdessen unerwartet einen neuen heteroleptischen, prismatischen Käfig [Pd6(LA2)3(LB)6]12+ (P2). P2 kristallisiert in der triklinen Raumgruppe  mit einem ganzen Trimermolekül in der asymmetrischen Einheit. Der Assemblierungsmodus in Bezug auf LA ist ähnlich wie bei D2, und der durchschnittliche Pd⋅⋅⋅Pd-Abstand beträgt 15.3 Å (Abbildung S57). Unerwarteterweise wird G1 nicht von den drei Käfighohlräumen in der Festkörperstruktur eingefangen. Stattdessen werden benachbarte Trimere durch die Sulfonatgruppen von G1 über C-H⋅⋅⋅O-S-Wasserstoffbrücken und elektrostatische SO3−-zu-Pd2+-Wechselwirkungen verbrückt.
mit einem ganzen Trimermolekül in der asymmetrischen Einheit. Der Assemblierungsmodus in Bezug auf LA ist ähnlich wie bei D2, und der durchschnittliche Pd⋅⋅⋅Pd-Abstand beträgt 15.3 Å (Abbildung S57). Unerwarteterweise wird G1 nicht von den drei Käfighohlräumen in der Festkörperstruktur eingefangen. Stattdessen werden benachbarte Trimere durch die Sulfonatgruppen von G1 über C-H⋅⋅⋅O-S-Wasserstoffbrücken und elektrostatische SO3−-zu-Pd2+-Wechselwirkungen verbrückt.
Schließlich interessierte uns, ob diese heteroleptischen Systeme höherer Ordnung durch die Umlagerung homoleptischer Vorläufer gebildet werden können.15 Daher wurden C1 und das R/T-Gemisch in DMSO in einem Verhältnis von 3:4 kombiniert. Bei Raumtemperatur stellten wir fest, dass der Ligandenaustausch durch eine signifikante kinetische Barriere behindert wird. Das Erhitzen der Mischung auf 80 °C für 2 h führte gemäß den 1H-NMR-Spektren jedoch zur sauberen Bildung von T1 (Abbildungen 5, S38 und S39).
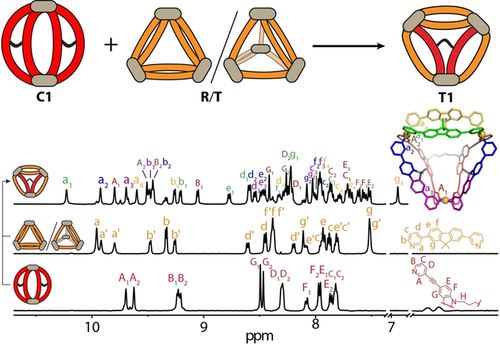
Käfig-zu-Käfig-Transformation von homoleptischem C1 und einer Mischung aus R und T zu heteroleptischem Pseudotetraeder T1.
Zusammenfassend berichten wir über eine neuartige Strategie für den Aufbau von heteroleptischen Mehrkavitätensystemen durch Verschmelzen von Liganden über deren Rückgrat. Die Topologie der gebildeten Produkte kann durch die Wahl des Linkers (starr oder flexibel), des Lösungsmittels und der Gäste moduliert werden. Die Reaktion mit dem flexibel überbrückten Liganden LA1 erwies sich als lösungsmittelabhängiger Prozess. Ein heteroleptischer Pseudo-Tetraeder T1, bestehend aus zwei verschiedenen Liganden, wurde zum ersten Mal in DMSO erhalten, während es uns gelang, aus CH3CN ein heteroleptisches Käfigdimer D1 zu kristallisieren. Die pseudotetraedrische Struktur ist auch über eine Käfig-zu-Käfig-Transformation zugänglich. Der mit starrem Linker verbrückte Ligand LA2 bildet Dimer D2, das kooperativ bis zu zwei Bis-Sulfonat-Gäste in seine beiden äußeren, identischen Hohlräume verkapseln kann, während ein Käfig-Trimer P2 durch Reorganisation während des Kristallisationsprozesses erhalten wurde. Unsere Strategie bietet die Grundlage für den Aufbau einer größeren Vielfalt an heteroleptischen Käfigen mit mehreren Kavitäten, wodurch die Komplexität solch supramolekularer Strukturen gesteigert werden und ihre Eigenschaften sowie Anwendungen profitieren sollten.
Acknowledgements
Wir danken dem Europäischen Forschungsrat (ERC Consolidator Grant 683083, RAMSES) und der Deutschen Forschungsgemeinschaft (DFG-Exzellenzcluster RESOLV – EXC 2033 – Projektnummer 390677874 und GRK2376 “Confinement-controlled Chemistry” – Projektnummer 331085229) für die finanzielle Unterstützung. Wir danken Laura Schneider für ESI-Massenspektrometrie-Messungen und Dr. Haeri Lee für hilfreiche Diskussionen. Open Access Veröffentlichung ermöglicht und organisiert durch Projekt DEAL.
Conflict of interest
Die Autoren erklären, dass keine Interessenkonflikte vorliegen.




