Mischungen konfigurationsstabiler und fluxionaler atropisomerer einzähniger P-Liganden in der asymmetrischen Rh-katalysierten Olefin-Hydrierung†
Manfred T. Reetz Prof. Dr.
Max-Planck-Institut für Kohlenforschung, Kaiser-Wilhelm-Platz 1, 45470 Mülheim/Ruhr, Deutschland, Fax: (+49) 208-306-2985
Search for more papers by this authorXiaoguang Li Dr.
Max-Planck-Institut für Kohlenforschung, Kaiser-Wilhelm-Platz 1, 45470 Mülheim/Ruhr, Deutschland, Fax: (+49) 208-306-2985
Search for more papers by this authorManfred T. Reetz Prof. Dr.
Max-Planck-Institut für Kohlenforschung, Kaiser-Wilhelm-Platz 1, 45470 Mülheim/Ruhr, Deutschland, Fax: (+49) 208-306-2985
Search for more papers by this authorXiaoguang Li Dr.
Max-Planck-Institut für Kohlenforschung, Kaiser-Wilhelm-Platz 1, 45470 Mülheim/Ruhr, Deutschland, Fax: (+49) 208-306-2985
Search for more papers by this authorWir danken dem Fonds der Chemischen Industrie für die großzügige Unterstützung.
Graphical Abstract
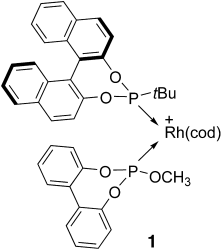
Gemischte (Prä)katalysatoren wie 1 entstehen, wenn [Rh(cod)2]BF4 mit 1:1-Mischungen aus von 2,2′-Dihydroxy-1,1′-binaphthyl (BINOL) abgeleiteten einzähnigen Phosphonit- oder Phosphit-Liganden und konfigurationslabilen atropisomeren Phosphiten mit Biphenol-Rückgrat kombiniert wird. Die Systeme liefern ausgezeichnete Ergebnisse bei der Rh-katalysierten asymmetrischen Hydrierung von β-Acylaminoacrylaten. cod=Cycloocta-1,5-dien.
References
- 1
- 1aM. T. Reetz, G. Mehler, Angew. Chem. 2000, 112, 4047–4049;
10.1002/1521-3757(20001103)112:21<4047::AID-ANGE4047>3.0.CO;2-Z Google ScholarAngew. Chem. Int. Ed. 2000, 39, 3889–3890;10.1002/1521-3773(20001103)39:21<3889::AID-ANIE3889>3.0.CO;2-T CAS PubMed Web of Science® Google Scholar
- 1bM. T. Reetz, G. Mehler, A. Meiswinkel, Patentanmeldung, WO 01/94278A1, 2001.
- 2
- 2aM. T. Reetz, T. Sell, Tetrahedron Lett. 2000, 41, 6333–6336;
- 2bC. Claver, E. Fernandez, A. Gillon, K. Heslop, D. J. Hyett, A. Martorell, A. G. Orpen, P. G. Pringle, Chem. Commun. 2000, 961–962.
- 3M. van den Berg, A. J. Minnaard, E. P. Schudde, J. van Esch, A. H. M. de Vries, J. G. de Vries, B. L. Feringa, J. Am. Chem. Soc. 2000, 122, 11 539–11 540.
- 4
- 4aK. Junge, B. Hagemann, S. Enthaler, G. Oehme, M. Michalik, A. Monsees, T. Riermeier, U. Dingerdissen, M. Beller, Angew. Chem. 2004, 116, 5176–5179;
10.1002/ange.200460190 Google ScholarAngew. Chem. Int. Ed. 2004, 43, 5066–5069;
- 4bI. V. Komarov, A. Börner, Angew. Chem. 2001, 113, 1237–1240;
10.1002/1521-3757(20010401)113:7<1237::AID-ANGE1237>3.0.CO;2-Z Google ScholarAngew. Chem. Int. Ed. 2001, 40, 1197–1200;10.1002/1521-3773(20010401)40:7<1197::AID-ANIE1197>3.0.CO;2-G CAS PubMed Web of Science® Google Scholar
- 4cM. Ostermeier, J. Prieß, G. Helmchen, Angew. Chem. 2002, 114, 625–628;
10.1002/1521-3757(20020215)114:4<625::AID-ANGE625>3.0.CO;2-E Google ScholarAngew. Chem. Int. Ed. 2002, 41, 612–617;
- 4dY. Chi, X. Zhang, Tetrahedron Lett. 2002, 43, 4849–4852;
- 4eW. Chen, J. Xiao, Tetrahedron Lett. 2001, 42, 8737–8740;
- 4fH. Huang, Z. Zheng, H. Luo, C. Bai, X. Hu, H. Chen, J. Org. Chem. 2004, 69, 2355–2361;
- 4gA.-G. Hu, Y. Fu, J.-H. Xie, H. Zhou, L.-X. Wang, Q.-L. Zhou, Angew. Chem. 2002, 114, 2454–2456;
Angew. Chem. Int. Ed. 2002, 41, 2348–2350;
10.1002/1521-3773(20020703)41:13<2348::AID-ANIE2348>3.0.CO;2-K CAS PubMed Web of Science® Google Scholar
- 4hZ. Pakulski, O. M. Demchuk, J. Frelek, R. Luboradzki, K. M. Pietrusiewicz, Eur. J. Org. Chem. 2004, 3913–3918;
- 4iT. Jerphagnon, J.-L. Renaud, C. Bruneau, Tetrahedron: Asymmetry 2004, 15, 2101–2111;
- 4jF. Lagasse, H. B. Kagan, Chem. Pharm. Bull. 2000, 48, 315–324;
- 4kJ. Ansell, M. Wills, Chem. Soc. Rev. 2002, 31, 259–268.
- 5A. Meiswinkel, Dissertation, Ruhr-Universität Bochum, 2003
- 6
- 6aM. T. Reetz, T. Sell, A. Meiswinkel, G. Mehler, Angew. Chem. 2003, 115, 814–817;
10.1002/ange.200390178 Google ScholarAngew. Chem. Int. Ed. 2003, 42, 790–793;
- 6bM. T. Reetz, Chim. Oggi 2003, 21, 5–8; siehe auch
- 6cD. Peña, A. J. Minnaard, J. A. F. Boogers, A. H. M. de Vries, J. G. de Vries, B. L. Feringa, Org. Biomol. Chem. 2003, 1, 1087–1089.
- 7M. T. Reetz, G. Mehler, Tetrahedron Lett. 2003, 44, 4593–4596.
- 8M. T. Reetz, X. Li, Tetrahedron 2004, 60, 9709–9714, sowie dort zitierte Literatur über vorangegangene Arbeiten zur Hydrierung von 3.
- 9Hier sind Daten für nur etwa die Hälfte der kombinatorischen Suche aufgeführt. Kombinationen des Phosphonits 1 (X=CH3) mit 2 oder 5–11 führen dagegen nicht zu positiven Effekten.
- 10Wir haben früher schon zeigen können, dass bestimmte Diphosphite aus einem chiralen Diol als Rückgrat und fluxionalen atropisomeren Biphenol-Derivaten bei Olefin-Hydrierungen bis zu 99 % ee liefern können, wobei drei rasch ineinander übergehende Diastereomere beteiligt sind:
- 10aM. T. Reetz, T. Neugebauer, Angew. Chem. 1999, 111, 134–137;
10.1002/(SICI)1521-3757(19990115)111:1/2<134::AID-ANGE134>3.0.CO;2-2 Google ScholarAngew. Chem. Int. Ed. 1999, 38, 179–181;
- 10bD. G. Blackmond, T. Rosner, T. Neugebauer, M. T. Reetz, Angew. Chem. 1999, 111, 2333–2335;
10.1002/(SICI)1521-3757(19990802)111:15<2333::AID-ANGE2333>3.0.CO;2-7 Google ScholarAngew. Chem. Int. Ed. 1999, 38, 2196–2199. Verwandte Effekte:10.1002/(SICI)1521-3773(19990802)38:15<2196::AID-ANIE2196>3.0.CO;2-9 CAS PubMed Web of Science® Google Scholar
- 10cK. Mikami, T. Korenaga, M. Terada, T. Ohkuma, T. Pham, R. Noyori, Angew. Chem. 1999, 111, 517–519;
10.1002/(SICI)1521-3757(19990215)111:4<517::AID-ANGE517>3.0.CO;2-E Google ScholarAngew. Chem. Int. Ed. 1999, 38, 495–497;10.1002/(SICI)1521-3773(19990215)38:4<495::AID-ANIE495>3.0.CO;2-O CAS PubMed Web of Science® Google Scholar
- 10dM. Diéguez, S. Deerenberg, O. Pàmies, C. Claver, P. W. N. M. van Leeuwen, P. Kamer, Tetrahedron: Asymmetry 2000, 11, 3161–3166;
- 10eJ. W. Faller, A. R. Lavoie, J. Parr, Chem. Rev. 2003, 103, 3345–3367;
- 10fP. J. Walsh, A. E. Lurain, J. Balsells, Chem. Rev. 2003, 103, 3297–3344;
- 10gK. Mikami, M. Yamanaka, Chem. Rev. 2003, 103, 3369–3400;
- 10hM. Diéguez, O. Pàmies, A. Ruiz, S. Castillón, C. Claver, Chem. Eur. J. 2001, 7, 3086–3094;
10.1002/1521-3765(20010716)7:14<3086::AID-CHEM3086>3.0.CO;2-O CAS PubMed Web of Science® Google Scholar
- 10iZ. Luo, Q. Liu, L. Gong, X. Cui, A. Mi, Y. Jiang, Angew. Chem. 2002, 114, 4714–4717;
Angew. Chem. Int. Ed. 2002, 41, 4532–4535;
10.1002/1521-3773(20021202)41:23<4532::AID-ANIE4532>3.0.CO;2-5 CAS PubMed Web of Science® Google Scholar
- 10jA. Suárez, A. Pizzano, Tetrahedron: Asymmetry 2001, 12, 2501–2504;
- 10kT. Ooi, Y. Uematsu, M. Kameda, K. Maruoka, Angew. Chem. 2002, 114, 1621–1624;
10.1002/1521-3757(20020503)114:9<1621::AID-ANGE1621>3.0.CO;2-5 Google ScholarAngew. Chem. Int. Ed. 2002, 41, 1551–1554;10.1002/1521-3773(20020503)41:9<1551::AID-ANIE1551>3.0.CO;2-L CAS PubMed Web of Science® Google Scholar
- 10lC. Monti, C. Gennari, U. Piarulli, Tetrahedron Lett. 2004, 45, 6859–6862;
- 10mH. Horibe, K. Kazuta, M. Kotoku, K. Kondo, H. Okuno, Y. Murakami, T. Aoyama, Synlett 2003, 2047–2051;
- 10nK. Tissot-Croset, D. Polet, A. Alexakis, Angew. Chem. 2004, 116, 2480–2482;
10.1002/ange.200353744 Google ScholarAngew. Chem. Int. Ed. 2004, 43, 2426–2428, zit. Lit.
- 11Dabei bieten beispielsweise Mischungen aus den Phosphoramiditen 1 (X=NR2) und fluxionalen atropisomeren Phosphoramiditen (die wir aus Biphenol und Aminen wie Dimethylamin oder Piperidin hergestellt haben) interessante Perspektiven.
- 12Eine weitere Arbeit zur kombinatorischen Katalyse: M. T. Reetz, X. Li, Angew. Chem. 2005, 117, 3022; Angew. Chem. Int. Ed. 2005, 44, 2962.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.