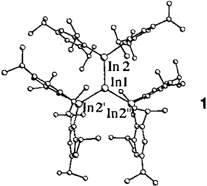
In(InTrip2)3: ein neuartiger In4-Cluster mit kurzen In-In-Bindungen und trigonal-planarer Geometrie†
Corresponding Author
Dr. Penelope J. Brothers
Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Penelope J. Brothers, Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Philip P. Power, Department of Chemistry, University of California Davis, CA 95616 (USA)
Search for more papers by this authorKlaus Hübler
Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Search for more papers by this authorDr. Ute Hübler
Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Search for more papers by this authorDr. Bruce C. Noll
Department of Chemistry, University of California Davis, CA 95616 (USA)
Search for more papers by this authorDr. Marilyn M. Olmstead
Department of Chemistry, University of California Davis, CA 95616 (USA)
Search for more papers by this authorCorresponding Author
Prof. Philip P. Power
Department of Chemistry, University of California Davis, CA 95616 (USA)
Penelope J. Brothers, Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Philip P. Power, Department of Chemistry, University of California Davis, CA 95616 (USA)
Search for more papers by this authorCorresponding Author
Dr. Penelope J. Brothers
Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Penelope J. Brothers, Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Philip P. Power, Department of Chemistry, University of California Davis, CA 95616 (USA)
Search for more papers by this authorKlaus Hübler
Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Search for more papers by this authorDr. Ute Hübler
Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Search for more papers by this authorDr. Bruce C. Noll
Department of Chemistry, University of California Davis, CA 95616 (USA)
Search for more papers by this authorDr. Marilyn M. Olmstead
Department of Chemistry, University of California Davis, CA 95616 (USA)
Search for more papers by this authorCorresponding Author
Prof. Philip P. Power
Department of Chemistry, University of California Davis, CA 95616 (USA)
Penelope J. Brothers, Department of Chemistry, The University of Auckland Private Bag 92019, Auckland (Neuseeland) Telefax: Int. + 64/9373 7422
Philip P. Power, Department of Chemistry, University of California Davis, CA 95616 (USA)
Search for more papers by this authorDiese Arbeit wurde von der U.S. National Science Foundation unterstützt. P. J. B. dankt der University of Auckland für ein Freisemester und K. H. der Alexander-von-Humboldt-Stiftung für ein Feodor-Lynen-Stipendium.
Abstract
Trigonal-planar umgeben ist das Indiumzentrum in In(InTrip2)3 1 (Trip = 2, 4, 6-iPr3C6H2), dem ersten Indan mit drei außergewöhnlich kurzen Bindungen zu Indanylsubstituenten. Die Verbindung wird durch Reduktion des Diindans Trip2 In- InTrip2 mit Lithium erhalten. Im Gegensatz dazu reagieren die Aluminium- und Galliumanaloga zu (Trip2M…MTrip2)−-Ionen, deren M-M-Bindung eine π-Bindungsordnung von 0.5 aufweist.
References
- 1
Übersichtsartikel: a)
M. J. Taylor,
P. J. Brothers
in
Chemistry of Aluminium. Gallium, Indium and Thallium
(Hrsg.: A. J. Downs),
Blackie-Chapman-Hall, London,
1993,
Kap. 3;
b)
P. J. Brothers,
P. P. Power,
Adv. Organomet. Chem.
1996,
39,
1;
c)
W. Uhl,
Angew. Chem.
1993,
105,
1449;
Angew. Chem. Int. Ed. Engl.
1993,
32,
1386;
d)
C. Dohmeier,
D. Loos,
H. Schnöckel,
Angew. Chem. Int. Ed. Engl.
1996,
108,
141 bzw.
10.1002/ange.19961080204 Google ScholarAngew. Chem. Int. Ed. Engl. 1996, 35, 129.
- 2 R. D. Schluter, A. H. Cowley, D. A. Atwood, R. A. Jones, M. R. Bond, C. J. Carrano, J. Am. Chem. Soc. 1993, 115, 2070.
- 3 M. Veith, F. Goffing, S. Becker, V. Huch, J. Organomet. Chem. 1991, 406, 105.
- 4 W. Uhl, M. Layh, W. Hiller, J. Organomet. Chem. 1989, 368, 139.
- 5
N. Wiberg,
K. Amelunxen,
H. Nöth,
M. Schmidt,
H. Schwenk,
Angew. Chem.
1996,
108,
110;
10.1002/ange.19961080126 Google ScholarAngew. Chem. Int. Ed. Engl. 1996, 35, 65.
- 6 S. Henkel, K. W. Klinkhammer, W. Schwarz, Angew. Chem. 1994, 106, 721; Angew. Chem. Int. Ed. Engl. 1994, 33, 681.
- 7a) X. He, R. A. Bartlett, M. M. Olmstead, K. Ruhlandt-Senge, B. E. Sturgeon, P. P. Power, Angew. Chem. 1993, 105, 761; Angew. Chem. Int. Ed. Engl. 1993, 32, 717; b) R. J. Wehmschulte, K. Ruhlandt-Senge, M. M. Olmstead, H. Hope, B. E. Sturgeon, P. P. Power, Inorg. Chem. 1993, 32, 2983.
- 8a) W. Uhl, R. Graupner, M. Layh, U. Schütz, J. Organomet. Chem. 1995, 493 C1; b) R. D. Schluter, A. H. Cowley, D. A. Atwood, R. A. Jones, J. L. Atwood, J. Coord. Chem. 1993, 30, 25.
- 9 O. T. Beachley, Jr., M. R. Churchill, J. C. Fettinger, J. C. Pazik, L. Victoriano, J. Am. Chem. Soc. 1986, 108, 4666.
- 10 M. Mocker, C. Robl, H. Schnöckel, Angew. Chem. 1994, 106, 1860; Angew. Chem. Int. Ed. Engl. 1994, 33, 1754.
- 11 X.-W. Li, W. T. Pennington, G. H. Robinson, J. Am. Chem. Soc. 1995, 117, 7578.
- 12
G. Linti,
W. Köstler,
Angew. Chem.
1996,
108,
593;
10.1002/ange.19961080521 Google ScholarAngew. Chem. Int. Ed. Engl. 1996, 35, 550.
- 13 D. Loos, H. Schnöckel, D. Fenske, Angew. Chem. 1993, 105, 1124; Angew. Chem. Int. Ed. Engl. 1993, 32, 1059.
- 14 Kristallstrukturanalyse von 1: C62H92In2: Mr = 1067.05, orthorhombisch, Raumgruppe Ccca, T = 130 K, a = 13.523(3), b = 24.257(7), c = 19.264(5) Å, V = 6319(3) Å3, Z = 4, Qber. = 1.122 g cm−3, F(000) = 2248, ä(MoKα) = 0.762 mm−1. Geeignete Einkristalle (0.16 × 0.24 × 0.32 mm3) wurden durch Umkristallisieren aus Hexan erhalten. Siemens-R3m/V-Diffraktometer mit MoKα-Strahlung (Λ = 0.71069 Å); ω-Scan. 3987 Reflexe mit 0 < 2θ 55°, davon 3637 unabhängig. Mit 2198 beobachteten Reflexen (Fo > 4° (Fo)) wurden 143 Parameter verfeinert. R = 0.066, Rw = 0.079, GooF = 0.88. Minimale und maximale Restelektronendichte: - 0.99 und 1.52 e Å−3. Die Struktur wurde mit Patterson-Methoden gelöst und nach F verfeinert (SHELXTL Plus). Eine Isopropylgruppe ist fehlgeordnet und wurde mit zwei Sätzen von Methyl-Kohlenstoffatomen mit einem relativen Besetzungsgrad von 3 zu 2 und gleicher relativer Geometrie jedoch freien Auslenkungsparametern verfeinert. Alle Nichtwasserstoffatome, mit Ausnahme der fehlgeordneten Methylgruppen, wurden anisotrop verfeinert; Wasserstoffatome wurden auf berechneten Lagen oder nach einem Reitermodell isotrop verfeinert. Absorptionskorrektur mit der Prozedur XABS (0.83 < T < 0.90).
- 15 Kristallstrukturanalyse von 2 · 3Et2O: C102H168In4O3: Mr = 1901.73, hexagonal, Raumgruppe R3, T = 130 K, a = 17.804(1), c = 28.806(4) Å, V = 7907.7(13) Å3, Z = 3, Qber. = 1.198 g cm−3, F(000) = 3000, ä(CuKα) = 7.215 mm−1. Geeignete Einkristalle (0.6 × 0.3 × 0.2 mm3) wurden durch Umkristallisieren aus Diethylether erhalten. Siemens-Vierkreisdiffraktometer-P4 mit CuKα-Strahlung (Λ = 1.54178 Å); 2°-Scan. 2499 Reflexe mit 3.3 ° ⩽ 49.9°, davon 2019 unabhängig. Mit 1994 beobachteten Reflexen und 3 Restraints wurden 286 Parameter verfeinert. wR2 = 0.158, R1 = 0.064 (für 1225 Reflexe mit Fo > 4° (Fo)), GooF = 1.04. Minimale und maximale Restelektronendichte: −0.27 und 0.43 e Å−3. Die Struktur wurde mit Patterson-Methoden gelöst (SHELXTL Plus) und nach F2 verfeinert (SHELXL93). Alle Nichtwasserstoffatome, mit Ausnahme der Atome des Solvensmoleküls, wurden anisotrop verfeinert; Wasserstoffatome wurden in berechneten Lagen oder nach einem Reitermodell (CH3) isotrop verfeinert. Absorptionskorrektur mit der Prozedur Difabs (0.747 < T < 1.000). Die kristallographischen Daten (ohne Strukturfaktoren) der in dieser Veröffentlichung beschriebenen Strukturen wurden als „supplementary publication no. CCDC-179-88”︁ beim Cambridge Crystallographic Data Centre hinterlegt. Kopien der Daten können kostenlos bei folgender Adresse angefordert werden: The Director, CCDC, 12 Union Road, GB-Cambridge CB2 1EZ (Telefax: Int. + 1223/336033; E-mail: [email protected]).
- 16 Drei fehlgeordnete Diethylethermoleküle je In(InTrip2)3 2 befinden sich in Hohlräumen der Struktur. Die Möglichkeit, daß ein fehlgeordnetes Lithiumkation mit den Diethylethermolekülen verknüpft ist, steht im Gegensatz zur Farbe von 2, die typisch für neutrale Organoindium-Verbindungen ist und der von 1 sehr ähnelt. In der Kristallstruktur konnte kein Lithiumkation lokalisiert werden.
- 17 L. R. Sita, Adv. Organomet. Chem. 1995, 38, 189.
- 18 J. Donohue, The Structures of the Elements, Wiley, New York, 1974, S. 244.
- 19 H. Schumann, C. Janiak, F. Görlitz, J. Loebel, A. Dietrich, J. Organomet. Chem. 1989, 363, 243.
- 20 H. Mattausch, A. Simon, E.-M. Peters, Inorg. Chem. 1986, 25, 3428.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.