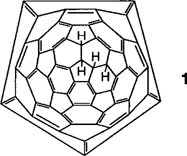
C60H4: Kinetik und Thermodynamik der mehrfachen Addition an C60 †
Dr. Craig C. Henderson
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624
Search for more papers by this authorDr. Celeste Mcmichael Rohlfing
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624
Search for more papers by this authorDr. Roger A. Assink
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624
Search for more papers by this authorCorresponding Author
Dr. Paul A. Cahill
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624Search for more papers by this authorDr. Craig C. Henderson
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624
Search for more papers by this authorDr. Celeste Mcmichael Rohlfing
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624
Search for more papers by this authorDr. Roger A. Assink
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624
Search for more papers by this authorCorresponding Author
Dr. Paul A. Cahill
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624
Chemistry of Organic Materials, Sandia National Laboratories Albuquerque, NM 87185-0368 (USA) Telefax: Int. + 505/844-9624Search for more papers by this authorDiese Arbeit wurde vom US Department of Energy (Laboratory Directed Research and Development Program, DE-AC04-94AL85000) gefördert.
Abstract
References
- 1 Zu C60XY siehe a) C. C. Henderson, P. A. Cahill, Science 1993, 259, 1885; b) A. Hirsch, A. Soi, H. R. Karfunkel, Angew. Chem. 1992, 104, 808; Angew. Chem. Int. Ed. Engl. 1992, 31, 766; c) A. Hirsch, T. Grosser, A. Skiebe, A. Soi, Chem. Ber. 1993, 126, 1061; d) N. Matsuzawa, D. A. Dixon, T. Fukunaga, J. Phys. Chem. 1992, 96, 7594; e) C. C. Henderson, P. A. Cahill, Chem. Phys. Lett. 1992, 198, 570; f) S. Ballenweg, R. Gleiter, W. Krätschmer, Tetrahedron Lett. 1993, 34, 3737.
- 2 Zu C70XY siehe Lit [7]; H. R. Karfunkel, A. Hirsch, Angew. Chem. 1992, 104, 1529; Angew. Chem. Int. Ed. Engl. 1992, 31, 1468; Lit [1c]; C. C. Henderson, C. M. Rohlfing, P. A. Cahill, Vorgestellt bei der Tagung der American Chemical Society, August 1993.
- 3 Eine neue übersicht zur Chemie der Fullerene: R. Taylor, D. R. M. Walton, Nature 1963, 363, 685; siehe auch A. Hirsch, Angew. Chem. 1993, 105, 1189; Angew. Chem. Int. Ed. Engl. 1993, 32, 1138.
- 4 Die Numerierung entspricht der in Abb. 2 in R. Taylor, J. Chem. Soc. Perkin Trans. 2 1993, 813:
- 5 Die Isolierung von 1 wurde zunächst auf der Frühjahrstagung der Materials Research Society vorgestellt, San Francisco, CA, USA, April 1993. Auch die Bildung einiger C60H4- und C70H4-Isomere durch die Reduktion mit Diimid wurde beschrieben: R. Taylor, Vorgetragen auf der Tagung der American Chemical Society, August 1993; A. G. Avent, A. D. Darwish, D. K. Heimbach, H. W. Kroto, M. F. Meidine, J. P. Parsons, C. Remars, R. Roers, O. Ohashi, R. Taylor, D. R. M. Walton, J. Chem. Soc. Perkin Trans. 2 1994, 15. In Tabelle 1 dieser Veröffentlichung sollte Isomer 1,2,57,58 durch 1,2,55,60 ersetzt werden. Wir danken R. Taylor für einen Vorabdruck dieser Arbeit.
- 6 N. Matsuzawa, T. Fukunaga, D. A. Dixon, J. Phys. Chem. 1992, 96, 10747.
- 7 C. C. Henderson, C. M. Rohlfing, P. A. Cahill, Chem. Phys. Lett. 1993, 213, 383.
- 8 Für die Gleichgewichtseinstellung zwischen 7,8- und 1,9-C70H2 wurde eine sehr gute übereinstimmung zwischen der exprimentell bestimmten Differenz der Freien Energien (1.4 ± 0.2 kcal mol−1) und der Differenz der HF/6-31G*-Gesamtenergien (1.3 kcal mol−1) erzielt: C. C. Henderson, C. M. Rohlfing, K. T. Gillen, P. A. Cahill, Science, im Druck. Das 1,9-Isomer ist sowohl das Produkt der kinetisch kontrollierten Hydroborierung/Hydrolyse als auch das thermodynamisch stabilste Isomer.
- 9 GAUSSIAN 92: M. J. Frisch, G. W. Trucks, M. Head-Gordon, P. M. W. Gill, M. W. Wong, J. B. Foresman, B. G. Johnson, H. B. Schlegel, M. A. Robb, E. S. Replogle, R. Gomberts, J. L. Andres, K. Raghavachari, J. S. Binkley, C. Gonzalez, R. L. Martin, D. J. Fox, D. J. DeFrees, J. Baker, J. J. P. Stewart, J. A. Pople, Gaussian Inc., Pittsburgh, PA, USA, 1992.
- 10 Die relativen Energien anderer C60H4-Isomere, besonders derjenigen mit einem 1,4-Additionmuster, können innerhalb des Bereichs der Energien der Isomere liegen, die in Tabelle 1 aufgelistet sind.
- 11 C. J. Welch, W. H. Pirkle, J. Chromatogr. 1992, 609, 89.
- 12 L. M. Jackman, S. Sternhell, Applications of Nuclear Magnetic Resonance Spectroscopy in Organic Chemistry, 2. Aufl., Pergamon, Oxford, 1969, S. 336.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.