Enzymatische Synthese chiraler C4-Bausteine aus meso-Weinsäure
Abstract
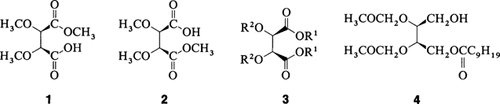
Letzlich aus Maleinsäure sind die optisch aktiven C4-Bausteine 1, 2 und 4 im 10 mmol-Maßstab zugänglich. 1 und 2 werden aus dem O-methylierten meso-Weinsäuredimethylester 3 (R1 = R2 = CH3) durch Verseifung entweder an der pro-R-oder der pro-S-Estergruppe erhalten, wobei als Enzyme Schweineleber-Esterase (als Schweineleber-Aceton-Puder) bzw. Lipase aus Candida cylindricea eingesetzt werden. 4 wird aus einem Reduktionsprodukt von 3 durch enzymatische Acylierung erhalten. Chemische Ausbeuten und ee-Werte liegen bei allen Reaktionen über 90%.