Nicht-kovalente bindende Wechselwirkungen zwischen Tetraphenylborat-Anionen und Paraquat- oder Diquat-Dikationen†
Dr. Gwilym J. Moody
Department of Applied Chemistry, PO Box 13, UWIST Cardiff CF1 3XF (Großbritannien)
Search for more papers by this authorDr. Richard K. Owusu
Department of Applied Chemistry, PO Box 13, UWIST Cardiff CF1 3XF (Großbritannien)
Search for more papers by this authorAlexandra M. Z. Slawin
Chemical Crystallography Laboratory Department of Chemistry, Imperial College London SW7 2AY (Großbritannien)
Search for more papers by this authorNeil Spencer
Department of Chemistry, The University Sheffield S3 7HF (Großbritannien)
Search for more papers by this authorCorresponding Author
J. Fraser Stoddart
Department of Chemistry, The University Sheffield S3 7HF (Großbritannien)
Department of Chemistry, The University Sheffield S3 7HF (Großbritannien)Search for more papers by this authorDr. J. D. Ronald Thomas
Department of Applied Chemistry, PO Box 13, UWIST Cardiff CF1 3XF (Großbritannien)
Search for more papers by this authorDr. David J. Williams
Chemical Crystallography Laboratory Department of Chemistry, Imperial College London SW7 2AY (Großbritannien)
Search for more papers by this authorDr. Gwilym J. Moody
Department of Applied Chemistry, PO Box 13, UWIST Cardiff CF1 3XF (Großbritannien)
Search for more papers by this authorDr. Richard K. Owusu
Department of Applied Chemistry, PO Box 13, UWIST Cardiff CF1 3XF (Großbritannien)
Search for more papers by this authorAlexandra M. Z. Slawin
Chemical Crystallography Laboratory Department of Chemistry, Imperial College London SW7 2AY (Großbritannien)
Search for more papers by this authorNeil Spencer
Department of Chemistry, The University Sheffield S3 7HF (Großbritannien)
Search for more papers by this authorCorresponding Author
J. Fraser Stoddart
Department of Chemistry, The University Sheffield S3 7HF (Großbritannien)
Department of Chemistry, The University Sheffield S3 7HF (Großbritannien)Search for more papers by this authorDr. J. D. Ronald Thomas
Department of Applied Chemistry, PO Box 13, UWIST Cardiff CF1 3XF (Großbritannien)
Search for more papers by this authorDr. David J. Williams
Chemical Crystallography Laboratory Department of Chemistry, Imperial College London SW7 2AY (Großbritannien)
Search for more papers by this authorDiese Arbeit wurde vom Science and Engineering und vom Agricultural and Food Research Council in the United Kingdom gefördert. Wir danken dem Leverhulme Trust für ein Forschungsstipendium für J. F. S.
Abstract
Einen ternären Komplex – in Lösung und im Kristall – mit π-π-Charge-Transfer-Wechselwirkungen bilden das Dikation Paraquat (Me\documentclass{article}\pagestyle{empty}\begin{document}$ \mathop {\rm N}\limits^ \oplus $\end{document}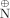 Ň5H4C5H4\documentclass{article}\pagestyle{empty}\begin{document}$ \mathop {\rm N}\limits^ \oplus $\end{document}
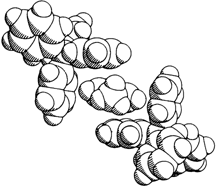
Ň5H4C5H4\documentclass{article}\pagestyle{empty}\begin{document}$ \mathop {\rm N}\limits^ \oplus $\end{document}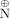 NMe) und zwei Tetraphenylborat-Anionen. Dabei treten Fläche-auf-Fläche- und Fläche-auf-Kante-Wechselwirkungen zwischen Pyridinium- und Phenylringen auf. Vom langgestreckten Paraquat ist im Bild rechts kaum mehr als eine Methylgruppe zu erkennen.
NMe) und zwei Tetraphenylborat-Anionen. Dabei treten Fläche-auf-Fläche- und Fläche-auf-Kante-Wechselwirkungen zwischen Pyridinium- und Phenylringen auf. Vom langgestreckten Paraquat ist im Bild rechts kaum mehr als eine Methylgruppe zu erkennen.
References
- 1 H. M. Colquhoun, E. P. Goodings, J. M. Maud, J. F. Stoddart, D. J. Williams, J. B. Wolstenholme, J. Chem. Soc. Perkin Trans. 2 1985, 607.
- 2 Dies gilt für CH2Cl2-Lösungen [1]. Mischt man äquimolare Mengen von [PQT·2PF6] und DB30C10 in Aceton, wird eine schwache Oangefärbung beobachtet, die eine schwache Charge-Transfer-Wechselwirkung anzeigt.
- 3 G. J. Moody, R. K. Owusu, J. D. R. Thomas, Analyst (London) 112 (1987) 121.
- 4 B. L. Allwood, N. Spencer, H. Shahriari-Zavareh, J. F. Stoddart, D. J. Williams, J. Chem. Soc. Chem. Commun. 1987, 1064.
- 5 Die UV-Spektren von 1 ([DQT·2BPh4]) und 2 ([PQT·2BPh4]) in Aceton enthalten sehr breite Banden, die bis über λ = 500 nm hinausreichen. Für 1 sind zwei Schultern bei λ = 380 und 480 nm zu identifizieren; 2 zeigt nur eine Schulter bei λ = 360 nm. Da weder [DQT·2PF6] oder [PQT·2PF6] noch nBu4NBF4 im sichtbaren Bereich absorbieren, können diese Absorptionen Charge-Transfer-Wechselwirkungen zugeschrieben werden (R. Foster: Organic Charge-Transfer Complexes, Academic Press, London 1969).
- 6 C. J. Bender, Chem. Soc. Rev. 15 (1986) 475.
- 7 Eine Ionenpaar-Komplexierung mit Charge-Transfer-Wechselwirkungen zwischen PQT2⊖ und anorganischen Anionen ist bekannt (L. A. Summers: The Bipyridinium Herbicides, Academic Press, New York 1980, S. 116). Eine Ionenpaar-Komplexierung zwischen großen metallorganischen Kationen und großen organischen Anionen ist ebenfalls bekannt (neues Beispiel: S. Tachiyashiki, H. Yamatera, Inorg. Chem. 25 (1986) 3209).
- 8 R. S. Mulliken, J. Am. Chem. Soc. 74 (1952) 811; M. Meot-Ner (Mautner), Acc. Chem. Res. 17 (1984) 186.
- 9 2: monoklin, a = 9.925(2), b = 14.734(3), c = 17.487(5) Å, β = 93.85(2)°, V = 2549 Å3, P21/c, Z = 2. Der Komplex hat ein Symmetriezentrum. ρber. = 1.10 g cm−1 Nicolet-R3m-Diffraktometer, ω-Scan, Graphit-Monochromator, CuKα-Strahlung. Die Struktur wurde mit direkten Methoden gelöst und anisotrop verfeinert; R = 0.085, Rw = 0.095 für 1859 unabhängige Reflexe [|F0|> 3σ(|F0|), ≥50°]. Der hohe R-Faktor resultiert aus einer leichten Fehlordnung der Phenylgruppen im Anion und aus der Anwesenheit fehlgeordneter Solvensmoleküle. Einzelheiten zur Kristallstrukturuntersuchung können vom Direktor des Cambridge Crystallographic Data Centre, University Chemical Laboratory, Lensfield Road, Cambridge CB2 1EW (England), unter Angabe der Autoren und des Zeitschriftenzitats angefordert werden.
- 10 Arbeitsvorschrift für 2 ([PQT·2 BPh4]): 10 mg (0.018 mmol) nBu4NBPh4 werden in 0.7 mL [D6]Aceton gelöst; diese Lösung wird zu 4.25 mg (0.009 mmol) [PQT·2 PF6] gegeben. Die Lösung färbt sich augenblicklich dunkelgelb, und anschließend fallen geringe Mengen eines Niederschlags aus. Nach Filtration bilden sich innerhalb von 24 h rote, für eine Röntgenstrukturanalyse geeignete Einkristalle; Fp = 215–220°C (Zers.).
- 11 R. O. Gould, A. M. Gray, P. Taylor, M. D. Walkinshaw, J. Am. Chem. Soc. 707 (1985) 5921.
- 12 S. K. Burley, G. A. Petsko, Science (Washington, DC) 229 (1985) 23; J. Am. Chem. Soc. 108 (1986) 7995.
- 13 Ein Rezeptor aus zwei 1,1,1-Triphenylethan-Einheiten, die über drei OCH2C°C–CČH2O-Brücken verknüpft sind, schließt in benzolischer Lösung ein Benzolmolekül ein. Im resultierenden Käfig ist das Benzolmolekül von zwei Phenylringen umgeben, die mit ihren Kanten auf die gegenüberliegenden Flächen zeigen (E. O'Krongley, S. R. Denmeade, M. Y. Chiang, R. Breslow, J. Am. Chem. Soc. 107 (1985) 5544).
- 14 Kürzlich haben wir mehrfach T-Stapelung von aromatischen Ringen gefunden: 1) im Makrocyclus BPP25C7, einem kleineren Analogon von BPP34C10 (A. M. Z. Slawin, N. Spencer, J. F. Stoddart, D. J. Williams, J. Chem. Soc. Chem. Commun. 1987, 1070), und 2) in einem 1:2-Addukt zwischen [Pt(NH3)4]2⊕ und zwei bicyclischen Polyether-Liganden mit jeweils zwei 2,6-Bis(hydroxymethyl)phenol-Resten (D. R. Alston, A. M. Z. Slawin, J. F. Stoddart, D. J. Williams, R. Zarzycki, Angew. Chem. 99 (1987) 697, 698; Angew. Chem. Int. Ed. Engl. 26 (1987) 692, 693). Während die anziehenden T-Wechselwirkungen im ersten Beispiel intramolekularer Natur waren, handelt es sich im zweiten Beispiel - ähnlich wie in [PQT-2BPh4] 2 (Abb. 1–3) - um intermnolekulare, Wechselwirkungen.
- 15 Ähnlich deutliche Änderungen der chemischen Verschiebung von spezifischen Substrat- und Rezeptor-Protonen in Aceton haben wir bei der Bildung von 1 : 1-Einschlußkomplexen von DQT2⊕ und PQT2⊕ mit DB30C10 bzw. BPP34C10 beobachtet [1, 4]. Starke Effekte findet man auch bei der Bildung von 1 : 1-Einschlußkomplexen von zahlreichen wasserlöslichen makrocyclischen Rezeptoren des Cyclophan-Typs, die (substituierte) Diphenylmethan-Reste enthalten, mit aromatischen Substraten, z. B. 2,7-Dihydroxynaphthalin und Pyren (K. Odashima, A. Itai, Y. Iitaka, Y. Arata, K. Koga, Tetrahedron Lett. 21 (1980) 4347; J. Winkler, E. Coutouli-Argyropoulou, R. Leppkes, R. Breslow, J. Am. Chem. Soc. 105 (1983) 7198; F. Diederich, K. Dick, Angew. Chem. 95 (1983) 730; Angew. Chem. Int. Ed. Engl. 22 (1983) 715; Angew. Chem. Suppl. 1983, 957; F. Diederich, D. Griebel, J. Am. Chem. Soc. 105 (1984) 8037).
- 16 Daß [PQT·2BPh4] 2 in Acetonlousung als hochstrukturierter ternärer Komplex vorliegt, wird durch die Kristallisationsneigung nahegelegt. Für [DQT·2BPh4] 1 ergab sich bei der 1H-NMR-spektroskopischen Verfolgung der Titration von [DQT·2PF6] mit nBu4NBPh4 ein „Knie”︁ beim Molverhältnis DQT2⊕ :BPh4⊕ = 1:2.
- 17 Der Abstand von 6.9 Å zwischen C14 und C24′ (und C14′ und C24) in 2 (Abb. 1) könnte beispielsweise von einer OCH2CH2OCH2CH2O- oder einer OCH2C°C–CČH2O-Einheit überbrückt werden. Derartige Verbindungen hätten eine gewisse Ähnlichkeit mit einigen in [13] und [14] erwähnten Makrocyclen.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.