Bis(phosphoryl)-verbrückte Biphenyle durch radikalische Phosphanylierung: Synthese, photophysikalische und elektrochemische Eigenschaften†
Achim Bruch
Organisch-Chemisches Institut, Westfälische Wilhelms-Universität, Corrensstraße 40, 48149 Münster (Deutschland)
Search for more papers by this authorProf. Dr. Aiko Fukazawa
Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Search for more papers by this authorEriko Yamaguchi
Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Search for more papers by this authorCorresponding Author
Prof. Dr. Shigehiro Yamaguchi
Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Shigehiro Yamaguchi, Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Armido Studer, Organisch-Chemisches Institut, Westfälische Wilhelms-Universität, Corrensstraße 40, 48149 Münster (Deutschland)
Search for more papers by this authorCorresponding Author
Prof. Dr. Armido Studer
Organisch-Chemisches Institut, Westfälische Wilhelms-Universität, Corrensstraße 40, 48149 Münster (Deutschland)
Shigehiro Yamaguchi, Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Armido Studer, Organisch-Chemisches Institut, Westfälische Wilhelms-Universität, Corrensstraße 40, 48149 Münster (Deutschland)
Search for more papers by this authorAchim Bruch
Organisch-Chemisches Institut, Westfälische Wilhelms-Universität, Corrensstraße 40, 48149 Münster (Deutschland)
Search for more papers by this authorProf. Dr. Aiko Fukazawa
Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Search for more papers by this authorEriko Yamaguchi
Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Search for more papers by this authorCorresponding Author
Prof. Dr. Shigehiro Yamaguchi
Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Shigehiro Yamaguchi, Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Armido Studer, Organisch-Chemisches Institut, Westfälische Wilhelms-Universität, Corrensstraße 40, 48149 Münster (Deutschland)
Search for more papers by this authorCorresponding Author
Prof. Dr. Armido Studer
Organisch-Chemisches Institut, Westfälische Wilhelms-Universität, Corrensstraße 40, 48149 Münster (Deutschland)
Shigehiro Yamaguchi, Department of Chemistry, Graduate School of Science, Nagoya University and JST-CREST, Furo, Chikusa, Nagoya 464-8602 (Japan)
Armido Studer, Organisch-Chemisches Institut, Westfälische Wilhelms-Universität, Corrensstraße 40, 48149 Münster (Deutschland)
Search for more papers by this authorA.S. und A.B. danken der Deutschen Forschungsgemeinschaft für finanzielle Unterstützung.
Graphical Abstract
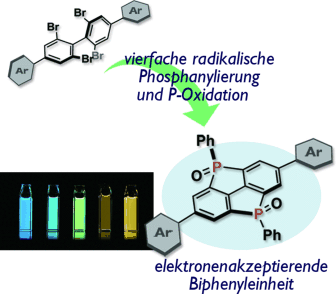
Die effiziente vierfache radikalische Phosphanylierung von 2,2,2′,2′-Tetrabrombiphenyl mit einem Bis(stannyl)phosphan, gefolgt von P-Oxidation, führt zu gespannten Biphenylen mit zwei Phosphorylbrücken (siehe Bild). Verlängerte π-konjugierte Verbindungen mit diesem Biphenylkern können auch durch die mehrfache radikalische Phosphanylierung synthetisiert werden. Die zwei Phosphorylbrücken machen das Biphenyl zu einem einzigartigen elektronenziehenden Gerüst.
Supporting Information
Detailed facts of importance to specialist readers are published as ”Supporting Information”. Such documents are peer-reviewed, but not copy-edited or typeset. They are made available as submitted by the authors.
| Filename | Description |
|---|---|
| ange_201104114_sm_miscellaneous_information.pdf4.6 MB | miscellaneous_information |
Please note: The publisher is not responsible for the content or functionality of any supporting information supplied by the authors. Any queries (other than missing content) should be directed to the corresponding author for the article.
References
- 1J. E. Anthony, A. Facchetti, M. Heeney, S. R. Marder, X. Zhan, Adv. Mater. 2010, 22, 3876–3892, zit. Lit.
- 2A. Ajayaghosh, Chem. Soc. Rev. 2003, 32, 181–191, zit. Lit.
- 3A. Fukazawa, S. Yamaguchi, Chem. Asian J. 2009, 4, 1386–1400.
- 4K. L. Chan, M. J. McKiernan, C. R. Towns, A. B. Holmes, J. Am. Chem. Soc. 2005, 127, 7662–7663.
- 5Aktuelle Beispiele:
- 5aS. Zhang, R. Chen, J. Yin, F. Liu, H. Jiang, N. Shi, Z. An, C. Ma, B. Liu, W. Huang, Org. Lett. 2010, 12, 3438–3441;
- 5bN. Fukawa, T. Osaka, K. Noguchi, K. Tanaka, Org. Lett. 2010, 12, 1324–1327;
- 5cJ. Yin, S.-L. Zhang, R.-F. Chen, Q.-D. Ling, W. Huang, Phys. Chem. Chem. Phys. 2010, 12, 15448–15458;
- 5dK. Geramita, J. McBee, T. D. Tilley, J. Org. Chem. 2009, 74, 820–829;
- 5eH.-C. Su, O. Fadhel, C.-J. Yang, T.-Y. Cho, C. Fave, M. Hissler, C.-C. Wu, R. Réau, J. Am. Chem. Soc. 2006, 128, 983–995.
- 6Aktuelle Beispiele:
- 6aI. I. Perepichka, I. F. Perepichika, M. R. Bryce, L.-O. Pålsson, Chem. Commun. 2005, 3397–3399;
- 6bC. Wang, H. Dong, H. Li, H. Zhao, Q. Meng, W. Hu, Cryst. Growth Des. 2010, 10, 4155–4160.
- 7Übersichtsartikel über P-haltige π-konjugierte Materialien:
- 7aT. Baumgartner, R. Réau, Chem. Rev. 2006, 106, 4681–4727; Korrektur: T. Baumgartner, R. Réau, Chem. Rev. 2007, 107, 303;
- 7bF. Mathey, Angew. Chem. 2003, 115, 1616–1643;
10.1002/ange.200200557 Google ScholarAngew. Chem. Int. Ed. 2003, 42, 1578–1604.
- 8Aktuelle Beispiele:
- 8aY. Ren, T. Baumgartner, J. Am. Chem. Soc. 2011, 133, 1328–1340;
- 8bY. Liu, J. Feng, A. Ren, J. Comput. Chem. 2007, 28, 2500–2509;
- 8cT. Baumgartner, T. Neumann, B. Wirges, Angew. Chem. 2004, 116, 6323–6328;
10.1002/ange.200461301 Google ScholarAngew. Chem. Int. Ed. 2004, 43, 6197–6201.
- 9
- 9aA. Fukazawa, T.-a. Murai, L. Li, Y. Chen, S. Yamaguchi, C. R. Chim. 2010, 13, 1082–1090;
- 9bA. Fukazawa, Y. Ichihashi, Y. Kosaka, S. Yamaguchi, Chem. Asian J. 2009, 4, 1729–1740;
- 9cA. Fukazawa, M. Hara, T. Okamoto, E.-C. Son, C. Xu, K. Tamao, S. Yamaguchi, Org. Lett. 2008, 10, 913–916.
- 10M. Shimizu, H. Tatsumi, K. Mochida, K. Oda, T. Hiyama, Chem. Asian J. 2008, 3, 1238–1247.
- 11T. Kimura, Y. Izumi, N. Furukawa, Y. Minoshima, Heteroat. Chem. 1996, 7, 143–147.
- 12T. Kimura, Y. Ishikawa, N. Furukawa, Chem. Lett. 1993, 635–636.
- 13T. Kimura, Y. Ishikawa, S. Ogawa, T. Nishio, I. Iida, N. Furukawa, Tetrahedron Lett. 1992, 33, 6355–6358.
- 14B. M. Trost, P. L. Kinson, J. Am. Chem. Soc. 1970, 92, 2591–2593.
- 15In der Tat wurde nur die Dilithiierung von 4 mit einem Überschuss an Butyllithium beschrieben: Q. Perron, J. Praz, A. Alexakis, Tetrahedron: Asymmetry 2009, 20, 1004–1007.
- 16
- 16aS. Vaillard, C. Mück-Lichtenfeld, S. Grimme, A. Studer, Angew. Chem. 2007, 119, 6653–6656;
10.1002/ange.200701650 Google ScholarAngew. Chem. Int. Ed. 2007, 46, 6533–6536;
- 16bA. Bruch, A. Ambrosius, R. Frohlich, A. Studer, D. B. Guthrie, H. Zhang, D. P. Curran, J. Am. Chem. Soc. 2010, 132, 11452–11454;
- 16cM.-C. Lamas, A. Studer, Org. Lett. 2011, 13, 2236–2239.
- 17Kristallographische Daten für trans-2 und cis-2: siehe Hintergrundinformationen. CCDC 829426 (trans-2) und 829425 (cis-2) enthalten die ausführlichen kristallographischen Daten zu dieser Veröffentlichung. Die Daten sind kostenlos beim Cambridge Crystallographic Data Centre über www.ccdc.cam.ac.uk/data_request/cif erhältlich.
- 18G. B. Robertson, Nature 1961, 191, 593–594.
- 19A. Decken, CCDC 254271 enthält die ausführlichen kristallographischen Daten zu dieser Veröffentlichung. Die Daten sind kostenlos beim Cambridge Crystallographic Data Centre über www.ccdc.cam.ac.uk/data_request/cif erhältlich.
- 20
- 20aW. Egan, R. Tang, G. Zon, K. Mislow, J. Am. Chem. Soc. 1971, 93, 6205–6216;
- 20bM. Widhalm, L. Brecker, K. Mereiter, Tetrahedron: Asymmetry 2006, 17, 1355–1369.
- 21
- 21aT. Ishiyama, J. Takagi, K. Ishida, N. Miyaura, N. R. Anastasi, J. F. Hartwig, J. Am. Chem. Soc. 2002, 124, 390–391;
- 21bT. Ishiyama, J. Takagi, J. F. Hartwig, N. Miyaura, Angew. Chem. 2002, 114, 3182;
10.1002/1521-3757(20020816)114:16<3182::AID-ANGE3182>3.0.CO;2-9 Google ScholarAngew. Chem. Int. Ed. 2002, 41, 3056.10.1002/1521-3773(20020816)41:16<3056::AID-ANIE3056>3.0.CO;2-# CAS PubMed Web of Science® Google Scholar
- 22Z. H. Li, M. S. Wong, Y. Tao, M. D’Iorio, J. Org. Chem. 2004, 69, 921–927.
- 23J. R. Lakowicz, Principles of Fluorescence Spectroscopy, 3. Aufl., Springer, Berlin, 2006, S. 205–213.
10.1007/978-0-387-46312-4_6 Google Scholar
- 24Obwohl die Lippert-Mataga-Gleichung ursprünglich das Vorhandensein eines molekularen Dipols annimmt, wurde gezeigt, dass sie auf mehrere quadrupolare π-konjugierte Verbindungen anwendbar ist;
- 24aB. Strehmel, A. M. Sarker, J. H. Malpert, V. Strehmel, H. Seifert, D. C. Neckers, J. Am. Chem. Soc. 1999, 121, 1226–1236;
- 24bF. C. Krebs, H. Spanggaared, J. Org. Chem. 2002, 67, 7185–7192;
- 24cC.-H. Zhao, E. Sakuda, A. Wakamiya, S. Yamaguchi, Chem. Eur. J. 2009, 15, 10603–10612.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.