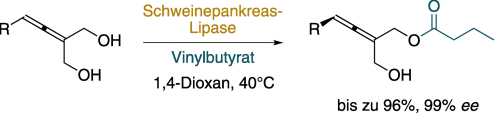
Enantioselektive enzymatische Desymmetrisierung prochiraler Allendiole†
Dipl.-Chem. Chicco Manzuna Sapu
Department Chemie, Universität zu Köln, Greinstraße 4, 50939 Köln (Deutschland) http://www.oc.uni-koeln.de/deska
Search for more papers by this authorProf. Jan-E. Bäckvall
Department of Organic Chemistry, Arrheniuslaboratoriet, Stockholm University (Schweden)
Search for more papers by this authorCorresponding Author
Dr. Jan Deska
Department Chemie, Universität zu Köln, Greinstraße 4, 50939 Köln (Deutschland) http://www.oc.uni-koeln.de/deska
Department Chemie, Universität zu Köln, Greinstraße 4, 50939 Köln (Deutschland) http://www.oc.uni-koeln.de/deskaSearch for more papers by this authorDipl.-Chem. Chicco Manzuna Sapu
Department Chemie, Universität zu Köln, Greinstraße 4, 50939 Köln (Deutschland) http://www.oc.uni-koeln.de/deska
Search for more papers by this authorProf. Jan-E. Bäckvall
Department of Organic Chemistry, Arrheniuslaboratoriet, Stockholm University (Schweden)
Search for more papers by this authorCorresponding Author
Dr. Jan Deska
Department Chemie, Universität zu Köln, Greinstraße 4, 50939 Köln (Deutschland) http://www.oc.uni-koeln.de/deska
Department Chemie, Universität zu Köln, Greinstraße 4, 50939 Köln (Deutschland) http://www.oc.uni-koeln.de/deskaSearch for more papers by this authorDiese Arbeit wurde vom Fonds der Chemischen Industrie (Liebig-Stipendium), dem Deutschen Akademischen Austauschdienst, dem Vetenskapsrådet und der K&W Wallenberg Stiftelse sowie Carbolution Chemicals unterstützt.
Graphical Abstract
Supporting Information
Detailed facts of importance to specialist readers are published as ”Supporting Information”. Such documents are peer-reviewed, but not copy-edited or typeset. They are made available as submitted by the authors.
| Filename | Description |
|---|---|
| ange_201103227_sm_miscellaneous_information.pdf3.3 MB | miscellaneous_information |
Please note: The publisher is not responsible for the content or functionality of any supporting information supplied by the authors. Any queries (other than missing content) should be directed to the corresponding author for the article.
References
- 1
- 1aN. Krause, A. S. K. Hashmi, Modern Allene Chemistry, 1. Aufl., Wiley-VCH, Weinheim, 2004;
- 1bA. S. K. Hashmi in Organic Synthesis Highlights V, 1. Aufl. (Hrsg.: H.-G. Schmalz, T. Wirth), Wiley-VCH, Weinheim, 2003, S. 56–67.
- 2Ausgewählte aktuelle Bespiele: Pd-Katalyse:
- 2aR. Zimmer, C. U. Dinesh, E. Nandanan, F. A. Khan, Chem. Rev. 2000, 100, 3067;
- 2bS. Ma, Z. Yu, Angew. Chem. 2002, 114, 1853; Angew. Chem. Int. Ed. 2002, 41, 1775;
- 2cJ. Franzén, J.-E. Bäckvall, J. Am. Chem. Soc. 2003, 125, 6056;
- 2dA. K. Å. Persson, J.-E. Bäckvall, Angew. Chem. 2010, 122, 4728; Angew. Chem. Int. Ed. 2010, 49, 4624; Ru-Katalyse:
- 2eB. M. Trost, A. B. Pinkerton, J. Am. Chem. Soc. 1999, 121, 10 842;
- 2fB. M. Trost, D. R. Fandrick, D. C. Dinh, J. Am. Chem. Soc. 2005, 127, 14 186; Rh-Katalyse:
- 2gK. M. Brummond, H. Chen, B. Mitasev, A. D. Casarez, Org. Lett. 2004, 6, 2161;
- 2hT. Nishimura, S. Hirabayashi, Y. Yasuhara, T. Hayashi, J. Am. Chem. Soc. 2006, 128, 2556;
- 2iT. Seiser, N. Cramer, Angew. Chem. 2008, 120, 9435; Angew. Chem. Int. Ed. 2008, 47, 9294;
- 2jA. H. Stoll, S. B. Blakey, J. Am. Chem. Soc. 2010, 132, 2108; Ag-Katalyse:
- 2kJ. A. Marshall, M. A. Wolf, E. M. Wallace, J. Org. Chem. 1997, 62, 367;
- 2lM. P. VanBrunt, R. F. Standaert, Org. Lett. 2000, 2, 705; Au-Katalyse:
- 2mN. Nishina, Y. Yamamoto, Angew. Chem. 2006, 118, 3392; Angew. Chem. Int. Ed. 2006, 45, 3314;
- 2nN. Bongers, N. Krause, Angew. Chem. 2008, 120, 2208; Angew. Chem. Int. Ed. 2008, 47, 2178;
- 2oC. Winter, N. Krause, Angew. Chem. 2009, 121, 6457; Angew. Chem. Int. Ed. 2009, 48, 6339.
- 3A. Hoffmann-Röder, N. Krause, Angew. Chem. 2004, 116, 1216; Angew. Chem. Int. Ed. 2004, 43, 1196.
- 4Ausgewählte Beispiele:
- 4aN. Krause, A. Hoffmann-Röder, Tetrahedron 2004, 60, 11 671;
- 4bB. D. Sherry, F. D. Toste, J. Am. Chem. Soc. 2004, 126, 15 978;
- 4cC. Deutsch, B. H. Lipshutz, N. Krause, Org. Lett. 2009, 11, 5010.
- 5Übersichtsartikel zur chemischen wie enzymatischen Racematspaltung von Allenen:
- 5aM. Ogasawara, Tetrahedron: Asymmetry 2009, 20, 259; siehe außerdem:
- 5bG. Kresze, W. Runge, E. Ruch, Liebigs Ann. Chem. 1972, 756, 112;
- 5cJ. Nyhlén, L. Eriksson, J.-E. Bäckvall, Chirality 2007, 20, 47.
- 6J. Deska, J.-E. Bäckvall, Org. Biomol. Chem. 2009, 7, 3379.
- 7
- 7aU. T. Bornscheuer, R. J. Kazlauskas, Hydrolases in Organic Synthesis: Regio- and Stereoselective Biotransformations, 2. Aufl., Wiley-VCH, Weinheim, 2005;
- 7bK. Faber, Biotransformations in Organic Chemistry, 5. Aufl., Springer, Berlin, 2008;
- 7cV. Gotor, I. Alfonso, E. García-Urdiales, Asymmetric Organic Synthesis with Enzymes, 1. Aufl., Wiley-VCH, Weinheim, 2008.
- 8Übersichtsartikel:
- 8aA. Stecher, K. Faber, Synthesis 1997, 1;
- 8bO. Pàmies, J.-E. Bäckvall, Chem. Rev. 2003, 103, 3247;
- 8cN. J. Turner, Curr. Opin. Chem. Biol. 2004, 8, 114;
- 8dB. Martín-Matute, J.-E. Bäckvall, Curr. Opin. Chem. Biol. 2007, 11, 226;
- 8eJ. H. Lee, K. Han, M.-J. Kim, J. Park, Eur. J. Org. Chem. 2010, 999;
- 8fH. Pellissier, Tetrahedron 2011, 67, 3769.
- 9J. Deska, C. del Pozo Ochoa, J.-E. Bäckvall, Chem. Eur. J. 2010, 16, 4447.
- 10Übersichtsartikel:
- 10aE. Schoffers, A. Golebiowski, C. R. Johnson, Tetrahedron 1996, 52, 3769;
- 10bE. García-Urdiales, A. Ignacio, V. Gotor, Chem. Rev. 2005, 105, 313.
- 11Guanti et al. berichteten erstmals von einem Versuch der enzymatischen Allen-Desymmetrisierung, verfolgten diesen Weg jedoch nicht weiter:
- 11aG. Guanti, L. Banfi, E. Narisano, J. Org. Chem. 1992, 57, 1540; weitere Beispiele zur enzymatischen Desymmetrisierung axial-chiraler Verbindungen (Biaryle und Spiro[3.3]heptane):
- 11bK. Naemura, A. Furutani, J. Chem. Soc. Perkin Trans. 1 1990, 3215;
- 11cT. Matsumoto, T. Konegawa, T. Nakamura, K. Suzuki, Synlett 2002, 122;
- 11dK. Okuyama, K. Shingubara, S.-I. Tsujiyama, K. Suzuki, T. Matsumoto, Synlett 2009, 941;
- 11eB. Yuan, A. Page, C. P. Worrall, F. Escalettes, S. C. Willies, J. J. W. McDouall, N. J. Turner, J. Clayden, Angew. Chem. 2010, 122, 7164; Angew. Chem. Int. Ed. 2010, 49, 7010.
- 12R. Birner-Grünberger, H. Scholze, K. Faber, A. Hermetter, Biotechnol. Bioeng. 2004, 85, 147.
- 13“Lipase from porcine pancreas” der Firma MP Biomedicals wurde in unseren Untersuchungen verwendet, und die erzielten Ergebnisse gaben keine Hinweise auf einen solchen Effekt. Jedoch zeigten Umsetzungen mit “PPL type II” von Sigma, die bekanntermaßen Verunreinigungen enthalten kann,[12] deutlich verringerte Enantioselektivitäten.
- 14Die absolute Konfiguration der erhaltenen Monoester wurde durch Abbau zu 4-Methyl-2-phenyl-2,5-dihydrofuran und den Vergleich der Drehwerte mit Literaturdaten bestimmt (siehe Hintergrundinformationen). Die Monoester zeigten keine Tendenz zu racemisieren, und selbst nach Aufbewahrung über drei Monate bei 4 °C konnte nur ein marginaler Verlust an optischer Aktivität beobachtet werden.
- 15Während Diester 3 a auch in der Umesterung mit Butanol noch eine akzeptable Umsatzgeschwindigkeit zeigte, konnte bei anderen Allenyldiestern teilweise eine deutlich verlängerte Reaktionsdauer beobachtet werden. Wegen der Reversibilität der Umesterung ist hier kein vollständiger Umsatz zu erreichen, sodass weitere Untersuchungen, insbesondere zur Verwendung anderer Nucleophile, vonnöten sein werden. Die ausgezeichnete Enantioselektivität hingegen wurde auch in sämtlichen solvolytischen Desymmetrisierungen bestätigt.
- 16Ausgewählte aktuelle Beispiele:
- 16aM. K. Gurjar, S. Nayak, C. V. Ramana, Tetrahedron Lett. 2005, 46, 1881;
- 16bS. Inuki, S. Oishi, N. Fujii, H. Ohno, Org. Lett. 2008, 10, 5239;
- 16cY. Sawama, Y. Sawama, N. Krause, Org. Biomol. Chem. 2008, 6, 3573;
- 16dZ. Gao, Y. Li, J. P. Cooksey, T. N. Snaddon, S. Schunk, E. M. E. Viseux, S. M. McAteer, P. J. Kocienski, Angew. Chem. 2009, 121, 5122; Angew. Chem. Int. Ed. 2009, 48, 5022;
- 16eF. Volz, S. H. Wadman, A. Hoffmann-Röder, N. Krause, Tetrahedron 2009, 65, 1902.
- 17W. Wang, Y. H. Zeng, K. Osman, K. Shinde, M. Rahman, S. Gibbons, Q. Mu, J. Nat. Prod. 2010, 73, 1815.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.