Der asymmetrische konjugierte Silyltransfer in iterativen katalytischen Sequenzen: Synthese des C7–C16-Fragments von (+)-Neopeltolid†
Eduard Hartmann
Organisch-Chemisches Institut, Westfälische Wilhelms-Universität Münster, Corrensstraße 40, 48149 Münster (Deutschland), Fax: (+49)251-83-36501 http://www.uni-muenster.de/Chemie.oc/oestreich
Search for more papers by this authorMartin Oestreich Prof. Dr.
Organisch-Chemisches Institut, Westfälische Wilhelms-Universität Münster, Corrensstraße 40, 48149 Münster (Deutschland), Fax: (+49)251-83-36501 http://www.uni-muenster.de/Chemie.oc/oestreich
Search for more papers by this authorEduard Hartmann
Organisch-Chemisches Institut, Westfälische Wilhelms-Universität Münster, Corrensstraße 40, 48149 Münster (Deutschland), Fax: (+49)251-83-36501 http://www.uni-muenster.de/Chemie.oc/oestreich
Search for more papers by this authorMartin Oestreich Prof. Dr.
Organisch-Chemisches Institut, Westfälische Wilhelms-Universität Münster, Corrensstraße 40, 48149 Münster (Deutschland), Fax: (+49)251-83-36501 http://www.uni-muenster.de/Chemie.oc/oestreich
Search for more papers by this authorDiese Arbeit wurde von der Deutschen Forschungsgemeinschaft (Oe 249/3-2) und dem Fonds der Chemischen Industrie (Chemiefonds-Stipendium für E.H., 2009–2011) gefördert. Wir danken der Solvias AG (Basel) für die Überlassung zahlreicher Liganden.
Graphical Abstract
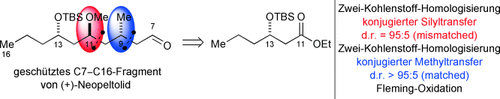
Was nicht passt, wird passend gemacht! Die anti,anti-Konfiguration des C7–C16-Fragments von (+)-Neopeltolid wird in einer iterativen Sequenz katalysatorkontrollierter Si- und Me-Gruppentransfers stereoselektiv aufgebaut, und das unbeeinträchtigt von der Mismatched-Selektivität in der ersten Iteration (Si=Me2PhSi, siehe Schema; TBS=tert-Butyldimethylsilyl).
Supporting Information
Detailed facts of importance to specialist readers are published as ”Supporting Information”. Such documents are peer-reviewed, but not copy-edited or typeset. They are made available as submitted by the authors.
| Filename | Description |
|---|---|
| ange_201002916_sm_miscellaneous_information.pdf1.5 MB | miscellaneous_information |
Please note: The publisher is not responsible for the content or functionality of any supporting information supplied by the authors. Any queries (other than missing content) should be directed to the corresponding author for the article.
References
- 1Zusammenfassungen:
- 1aB. ter Horst, B. L. Feringa, A. J. Minnaard, Chem. Commun. 2010, 46, 2535–2547;
- 1bS. Hanessian, S. Giroux, V. Mascitti, Synthesis 2006, 1057–1076.
- 2Katalysatorkontrollierte Carboaluminierung:
- 2aM. Magnin-Lachaux, Z. Tan, B. Liang, E.-i. Negishi, Org. Lett. 2004, 6, 1425–1427;
- 2bG. Zhu, E.-i. Negishi, Org. Lett. 2007, 9, 2771–2774.
- 3Katalysatorkontrollierte 1,4-Addition:
- 3aB. ter Horst, B. L. Feringa, A. J. Minnaard, Chem. Commun. 2007, 489–491;
- 3bB. ter Horst, B. L. Feringa, A. J. Minnaard, Org. Lett. 2007, 9, 3013–3015;
- 3cT.-K. Lum, S.-Y. Wang, T.-P. Loh, Org. Lett. 2008, 10, 761–764.
- 4Konjugierte Addition von RMgBr an E-konfigurierte α,β-ungesättigte Thioester (inklusive iterativer Synthesen):
- 4aR. Des Mazery, M. Pullez, F. López, S. R. Harutyunyan, A. J. Minnaard, B. L. Feringa, J. Am. Chem. Soc. 2005, 127, 9966–9967;
- 4bB. M. Ruiz, K. Geurts, M. Ángeles, M. A. Fernández-Ibáñez, B. ter Horst, A. J. Minnaard, B. L. Feringa, Org. Lett. 2007, 9, 5123–5126.
- 5Reagens- und substratkontrollierte allylische Substitution:
- 5aC. Herber, B. Breit, Angew. Chem. 2005, 117, 5401–5403;
10.1002/ange.200501612 Google ScholarAngew. Chem. Int. Ed. 2005, 44, 5267–5269;
- 5bC. Herber, B. Breit, Chem. Eur. J. 2006, 12, 6684–6691.
- 6Jüngst beschriebene katalysatorkontrollierte Strategien:
- 6aJ. T. Binder, S. F. Kirsch, Chem. Commun. 2007, 4164–4166;
- 6bH. Menz, S. F. Kirsch, Org. Lett. 2009, 11, 5634–5637;
- 6cY. Lu, I. S. Kim, A. Hassan, D. J. Del Valle, M. J. Krische, Angew. Chem. 2009, 121, 5118–5121; Angew. Chem. Int. Ed. 2009, 48, 5018–5021 und darin zitierte Arbeiten zu reagens- und substratkontrollierten iterativen Synthesen.
- 7Enantioselektiver Silyltransfer auf Z-konfigurierte α,β-ungesättigte Oxoester unter Verwendung von Me2PhSi-Bpin:[9]
- 7aC. Walter, G. Auer, M. Oestreich, Angew. Chem. 2006, 118, 5803–5805; Angew. Chem. Int. Ed. 2006, 45, 5675–5677;
- 7bC. Walter, M. Oestreich, Angew. Chem. 2008, 120, 3878–3880; Angew. Chem. Int. Ed. 2008, 47, 3818–3820;
- 7cC. Walter, R. Fröhlich, M. Oestreich, Tetrahedron 2009, 65, 5513–5520.
- 8Allgemeine Reaktionsvorschrift für den enantioselektiven Silyltransfer ebenfalls unter Verwendung von Me2PhSi-Bpin:[9] K.-s. Lee, A. H. Hoveyda, J. Am. Chem. Soc. 2010, 132, 2898–2900.
- 9Herstellung von Me2PhSi-Bpin:
- 9aM. Suginome, T. Matsuda, Y. Ito, Organometallics 2000, 19, 4647–4649; Zusammenfassung der Chemie von Me2PhSi-Bpin:
- 9bT. Ohmura, M. Suginome, Bull. Chem. Soc. Jpn. 2009, 82, 29–49.
- 10
- 10aK. Tamao, T. Kakui, M. Akita, T. Iwahara, R. Kanatani, J. Yoshida, M. Kumada, Tetrahedron 1983, 39, 983–990;
- 10bI. Fleming, R. Henning, H. Plaut, J. Chem. Soc. Chem. Commun. 1984, 29–31;
- 10cI. Fleming, P. E. J. Sanderson, Tetrahedron Lett. 1987, 28, 4229–4232.
- 11A. E. Wright, J. Cook Botelho, E. Guzmán, D. Harmody, P. Linley, P. J. McCarthy, T. P. Pitts, S. A. Pomponi, J. K. Reed, J. Nat. Prod. 2007, 70, 412–416.
- 12(Formale) Totalsynthesen über das C7–C16-Fragment:
- 12aW. Youngsaye, J. T. Lowe, F. Pohlki, P. Ralifo, J. S. Panek, Angew. Chem. 2007, 119, 9371–9374;
10.1002/ange.200704122 Google ScholarAngew. Chem. Int. Ed. 2007, 46, 9211–9214;
- 12bD. W. Custar, T. P. Zabawa, K. A. Scheidt, J. Am. Chem. Soc. 2008, 130, 804–805;
- 12cS. K. Woo, M. S. Kwon, E. Lee, Angew. Chem. 2008, 120, 3286–3288; Angew. Chem. Int. Ed. 2008, 47, 3242–3244;
- 12dX. Guinchard, E. Roulland, Org. Lett. 2009, 11, 4700–4703;
- 12eJ. S. Yadav, G. G. K. S. Narayana Kumar, Tetrahedron 2010, 66, 480–487.
- 13(Formale) Totalsynthesen über das siliciumgeschützte C7–C16-Fragment 2:
- 13aTBS:I. Paterson, N. A. Miller, Chem. Commun. 2008, 4708–4710;
- 13bTBDPS:V. V. Vintonyak, M. E. Maier, Org. Lett. 2008, 10, 1239–1242.
- 14Totalsynthesen basierend auf anderen Bindungsbrüchen:
- 14aH. Fuwa, S. Naito, T. Goto, M. Sasaki, Angew. Chem. 2008, 120, 4815–4817;
10.1002/ange.200801399 Google ScholarAngew. Chem. Int. Ed. 2008, 47, 4737–4739;
- 14bR. Kartika, T. R. Gruffi, R. E. Taylor, Org. Lett. 2008, 10, 5047–5050;
- 14cW. Tu, P. E. Floreancig, Angew. Chem. 2009, 121, 4637–4641; Angew. Chem. Int. Ed. 2009, 48, 4567–4571;
- 14dH. Kim, Y. Park, J. Hong, Angew. Chem. 2009, 121, 7713–7717; Angew. Chem. Int. Ed. 2009, 48, 7577–7581;
- 14eH. Fuwa, A. Saito, M. Sasaki, Angew. Chem. 2010, 122, 3105–3108;
10.1002/ange.201000624 Google ScholarAngew. Chem. Int. Ed. 2010, 49, 3041–3044.
- 15Der Kupfer(I)-katalysierte Methyltransfer erfordert eine E-Konfiguration, der Rhodium(I)-katalysierte Silyltransfer eine Z-Konfiguration.
- 16E-selektive Wittig-Olefinierung:
- 16aG. E. Keck, E. P. Boden, S. A. Mabury, J. Org. Chem. 1985, 50, 709–710; Z-selektive Still-Gennari-Olefinierung:
- 16bW. C. Still, C. Gennari, Tetrahedron Lett. 1983, 24, 4405–4408.
- 17Während in diesem speziellen Fall das E-Alken schneller als das Z-Alken reagiert, kennt man auch Fälle (bei vollständigem Umsatz), bei denen beide Isomere komplett abreagieren oder Z gar zu E isomerisiert. Mechanistische Untersuchung: S. R. Harutyunyan, F. López, W. R. Browne, A. Correa, D. Peña, R. Badorrey, A. Meetsma, A. J. Minnaard, B. L. Feringa, J. Am. Chem. Soc. 2006, 128, 9103–9118.
- 18F. López, S. R. Harutyunyan, A. Meetsma, A. J. Minnaard, B. L. Feringa, Angew. Chem. 2005, 117, 2812–2816; Angew. Chem. Int. Ed. 2005, 44, 2752–2756.
- 19Die chemischen Ausbeuten waren allerdings nur mäßig, und konjugierte Reduktion war eine schwerwiegende Nebenreaktion.[7b]
- 20Lit. [13a] bietet keine experimentellen Details zur Herstellung von 19. Enantioselektive Synthese seines Enantiomers: L.-S. Deng, X.-P. Huang, G. Zhao, J. Org. Chem. 2006, 71, 4625–4635.
- 21Die Tamao-Fleming-Oxidation des 1-OSiR3-3-Si-Motivs ist selten und nur für cyclische Substrate beschrieben: SiR3=TES:
- 21aS. Wendeborn, G. Binot, M. Nina, T. Winkler, Synlett 2002, 1683–1687; SiR3=TBS:
- 21bC. Boglio, S. Stahlke, S. Thorimbert, M. Malacria, Org. Lett. 2005, 7, 4851–4854.
- 22Nach Einreichen dieser Zuschrift stellten wir fest, dass Martinez-Solorio und Jennings die identische Sequenz unabhängig von uns ausgearbeitet hatten: D. Martinez-Solorio, M. P. Jennings, J. Org. Chem. 2010, 75, 4095–4104.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.