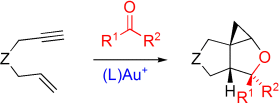
Gold-katalysierte intermolekulare Addition von Carbonylverbindungen an 1,6-Enine†
Mathias Schelwies
Organisch-Chemisches Institut, Universität Heidelberg, Im Neuenheimer Feld 270, 69120 Heidelberg, Deutschland, Fax: (+49) 6221-544-205
Search for more papers by this authorAdrian L. Dempwolff
Organisch-Chemisches Institut, Universität Heidelberg, Im Neuenheimer Feld 270, 69120 Heidelberg, Deutschland, Fax: (+49) 6221-544-205
Search for more papers by this authorFrank Rominger Dr.
Organisch-Chemisches Institut, Universität Heidelberg, Im Neuenheimer Feld 270, 69120 Heidelberg, Deutschland, Fax: (+49) 6221-544-205
Search for more papers by this authorGünter Helmchen Prof. Dr.
Organisch-Chemisches Institut, Universität Heidelberg, Im Neuenheimer Feld 270, 69120 Heidelberg, Deutschland, Fax: (+49) 6221-544-205
Search for more papers by this authorMathias Schelwies
Organisch-Chemisches Institut, Universität Heidelberg, Im Neuenheimer Feld 270, 69120 Heidelberg, Deutschland, Fax: (+49) 6221-544-205
Search for more papers by this authorAdrian L. Dempwolff
Organisch-Chemisches Institut, Universität Heidelberg, Im Neuenheimer Feld 270, 69120 Heidelberg, Deutschland, Fax: (+49) 6221-544-205
Search for more papers by this authorFrank Rominger Dr.
Organisch-Chemisches Institut, Universität Heidelberg, Im Neuenheimer Feld 270, 69120 Heidelberg, Deutschland, Fax: (+49) 6221-544-205
Search for more papers by this authorGünter Helmchen Prof. Dr.
Organisch-Chemisches Institut, Universität Heidelberg, Im Neuenheimer Feld 270, 69120 Heidelberg, Deutschland, Fax: (+49) 6221-544-205
Search for more papers by this authorDiese Arbeit wurde von der Deutschen Forschungsgemeinschaft (SFB 623), der Studienstiftung des deutschen Volkes (Stipendium für M.S.) und dem Fonds der Chemischen Industrie gefördert.
Graphical Abstract
References
- 1Übersichten:
- 1aC. Bruneau, Angew. Chem. 2005, 117, 2380–2386;
10.1002/ange.200462568 Google ScholarAngew. Chem. Int. Ed. 2005, 44, 2328–2334;
- 1bG. C. Lloyd-Jones, Org. Biomol. Chem. 2003, 1, 215–236;
- 1cB. M. Trost, M. J. Krische, Synlett 1998, 1–16;
- 1dC. Aubert, O. Buisine, M. Malacria, Chem. Rev. 2002, 102, 813–834;
- 1eM. Mori in Handbook of Metathesis, Vol. 2 (Hrsg.: ), Wiley, New York, 2004, S. 176–204.
- 2E. Jiménez-Núñez, C. K. Claverie, C. Nieto-Oberhuber, A. M. Echavarren, Angew. Chem. 2006, 118, 5578–5581;
10.1002/ange.200601575 Google ScholarAngew. Chem. Int. Ed. 2006, 45, 5452–5455.
- 3Übersichten:
- 3aE. Jiménez-Núñez, A. M. Echavarren, Chem. Commun. 2007, 333–346;
- 3bD. J. Gorin, F. D. Toste, Nature 2007, 446, 395–403;
- 3cA. S. K. Hashmi, G. J. Hutchings, Angew. Chem. 2006, 118, 8064–8105;
10.1002/ange.200602454 Google ScholarAngew. Chem. Int. Ed. 2006, 45, 7896–7936;
- 3dA. S. K. Hashmi, Gold Bull. 2004, 37, 51–65;
- 3eA. Hoffmann-Röder, N. Krause, Org. Biomol. Chem. 2005, 3, 387–391;
- 3fR. A. Widenhoefer, X. Han, Eur. J. Org. Chem. 2006, 4555–4563.
- 4
- 4aJ. H. Teles, S. Brode, M. Chabanas, Angew. Chem. 1998, 110, 1475–1478;
10.1002/(SICI)1521-3757(19980518)110:10<1475::AID-ANGE1475>3.0.CO;2-L Google ScholarAngew. Chem. Int. Ed. 1998, 37, 1415–1418;10.1002/(SICI)1521-3773(19980605)37:10<1415::AID-ANIE1415>3.0.CO;2-N CAS PubMed Web of Science® Google Scholar
- 4bA. S. K. Hashmi, T. M. Frost, J. W. Bats, J. Am. Chem. Soc. 2000, 122, 11553–11554;
- 4cM. T. Reetz, K. Sommer, Eur. J. Org. Chem. 2003, 3485–3496;
- 4dC. Nieto-Oberhuber, M. P. Muñoz, E. Buñuel, C. Nevado, D. J. Cárdenas, A. M. Echavarren, Angew. Chem. 2004, 116, 2456–2460;
10.1002/ange.200353207 Google ScholarAngew. Chem. Int. Ed. 2004, 43, 2402–2406;
- 4eV. Mamane, T. Gress, H. Krause, A. Fürstner, J. Am. Chem. Soc. 2004, 126, 8654–8655;
- 4fJ. J. Kennedy-Smith, S. T. Staben, F. D. Toste, J. Am. Chem. Soc. 2004, 126, 4526–4527;
- 4gR. L. LaLonde, B. D. Sherry, E. J. Kang, F. D. Toste, J. Am. Chem. Soc. 2007, 129, 2452–2453.
- 5C. Nieto-Oberhuber, M. P. Muñoz, S. López, E. Jiménez-Núñez, C. Nevado, E. Herrero-Gómez, M. Raducan, A. M. Echavarren, Chem. Eur. J. 2006, 12, 1677–1693.
- 6
- 6aC. Nieto-Oberhuber, S. López, M. P. Muñoz, E. Jiménez-Núñez, E. Buñuel, D. J. Cárdenas, A. M. Echavarren, Chem. Eur. J. 2006, 12, 1694–1702;
- 6bS. López, E. Herrero-Gómez, P. Pérez-Galán, C. Nieto-Oberhuber, A. M. Echavarren, Angew. Chem. 2006, 118, 6175–6178; Angew. Chem. Int. Ed. 2006, 45, 6029–6032;
- 6cC. Nieto-Oberhuber, S. López, E. Jiménez-Núñez, A. M. Echavarren, Chem. Eur. J. 2006, 12, 5916–5923.
- 7
- 7aC. H. M. Amijs, C. Ferrer, A. M. Echavarren, Chem. Commun. 2007, 698–700;
- 7bP. Y. Toullec, E. Genin, L. Leseurre, J.-P. Genêt, V. Michelet, Angew. Chem. 2006, 118, 7587–7590;
10.1002/ange.200601980 Google ScholarAngew. Chem. Int. Ed. 2006, 45, 7427–7430;
- 7ceine Addition von Arenen an eine anders erzeugte Gold-Carben-Spezies: N. D. Shapiro, F. D. Toste, J. Am. Chem. Soc. 2007, 129, 4160–4161.
- 8Als Beispiel die Kristallstrukturanalyse von 3 b: farbloser Kristall (Fragment), Kristallgröße 0.47×0.39×0.20 mm3, orthorhombisch, Raumgruppe P212121, Z=4, a=9.3604(15), b=9.9285(16), c=17.935(3) Å, V=1666.8(5) Å3, ρ=1.440 g cm−3, T=200(2) K, Θmax=28.33°, MoKα-Strahlung, λ=0.71073 Å, 0.3°-ω-Scans mit CCD-Flächendetektor; 16742 Reflexe gemessen, davon 4145 unabhängig (Rint=0.0320), 3813 mit I>2σ(I); Lorentz- und Polarisations-Korrektur; empirische Absorptionskorrektur mit SADABS,[14] μ=0.11 mm−1, Tmin=0.95, Tmax=0.98, Strukturlösung mit Direkten Methoden, Verfeinerung gegen F2 mit SHELXTL-PLUS (5.10),[15] 273 Parameter verfeinert, Wasserstoffatome wurden an konstruierten Positionen reitend berücksichtigt, außer jenen am zentralen Tricyclus, die isotrop verfeinert wurden, Flack-Parameter 0.3(9), Goodness-of-fit 1.09 für die beobachteten Reflexe, R-Werte mit R1(F)=0.047, wR(F2)=0.117 für die beobachteten Reflexe, max. Restelektronendichte zwischen −0.28 und 0.40 e Å−3. CCDC-641967 (3 b), CCDC-641968 (8), CCDC-641969 (10), CCDC-641970 (12) und CCDC-641971 (16) enthalten die ausführlichen kristallographischen Daten zu dieser Veröffentlichung. Die Daten sind kostenlos beim Cambridge Crystallographic Data Centre über www.ccdc.cam.ac.uk/data_request/cif erhältlich.
- 9Substrat 9 war über eine enantioselektive Iridium-katalysierte allylische Alkylierung mit einer Enantiomerenreinheit von 98 % ee zugänglich: G. Helmchen, A. Dahnz, P. Dübon, M. Schelwies, R. Weihofen, Chem. Commun. 2007, 675–691.
- 10E. A. Peterson, L. E. Overman, Proc. Natl. Acad. Sci. USA 2004, 101, 11943–11948.
- 11
- 11aA. S. K. Hashmi, M. Rudolph, J. P. Weyrauch, M. Wölfle, W. Frey, J. W. Bats, Angew. Chem. 2005, 117, 2858–2861; Angew. Chem. Int. Ed. 2005, 44, 2798–2801;
- 11bA. S. K. Hashmi, M. C. Blanco, E. Kurpejović, W. Frey, J. W. Bats, Adv. Synth. Catal. 2006, 348, 709–713.
- 12C. A. Witham, P. Mauleón, N. D. Shapiro, B. D. Sherry, F. D. Toste, J. Am. Chem. Soc. 2007, 129, 5838–5839.
- 13
- 13aA. Padwa, M. D. Weingarten, Chem. Rev. 1996, 96, 223–270;
- 13bA. Padwa, G. E. Fryxell, L. Zhi, J. Am. Chem. Soc. 1990, 112, 3100–3109.
- 14G. M. Sheldrick, Bruker Analytical X-ray Division, Madison, Wisconsin 2001.
- 15G. M. Sheldrick, Bruker Analytical X-ray Division, Madison, Wisconsin 1997.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.