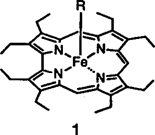
Metallocorrole mit formal vierwertigem Eisen†
Corresponding Author
Prof. Dr. Emanuel Vogel
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102Search for more papers by this authorDipl.-Chem. Stefan Will
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Search for more papers by this authorDipl.-Chem. Andreas Schulze Tilling
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Search for more papers by this authorDr. Ludger Neumann
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Search for more papers by this authorDr. Johann Lex
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Search for more papers by this authorDr. Alfred X. Trautwein
Institut für Physik der Universität Lübeck
Search for more papers by this authorProf. Dr. Karl Wieghardt
Lehrstuhl für Anorganische Chemie I der Universität Bochum
Search for more papers by this authorCorresponding Author
Prof. Dr. Emanuel Vogel
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102Search for more papers by this authorDipl.-Chem. Stefan Will
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Search for more papers by this authorDipl.-Chem. Andreas Schulze Tilling
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Search for more papers by this authorDr. Ludger Neumann
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Search for more papers by this authorDr. Johann Lex
Institut für Organische Chemie der Universität Greinstraße 4, D-50939 Köln Telefax: Int. +221/470-5102
Search for more papers by this authorDr. Alfred X. Trautwein
Institut für Physik der Universität Lübeck
Search for more papers by this authorProf. Dr. Karl Wieghardt
Lehrstuhl für Anorganische Chemie I der Universität Bochum
Search for more papers by this authorProfessor Ernst Otto Fischer zum 75. Geburtstag gewidmet
Abstract
Die ungewöhnliche Oxidationsstufe +IV für Eisenzentren kann durch den porphyrinähnlichen Corrolliganden so stabilisiert werden, daß die Verbindungen 1 (R = CI, Ph, OFe-Corrol) bei Raumtemperatur isolierbar sind. Das sauerstoffverbrückte zweikernige Eisen(IV)-corrol, das sich leicht in die einkernigen Eisen(IV)-corrole umwandeln läßt, entsteht als einziges definiertes Produkt bei der Umsetzung des Liganden mit [Fe2(CO)9] und Aufarbeitung an Luft. Die wenigen bisher bekannten Eisen(IV)-porphyrine sind demgegenüber zu unbeständig, um in Substanz gefaßt werden zu können.
References
- 1 P. R. Ortiz de Montellano, Cytochrome P-450; Structure, Mechanism and Biochemistry, Plenum, New York, 1986; R. H. Holm, Chem. Rev. 1987, 87, 1401; B. Meunier, Chem. Rev. 1992, 92, 1411; D. Ostovic, T. Bruice, Acc. Chem. Res. 1992, 25, 314.
- 2 D. Lançon, P. Cocolios, R. Guilard, K. M. Kadish, Organometallics 1984, 3, 1164; J. Am. Chem. Soc. 1984, 106, 4472; A. L. Balch, M. W. Renner, J. Am. Chem. Soc. 1986, 108, 2603; über ein bei Raumtemperatur (in Lösung) stabiles kationisches σ-Phenyleisen(IV)-porphyrin wurde inzwischen berichtet: K. M. Kadish, E. Van Caemelbecke, F. D'Souza, C. J. Medforth, K. M. Smith, A. Tabard, R. Guilard, Organometallics 1993, 12, 2411.
- 3 J. T. Groves, R. Quinn, T. J. McMurry, M. Nakamura, G. Lang, B. Boso, J. Am. Chem. Soc. 1985, 107, 354; J. T. Groves, J. A. Gilbert, Inorg. Chem. 1986, 25, 123.
- 4 D. Mansuy, J.-P. Lecomte, J.-C. Chottard, J.-F. Bartoli, Inorg. Chem. 1981, 20, 3119; K. M. Kadish, R. K. Rhodes, L. A. Bottomley, H. M. Goff, Inorg. Chem. 1981, 20, 3195; V. L. Goedken, M. R. Deakin, L. A. Bottomley, J. Chem. Soc. Chem. Commun. 1982, 607; D. R. English, D. N. Hendrickson, K. S. Suslick, Inorg. Chem. 1983, 22, 367; Inorg. Chem. 1985, 24, 121.
- 5 R. Guildard, Universität von Burgund, Dijon, persönliche Mitteilung.
- 6
A. W. Johnson,
I. T. Kay,
J. Chem. Soc.
1965,
1620;
A. W. Johnson
in
Porphyrins and Metalloporphyrins
(Hrsg.: K. M. Smith),
Elsevier,
Amsterdam,
1975,
S. 729;
R. Grigg
in
The Porphyrins,
Vol. II
(Hrsg.: D. Dolphin),
Academic Press,
New York,
1978,
S. 327;
10.1016/B978-0-12-220102-8.50017-8 Google ScholarN. S. Genokhova, T. A. Melent'eva, V. M. Berezovskii, Usp. Khim. 1980, 49, 2132 [Russ. Chem. Rev. (Engl. Transl.) 1980, 49, 1056];10.1070/RC1980v049n11ABEH002527 Google ScholarT. A. Melent'eva, Russ. Chem. Rev. (Engl. Transl.) 1983, 52, 1136 [bzw. Russ. Chem. Rev. (Engl. Transl.) 1983, 52, 641];10.1070/RC1983v052n07ABEH002871 Google ScholarK. M. Kadish, W. Koh, P. Tagliatesta, D. Sazou, R. Paolesse, S. Licoccia, T. Boschi, Inorg. Chem. 1992, 31, 2305; R. Paolesse, S. Licoccia, M. Fanciullo, E. Morgante, T. Boschi, Inorg. Chim. Acta 1993, 203, 107.
- 7 a) S. Will, A. Rahbar, H. Schmickler, J. Lex, E. Vogel, Angew. Chem. 1990, 102, 1434; Angew. Chem. Int. Ed. Engl. 1990, 29, 1390; b) E. Vogel, Pure Appl. Chem. 1993, 65, 143.
- 8 a) V. M. Leovac, R. Herak, B. Prelesnik, S. R. Niketic, J. Chem. Soc. Dalton Trans. 1991, 2295; b) N. V. Gerbeleu, Y. A. Simonov, V. B. Arion, V. M. Leovac, K. I. Turta, K. M. Indrichan, D. I. Gradinaru, V. E. Zavodnik, T. I. Malinovskii, Inorg. Chem. 1992, 31, 3264; c) U. Knof, T. Weyhermüller, T. Wolter, K. Wieghardt, E. Bill, C. Butzlaff, A. X. Trautwein, Angew. Chem. 1993, 105, 1701; Angew. Chem. Int. Ed. Engl. 1993, 32, 1635.
- 9 Weitere Beispiele für nichtporphyrinoide Eisen(IV)-Komplexe mit N4-Liganden: W. Hiller, J. Strähle, A. Datz, M. Hanack, W. E. Hatfield, L. W. ter Haar, P. Gütlich, J. Am. Chem. Soc. 1984, 106, 329; T. J. Collins, K. L. Kostka, E. Münck, E. S. Uffelman, J. Am. Chem. Soc. 1990, 112, 5637; T. J. Collins, B. G. Fox, Z. G. Hu, K. L. Kostka, E. Münck, C. E. F. Rickard, L. J. Wright, J. Am. Chem. Soc. 1992, 114, 8724; K. L. Kostka, B. G. Fox, M. P. Hendrich, T. J. Collins, C. E. F. Rickard, L. J. Wright, E. Münck, J. Am. Chem. Soc. 1993, 115, 6746. Zu sonstigen FeIV-Verbindungen siehe: F. M. Nelson in Comprehensive Coordination Chemistry, Vol. 4 (Hrsg.: G. Wilkinson, R. D. Gillard, J. A. McCleverty), Pergamon, Oxford, 1987, S. 217; D. Sellmann, M. Geck, F. Knoch, G. Ritter, J. Dengler, J. Am. Chem. Soc. 1991, 113, 3819.
- 10 Es sei hier vermerkt, daß die Oxidationszahl eines Metalls in Komplexen mit Liganden, die ausgedehnte π-Elektronensysteme aufweisen (sogenannte noninnocent ligands), wegen der Mischung von Metall- und Ligand-Orbitalen keine eindeutig definierte Größe darstellt. Zur Diskussion dieser subtilen Problematik siehe: F. C. Anson, T. J. Collins, T. G. Richmond, B. D. Santarsiero, J. E. Toth, B. G. R. T. Treco, J. Am. Chem. Soc. 1987, 109, 2974; Zitat [8c].
- 11 a) M. Conlon, A. W. Johnson, W. R. Overend, D. Rajapaksa, C. M. Elson, J. Chem. Soc. Perkin Trans. 1 1973, 2281; b) Y. Murakami, Y. Aoyama, M. Hayashida, J. Chem. Soc. Chem. Commun. 1980, 501; c) T. Boschi, S. Licoccia, R. Paolesse, P. Tagliatesta, M. A. Tehran, G. Pelizzi, F. Vitali, J. Chem. Soc. Dalton Trans. 1990, 463; d) S. Licoccia, M. Paci, R. Paolesse, T. Boschi, J. Chem. Soc. Dalton Trans. 1991, 461.
- 12 Y. Murakami, Y. Matsuda, K. Sakata, S. Yamada, Y. Tanaka, Y. Aoyama, Bull. Chem. Soc. Jpn. 1981, 54, 163. Die Synthese von Octaethylcorrol 5 durch oxidative intramolekulare Kupplung von 1,19-Didesoxyctaethylbiladien-ac-dihydrobromid erfolgte in der Weise, daß man die tetrapyrrolische Ausgangsverbindung in Methanol bei Raumtemperatur mit Chloranil in Gegenwart von Kaliumhydrogencarbonat behandelte (5 min). Das nach Zugabe von Hydrazin (zwecks Deprotonierung des Corrol-Hydrobromids und Reduktion des überschüssigen Chloranils) abgeschiedene Corrol 5 wurde durch Kristallisation (Methanol/Chloroform) in reiner Form erhalten; Schmp. 226–227°C (Ausbeutesteigerung gegenüber bisherigem Verfahren von 19 auf 60%).
- 13
7: C70H86Fe2N8O, Kristalle aus Hexan; monoklin, Raumgruppe P21/n, a = 15.589(4), b = 15.950(4), c = 25.933(7) å, β = 90.84(2)°, Z = 4; Qber. = 1.202 gcm−3; μMo = 4.98 cm−1; 10412 beobachtete Reflexe; θmax = 27°; R1 = 0.0421, WR2 = 0.1178. 8:C35H43ClFeN4 · C6H6, Kristalle aus Benzol; triklin, Raumgruppe P1, a = 10.191(2), b = 13.973(3), c = 14.684(3) å, α = 82.62(2), β = 71.19(2), γ = 69.65(2)°, Z = 2; Qber. = 1.234 gcm−3; μMo = 5.12 cm−1; 5844 beobachtete Reflexe; θmax = 27°; R1 = 0.0646, WR2 = 0.1614. 9: C41H48FeN4, Kristalle aus Hexan/Ether; triklin, Raumgruppe P1, a = 11.989(2), b = 12.443(2), c = 14.970(2) å, α = 60.39(2), β = 68.50(2), γ = 67.88(2)°, Z = 2; Qber. = 1.237 gcm−3; μMo = 4.64 cm−1; 4908 beobachtete Reflexe; θmax = 25°; R1 = 0.0644, WR2 = 0.1882. 10: C40H48FeN5, Kristalle aus Pentan/Pyridin; monoklin, Raumgruppe P21/n, a = 12.761(3), b = 14.644(4), c = 18.662(5) å, β = 95.58(2)°, Z = 4; Qber. = 1.253 gcm−3; μMo = 4.70 cm−1; 6186 beobachtete Reflexe; θmax = 27°; R1 = 0.0361, WR2 = 0.1121. Die Messung der Reflexintensitäten erfolgte auf einem Enraf-Nonius-CAD4-Diffraktometer (Raumtemperatur, MoKα-Strahlung, λ = 0.71069 å). Die Strukturen wurden mit Direkten Methoden gelöst und mit F2 für alle unabhängig beobachteten Reflexe (F
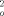 > 2 σ F
> 2 σ F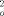 ) verfeinert (Schweratome mit anisotropen, H-Atome mit isotropen Temperaturfaktoren); WR2 = [ΣW(F
) verfeinert (Schweratome mit anisotropen, H-Atome mit isotropen Temperaturfaktoren); WR2 = [ΣW(F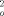 - F
- F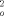 )2/ΣW(F
)2/ΣW(F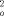 )2]1/2. Benutzte Programme: zur Strukturlösung MolEN (Enraf-Nonius) und zur Verfeinerung SHELXL-93
(G. M. Sheldrick,
Universität Göttingen). Weitere Einzelheiten zu den Kristallstrukturuntersuchungen können beim Fachinformationszentrum Karlsruhe D-76344 Eggenstein-Leopoldshafen, unter Angabe der Hinterlegungsnummer CSD-57965 angefordert werden.
)2]1/2. Benutzte Programme: zur Strukturlösung MolEN (Enraf-Nonius) und zur Verfeinerung SHELXL-93
(G. M. Sheldrick,
Universität Göttingen). Weitere Einzelheiten zu den Kristallstrukturuntersuchungen können beim Fachinformationszentrum Karlsruhe D-76344 Eggenstein-Leopoldshafen, unter Angabe der Hinterlegungsnummer CSD-57965 angefordert werden.
- 14 Zur bisher einzigen Röntgenstrukturanalyse eines unkomplexierten Corrols, des 8,12-Diethyl-2,3,7,13,17,18-hexamethylcorrols, siehe: H. R. Harrison, O. J. R. Hodder, D. C. Hodgkin, J. Chem. Soc. B 1971, 640.
- 15 a) W. R. Scheidt, C. A. Reed, Chem. Rev. 1981, 81, 543; b) W. R. Scheidt, M. Gouterman in Iron Porphyrins, Part I (Hrsg.: A. B. P. Lever, H. B. Gray), Addison-Wesley, Reading/Massachusetts, 1983, S. 89; c) W. R. Scheidt, Y. J. Lee, Struct. Bonding (Berlin) 1987, 64, 1.
- 16 W. R. Scheidt, B. Cheng, M. K. Safo, F. Cukiernik, J.-C. Marchon, P. G. Debrunner, J. Am. Chem. Soc. 1992, 114, 4420 (Zitat [8 g]).
- 17 K. Tatsumi, R. Hoffmann, J. Am. Chem. Soc. 1981, 103, 3328. Bei einem in Zitat [8 b] beschriebenen μ-Oxodieisen(IV)-Komplex mit einem Pentan-2,4-dion-bis(S-alkylisothiosemicarbazonato)-Liganden beträgt der Fe-O-Fe-Winkel sogar nur 153.7°.
- 18 Die Suszeptibilitätsmessungen erfolgten an gepulverten Proben im Temperaturbereich von 81 bis 293 K auf einer Faraday-Waage; der zugrundeliegende Diamagnetismus wurde mit Pascal-Konstanten berechnet. Die Mößbauer-Untersuchungen wurden an gepulverten Proben bei 4.2 bzw. 77 K im Nullfeld durchgeführt.
- 19 In Metalloporphyrin-Dimeren wird aufgrund der magnetischen Anisotropie der Liganden für die Perimeter-Protonen eine Hochfeldverschiebung beobachtet, die im Falle der meso-Protonen des μ-Oxodiscandium-Komplexes des Octaethylporphyrins ca. 0.5 ppm beträgt (siehe Zitat [22]). Durch Verklammerung zweier Porphyrin-Einheiten läßt sich der Abstand der Ringgerüste bis auf 3.4 å verringern, wodurch Verschiebungen bis zu 1.5 ppm zustandekommen (siehe M. O. Senge, K. R. Gerzevske, M. G. H. Vicente, T. P. Forsyth, K. M. Smith, Angew. Chem. 1993, 105, 745; Angew. Chem. Int. Ed. Engl. 1993, 32, 750). Da der mittlere Abstand der Ringgerüste in 7 4.3 å beträgt, vermag ein konventioneller Anisotropie-Effekt allein die hier festgestellten Verschiebungen kaum zu erklären.
- 20 D. M. Kurtz, Jr., Chem. Rev. 1990, 90, 585.
- 21 M. Lausmann, I. Zimmer, J. Lex, H. Lueken, K. Wieghardt, E. Vogel, Angew. Chem. 1994, 106, 776; Angew. Chem. Int. Ed. Engl. 1994, 33, Nr. 7.
- 22 J. W. Buchler, H. H. Schneehage, Z. Naturforsch. B 1973, 28, 433.
- 23 R. D. Arasasingham, A. L. Balch, R. L. Hart, L. Latos-Grazynski, J. Am. Chem. Soc. 1990, 112, 7566.
- 24 J. Ernst, J. Subramanian, J.-H. Fuhrhop, Z. Naturforsch. A 1977, 32, 1129.
- 25
G. N. La Mar,
F. A. Walker (Jensen)
in
The Porphyrins,
Vol. IV
(Hrsg.: D. Dolphin),
Academic Press,
New York,
1979,
S. 61;
10.1016/B978-0-12-220104-2.50009-0 Google ScholarH. M. Goff in Iron Porphyrins, Part I (Hrsg.: A. B. P. Lever, H. B. Gray), Addison-Wesley, Reading/Massachusetts, 1983, S. 237.
- 26 Die Zuordnung stützt sich bei 9 auf den Vergleich mit den 1H-NMR-Spektren des [D5]Phenyl-Derivats, der m-Tolyl-Verbindung und des in den meso-Positionen deuterierten Komplexes 9; bei 10 dienten die 1H-NMR-Spektren des [D5]Pyridin-Komplexes und des 3-Methylpyridin-Derivats als Referenz.
- 27 E. Bill, X.-Q. Ding, E. L. Bominaar, A. X. Trautwein, H. Winkler, D. Mandon, R. Weiss, A. Gold, K. Jayaraj, W. E. Hatfield, M. L. Kirk, Eur. J. Biochem. 1990, 188, 665.
- 28 W. R. Scheidt, D. K. Geiger, Y. J. Lee, C. A. Reed, G. Lang, Inorg. Chem. 1987, 26, 1039.
- 29 P. G. Debrunner in Iron Porphyrins, Part III (Hrsg.: A. B. P. Lever, H. B. Gray), VCH, New York, 1989, S. 137.
- 30 Das bisher einzige Beispiel hierfür ist der Oxochrom(V)-Komplex des 7,8,12,13-Tetraethyl-2,3,17,18-tetramethylcorrols: Y. Matsuda, S. Yamada, Y. Murakami, Inorg. Chim. Acta 1980, 44 L309.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.