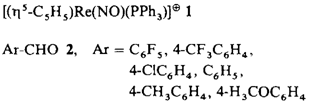Thermodynamisch kontrollierte enantiofaciale Selektivität bei der Bindung von Aldehyden an chirale Metallkomplex-Fragmente – der Mechanismus der Interkonversion diastereomerer π-Aldehyd-Komplexe [(η5-C5H5) Re(NO)(PPh3)(η2-O = CHAr)]BF4†
Diese Arbeit wurde von den National Institutes of Health gefördert. Ar steht hier für Aryl-Substituenten.
Abstract
Je höher die π-Acidität des Aldehyd-Liganden desto ausgeprägter die chirale Erkennung bei seiner Bindung an das chirale Komplexfragment 1. Dies ist das Ergebnis Tieftemperatur-NMR-spektroskopischer Untersuchungen der Komplexe von 1 mit den aromatischen Aldehyden 2, die zudem zeigten, daß sich die diastereomeren π-Aldehyd-Komplexe aus 1 und 2 intramolekular über einen σ-Aldehyd-Komplex ineinander umwandeln.