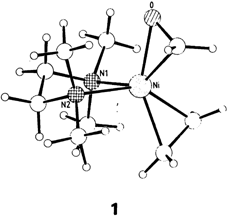
Synthese und Struktur des Formaldehydkomplexes [(tmeda)Ni(C2H4)(H2CO)]†
Wolfgang Schröder Dipl.-Chem.
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1
Search for more papers by this authorCorresponding Author
Dr. Klaus R. Pörschke
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1Search for more papers by this authorDr. Yi-Hung Tsay
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1
Einkristall-Strukturanalyse.
Search for more papers by this authorProf. Dr. Arl Krüger
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1
Search for more papers by this authorWolfgang Schröder Dipl.-Chem.
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1
Search for more papers by this authorCorresponding Author
Dr. Klaus R. Pörschke
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1Search for more papers by this authorDr. Yi-Hung Tsay
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1
Einkristall-Strukturanalyse.
Search for more papers by this authorProf. Dr. Arl Krüger
Max-Planck-Institut für Kohlenforschung Postfach 101353, D-4330 Mülheim a. d. Ruhr 1
Search for more papers by this authorTmeda-Nickel-Komplexe, 2. Mitteilung. TMEDA = N,N,N′,N′-Tetramethylethylendiamin. — 1. Mitteilung: [1].
Abstract
Der Ethen und Formaldehyd enthaltende Titelkomplex 1 kann in bis zu 35% Ausbeute in Form orangeroter, bis −15°C beständiger Kristalle durch Umsetzung von Tris(ethen)nickel, Paraformaldehyd und N,N,N′,N′-Tetramethylethylendiamin (TMEDA) erhalten werden. Im Unterschied zu Formaldehydkomplexen stärker oxophiler Metalle ist in 1 die NiC- kürzer als die NiO-Bindung (1.936(2) bzw. 1.966(1) Å). 1 interessiert als Modellverbindung für Zwischenstufen der Fischer-Tropsch-Synthese.
References
- 1 W. Schröder, K. R. Pörschke, J. Organomet. Chem. 322 (1987) 385.
- 2 H. Pichler, H. Schulz, Chem.-Ing.-Tech. 42 (1970) 1162.
- 3 Beispiele: a) [{Cp2Zr(H2CO)}3]: K. Kropp, V. Skibbe, G. Erker, C. Krüger, J. Am. Chem. Soc. 105 (1983) 3353; (b) [Cp2V(H2CO)]: S. Gambarotta, C. Floriani, A. Chiesi-Villa, C. Guastini, J. Am. Chem. Soc. 104 (1982) 2019; Organometallics 5 (1986) 2425; (c) [Cp2Mo(H2CO)]: G. E. Herberich, J. Okuda, Angew. Chem. 97 (1985) 400; Angew. Chem. Int. Ed. Engl. 24 (1985) 402; S. Gambarotta, C. Floriani, A. Chiesi-Villa, C. Guastini, J. Am. Chem. Soc. 107 (1985) 2985; (d) [(Me3P)4WH2(H2CO)]: M. L. H. Green, G. Parkin, K. J. Moynihan, K. Prout, J. Chem. Soc. Chem. Commun. 1984, 1540; [(Me3P)3W(C4H6)(H2CO)]: M. L. H. Green, G. Parkin, J. Chem. Soc. Chem. Commun. 1986, 90; (e) [Cp(NO)Re(PPh3)(H2CO)][PF6]: W. E. Buhro, A. T. Patton, C. E. Strouse, J. A. Gladysz, F. B. McCormick, M. C. Etter, J. Am. Chem. Soc. 105 (1983) 1056; (f) [{(MeO)3P}2(CO)2Fe(H2CO)]: H. Berke, G. Huttner, G. Weiler, L. Zsolnai, J. Organomet. Chem. 219 (1981) 353; H. Berke, R. Birk, G. Huttner, L. Zsolnai, Z. Naturforsch. B39 (1984) 1380; (g) [(Ph3P)2(CO)2Os(H2CO)]: K. L. Brown, G. R. Clark, C. E. L. Headford, K. Marsden, W. R. Roper, J. Am. Chem. Soc. 101 (1979) 503; G. R. Clark, C. E. L. Headford, K. Marsden, W. R. Roper, J. Organomet. Chem. 231 (1982) 335; (h) [(Et3P)2Pt(H2CO)]: R. A. Head, J. Chem. Soc. Dalton Trans. 1982, 1637.
- 4(a) E. L. Muetterties, J. Stein, Chem. Rev. 79 (1979) 479; (b) W. A. Herrmann, Angew. Chem. 94 (1982) 118; Angew. Chem. Int. Ed. Engl. 21 (1982) 117.
- 5(a) S. Sakaki, K. Kitaura, K. Morokuma, K. Ohkubo, Inorg. Chem. 22 (1983) 104; (b) C. Bianchini, A. Meli, Organometallics 4 (1985) 1537.
- 6 W. Schröder, Diplomarbeit, Universität Bonn 1986.
- 7(a) B. Bogdanović, M. Kröner, G. Wilke, Justus Liebigs Ann. Chem. 699 (1966) 1; (b) K. Fischer, K. Jonas, G. Wilke, Angew. Chem. 85 (1973) 620; Angew. Chem. Int. Ed. Engl. 12 (1973) 565.
- 8 Arbeitsvorschrift (unter Ausschluß von Sauerstoff): 3: Eine aus 1.165 g (5.0 mmol) 95proz. 1 [7a] und Ethen hergestellte Lösung von 2 [7b] in 20 mL Ether wird mit 2 mL TMEDA und 1 g Paraformaldehyd versetzt und 60 h bei -30°C gerührt. Nach Filtration über eine D4-Kühlmantelfritte scheiden sich bei -78°C langsam orangerote Kristalle ab, die man nach Entfernen der Mutterlauge mittels Kapillarheber zweimal mit kaltem Pentan wäscht und im Hochvakuum bei -30°C trocknet. Ausbeute 360 mg (31%). Es liegen korrekte Elementaranalysenwerte vor.
- 9 4: Ausbeute nicht optimiert; korrekte Elementaranalyse. - IR (KBr, -30°C): v = 1595 cm−1 (H2C = O); 1H-NMR ([D8]THF, 400 MHz, relativ TMS, -80°C): δ = 3.64 (t, H2CO), 1.14 (d,J(PH) = 7.2 Hz, PMe3), 1.12 (d,J(PH) = 6.4 Hz, PMe3); 13C-NMR ([D8]THF, 75.5 MHz, -80°C): δ = 70.9 (J(CH) = 165 Hz, 2J(PC) = 17.8 Hz, H2CO), 18.4 (1 J(PC) = 24.0 Hz, 3J(PC) = 4.0 Hz, PMe3), 16.4 (J(PC) = 19.3 Hz, PMe3); 31P{1H}-NMR ([D8]THF, 32.4 MHz, relativ 85proz. wäßrige H3PO4, -30°C): δ = -6.6 (d), -18.3 (d,J(PP) = 57 Hz).
- 10 3: IR (KBr, -40°C): v = 1605 cm−1 (H2CO); 1H-NMR ([D8]THF, 400 MHz, relativ TMS, -110°C): δ = 4.58 (d), 4.23 (d, 2J(H1H1′) = 21 Hz, H2CO), 3.04, 2.85, 2.25, 2.17 (NCH2, tmeda), 2.64, 2.54, 2.28, 2.07 (NCH3, tmeda), 2.07, 1.81 (H2CCH2); (−80°C): δ = 4.45 (H2CO), 2.55 (NCH2), 2.38 (NCH3), 1.92 (C2H4); 13C-NMR ([D8]THF, 75.5 MHz, relativ TMS, -120°C): δ = 82.3 (t,J (CH) = 163 Hz, H2CO), 46.2, 35.8 (breit, H2CCH2), 59.3, 58.8 (NCH2, tmeda), 51.8, 49.6, 44.9, 44.3 (NCH3, tmeda); (−80°C): δ = 82.7 (H2CO), 59.15 (NCH2), 52 bis 44 (NCH3), 41.2 (C2H4). Wir danken Dr. R. Benn und Dr. R. Mynott für die NMR-Spektren.
- 11(a) H. H. Blau Jr., H. H. Nielsen, J. Mol. Spectrosc. 1 (1957) 124; (b) M. Hesse, H. Meier, B. Zech: Spektroskopische Methoden in der Organischen Chemie, Thieme, Stuttgart 1979, S. 158; (c) H.-O. Kalinowski, S. Berger, S. Braun: 13C-NMR-Spektroskopie, Thieme, Stuttgart 1984, S. 173; (d) P. C. Lauterbur, J. Chem. Phys. 26 (1957) 217; (e) C. Kato, S. Konaka, T. Iljima, M. Kimura, Bull. Chem. Soc. Jpn. 42 (1969) 2148.
- 12 Monomerer Formaldehyd: δ(H) = 9.6 [3c], 2J(HH) = 42.2 Hz [11b], δ(C) = 197.0 [11c], J(CH) = 172 Hz [11d].
- 13 Kristallstrukturanalyse von 3: 0.55 mm × 0.52 mm × 0.19 mm Kristallgröße, Raumgruppe P21/n, a = 8.964(1),b = 11.571(1),c = 11.918(1)Å, β = 107.00(1)°,V = 1182.1 Å3,Z = 4, ρber. = 1.31 g cm−3, μ(MoKα) = 16.18 cm−1; Meßtemperatur -72°C; 9899 Reflexe gemessen (±h, ±k, + l), gemittelt zu 4752 unabhängigen Reflexen, davon 2721 als beobachtet eingestuft (I> 2σ(I)); empirische Absorptionskorrektur, Schweratommethode; H-Atome gefunden und isotrop verfeinert; 206 Parameter,R = 0.029; Rw = 0.026. Weitere Einzelheiten zur Kristallstrukturuntersuchung können beim Fachinformationszentrum Energie, Physik, Mathematik GmbH, D-7514 Eggenstein-Leopoldshafen 2, unter Angabe der Hinterlegungsnummer CSD-52215, der Autoren und des Zeitschriftenzitates angefordert werden.
- 14(a)
K. R. Pörschke,
W. Kleimann,
G. Wilke,
K. H. Claus,
C. Krüger,
Angew. Chem.
95
(1983)
1032;
10.1002/ange.19830951240 Google ScholarAngew. Chem. Int. Ed. Engl. 22 (1983) 991; (b) K. R. Pörschke, K. Jonas, G. Wilke, R. Benn, R. Mynott, R. Goddard, C. Krüger, Chem. Ber. 118 (1985) 275.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.