Spättypreaktionen auf oral und parenteral verabreichte Arzneimittel
Redaktion
Prof. Dr. D. Nashan, Dortmund
Makulopapulöse Arzneimittelreaktionen als Ausdruck einer T-Zell-vermittelten Spättypreaktion bzw. einer Intoleranzreaktion sind die häufigsten durch Medikamente ausgelösten Hauterkrankungen.
Die Sensibilisierungsphase kann bei ausreichend langer Applikation des Arzneimittels direkt in die Auslösephase übergehen.
Das klinische Bild der Spättypreaktion kann aufgrund der Heterogenität der T-Zell-Antwort stark variieren.
Dosis, Dauer der Applikation, Geschlecht, immungenetische Prädisposition und der aktuelle Aktivierungsstatus des Immunsystems gelten als relevante Faktoren für Sensibilisierungswahrscheinlichkeit und Intensität der Reaktion.
Insbesondere virale Infektionen gehen mit einer Aktivierung des Immunsystems und dadurch mit einer gesteigerten Bereitschaft für die Entwicklung von Arzneimittelreaktionen einher.
Schwere Arzneimittelreaktionen kündigen sich in der Initialphase durch typische Alarmzeichen an.
Eine allergologische Abklärung sollte bei begründetem Verdacht erfolgen, da eine erneute Exposition gegenüber dem verantwortlichen Arzneimittel – insbesondere nach einer vorausgegangenen schweren Reaktion – fatale Folgen für den Patienten haben kann.
Auch ein über viele Jahre appliziertes und vertragenes Medikament kann Auslöser einer Arzneimittelreaktion sein.
Eine gründliche dermatologische Untersuchung unter Einschluss der hautnahen Schleimhäute und Adnexstrukturen ist bei allen vermuteten arzneimittelinduzierten Erkrankungen unverzichtbar.
An der Haut gehen Soforttypreaktionen oft mit Urticae und Angioödemen einher, während Spättypreaktionen überwiegend in Form makulöser/makulopapulöser Hautveränderungen manifest werden.
Zum Nachweis einer Spättypreaktion werden Intrakutan- bzw. Scratch- und Epikutantests sowie gegebenenfalls Provokationstestungen mit den verdächtigten Arzneimitteln und/oder Ausweichpräparaten durchgeführt.
Bei fixen Arzneimittelexanthemen sollten zusätzlich In-loco-Testungen durchgeführt werden.
Eine Bestimmung spezifischer IgE-Antikörper ist bei Spättypreaktionen nicht zielführend.
Ist eine Identifikation des für die Reaktion verantwortlichen Arzneimittels durch Anamnese, Hauttestungen und/oder In-vitro-Testverfahren nicht möglich, kann eine Provokationstestung indiziert sein.
Im Gegensatz zu Soforttypreaktionen ist für die Auslösung von Spättypreaktionen oftmals die tatsächliche Tagesdosis notwendig.
Allergologische Testungen ohne anamnestischen Hinweis auf eine Unverträglichkeitsreaktion (prophetische Testungen) machen keinen Sinn.
Für alle diagnostischen Maßnahmen gilt, dass weder negative Haut- und In-vitro-Tests noch negative Resultate der Expositionstestungen eine Arzneimittelallergie bzw. -intoleranz sicher ausschließen.
Bei exanthematischen makulösen/makulopapulösen Hautveränderungen stellen viral bedingte Exantheme die wichtigste Differenzialdiagnose dar.
Kommen mehrere Medikamente als Auslöser in Frage, so sollte zunächst das am wahrscheinlichsten ursächliche Arzneimittel gemieden werden.
Reichen topische Glukokortikoide nicht aus, kann eine ergänzende Therapie mit systemisch wirksamen Kortikosteroiden angezeigt sein.
Ciclosporin A weist neueren Daten zu Folge eine gute Wirksamkeit bei der Behandlung von SJS/TEN auf.
Bei einem DRESS-Syndrom mit Beteiligung innerer Organe ist eine Behandlung mit systemisch applizierten Kortikosteroiden notwendig.
Besteht lediglich ein leicht ausgeprägtes makulopapulöses Exanthem, kann ein Durchbehandeln erwogen werden.
Toleranzinduktionen bei Hypersensitivitätsreaktionen vom Spättyp haben nur geringe Erfolgsaussichten.
Bei Patienten, bei denen aufgrund der Vorgeschichte eine allergische Reaktion wahrscheinlich ist und für die kein alternatives Arzneimittel zur Verfügung steht, kann eine prophylaktische systemische Therapie mit einem Glukokortikoid versucht werden.
Bis auf wenige Ausnahmen können nahezu alle Arzneimittel Unverträglichkeitsreaktionen vom Spättyp hervorrufen.
Vor allem Aminopenicilline rufen häufig Spättypreaktionen hervor.
Kreuzreaktionen zwischen Penicillinen und Cephalosporinen kommen weit seltener vor, als allgemein vermutet.
Cotrimoxazol gehört zu den häufigen Auslösern kutaner, aber auch schwerer systemischer Arzneimittelreaktionen.
Sowohl makulopapulöse und fixe Arzneimittelexantheme als auch photoallergische/phototoxische und schwere Hypersensitivitätsreaktionen wie die AGEP und das SJS/TEN sind für Fluorchinolone beschrieben.
Makrolide gelten als besonders sichere Arzneimittel.
Tetrazykline sind häufige Auslöser phototoxischer Reaktionen und selten auch Ursache des SJS/TEN, systemischer Hypersensitivitätsreaktionen und fixer Arzneimittelexantheme.
Schwere Arzneimittelreaktionen unter einer Clindamycin-Therapie sind selten.
Vancomycin ist als häufige Ursache makulopapulöser Exantheme, aber auch als Auslöser des DRESS-Syndroms bekannt.
Flush-artige Hautveränderungen unter einer Vancomycintherapie sind ungefährlich und bilden sich binnen Stunden spontan zurück.
Zellvermittelte exanthematische Spättypreaktionen treten unter NSAR selten auf.
Relativ häufig sind NSAR Ursache fixer Arzneimittelexantheme.
Nach Gabe von Röntgenkontrastmittel auftretende Hautveränderungen sind meist selbstlimitierend und heilen meist binnen drei bis sieben Tagen spontan ab.
Auslöser der Reaktionen ist nahezu immer das gesamte Kontrastmittelmolekül und nicht das daran gebundene Iod.
Lokalanästhetika vom Amidtyp lösen seltener Allergien aus als solche vom Estertyp und sollten deshalb bevorzugt werden.
Spättypreaktionen auf Lokalanästhetika sind selten.
Allopurinol ist häufiger Auslöser schwerer Hypersensitivitätsreaktionen. Patienten mit dem HLA-B*5801 Allel sind besonders gefährdet.
Aromatische Antiepileptika wie Carbamazepin, Phenytoin, Phenobarbital und Lamotrigin sind unter den Antikonvulsiva die häufigsten Auslöser allergischer Hypersensitivitätsreaktionen vom Spättyp.
Unter einer antiretroviralen Therapie treten sehr häufig auch kutane Reaktionen vom Spättyp auf. Ursache hierfür ist vermutlich die durch die HIV-Infektion bedingte Dysregulation des Immunsystems sowie eine veränderte Arzneimittelmetabolisierung.
Terbinafin ist eine relativ häufige Ursache für Spättypreaktionen.
Hypersensitivitätsreaktionen auf Tuberkulostatika manifestieren sich überwiegend während der ersten beiden Behandlungsmonate.
Bis zu 7,5 % der mit niedermolekularen Heparinen therapierten stationären Patienten und etwa 20 % der mit dieser Arzneimittelgruppe behandelten Schwangeren entwickeln eine allergische Hypersensitivitätsreaktion vom Spättyp.
Nadroparin löst häufiger als jedes andere niedermolekulare Heparin bei Schwangeren Hypersensitivitätsreaktionen aus und sollte deshalb bei dieser Patientinnengruppe nicht verwendet werden.
Allergische Reaktionen auf Clopidogrel treten meist 5–7 Tage nach Therapiebeginn in Form generalisierter makulöser oder makulopapulöser Exantheme auf.
Sehr viel häufiger als das Insulinmolekül selbst sind in Insulinpräparaten enthaltene Zusatzstoffe Auslöser von Spättypreaktionen.
Diltiazem gehört zu den häufigen Auslösern der AGEP.
Biologika sind selten Auslöser ausgeprägter Spättypreaktionen.
Interferon-α ist ein relativ häufig Auslöser ekzematöser Hautveränderungen.
Auch in Arzneimitteln enthaltene Zusatzstoffe sind gelegentlich Auslöser von Spättypreaktionen.
Zusammenfassung
Spättypreaktionen auf Arzneimittel gehören zu den häufigsten Ursachen für Dermatosen überhaupt und manifestieren sich überwiegend in Form relativ harmloser exanthematischer, makulöser oder makulopapulöser Läsionen. Etwa zwei Prozent der betroffenen Patienten allerdings entwickeln schwere oder gar lebensbedrohliche, mit systemischen Immunreaktionen und damit verbundenen Organbeteiligungen einhergehende Reaktionen, die frühestmöglich erkannt und adäquat behandelt werden müssen. Zahlreiche Medikamente können Auslöser dieser Hypersensitivitätsreaktionen sein; Antibiotika, Antiepileptika und der Xanthinoxidase-Inhibitor Allopurinol sind die häufigsten. Neben einer genetischen Prädisposition gelten hohe Dosen, Behandlungen mit multiplen Arzneimitteln, lange Therapiezeiten, weibliches Geschlecht sowie akute oder chronische Infektionen als prädisponierende Faktoren.
Einleitung
Definition
Hypersensitivitätsreaktionen sind gemäß einer Konsensuserklärung der World Allergy Organization (WAO) als objektiv reproduzierbare Symptome definiert, die durch Exposition gegenüber einem bestimmten Stimulus in einer Dosis hervorgerufen werden, die von Normalpersonen problemlos toleriert wird. Demnach fallen sowohl allergische, d. h. über spezifische immunologische Mechanismen vermittelte, als auch nichtallergische Reaktionen (pseudoallergische, idiosynkratische oder Intoleranzreaktionen) unter den Überbegriff Hypersensitivitätsreaktion. Neben den Arzneimittel-induzierten IgE- (Typ I nach Gell und Coombs) und nicht IgE-Antikörper vermittelten Soforttypreaktionen sind die durch T-Lymphozyten vermittelten Spättypreaktionen (Typ IV) von besonderer Bedeutung. Die verzögert auftretenden IgG- (zytotoxische Reaktion, Typ II) bzw. IgG- und/oder IgM-vermittelten Reaktionen (Immunkomplex-vermittelte Reaktion, Typ III) spielen aufgrund ihres relativ seltenen Vorkommens im Rahmen medikamentöser Hypersensitivitätsreaktionen eine untergeordnete Rolle.
Diese oben angeführten Reaktionen sind nicht vorhersehbar, nur bedingt dosisabhängig und werden als Typ-B-Reaktionen kategorisiert, während vorhersehbare, dosisabhängige unerwünschte Arzneimittelwirkungen (UAW), wie etwa gastrointestinale Beschwerden nach Einnahme nichtsteroidaler Antirheumatika, als Typ-A-Reaktionen bezeichnet werden und somit keine Hyperreaktivitätsreaktionen sind.
Epidemiologie
Die genaue Inzidenz der durch systemisch wirksame Arzneimittel hervorgerufenen Spättypreaktionen ist nicht bekannt. Als gesichert gilt, dass die exanthematische makulopapulöse Arzneimittelreaktion als Ausdruck einer T-Zell-vermittelten Spättypreaktion bzw. einer Intoleranzreaktion die häufigste durch Medikamente ausgelöste Hauterkrankung ist. Hospitalisierte Patienten sind sehr viel häufiger als ambulante betroffen, da erstere in der Regel schwerer erkrankt sind und deshalb mit multiplen Medikamenten therapiert werden. Für diese wird die Inzidenz mit 2–8 % angegeben 1, 2, für schwere, durch Arzneimittel ausgelöste Spättypreaktionen liegt sie bei 1–5/1 000 000 3.
Chronologie und Mechanismen der Spättypreaktion
Grundlage für die Entwicklung einer Allergie ist eine vorausgegangene immunologische Phase (Sensibilisierung gegen ein Antigen), die bei leicht- bis mittelgradig ausgeprägten Arzneimittelreaktionen in der Regel zwischen fünf und zehn Tagen dauert (Tabelle 1). Bei einer erneuten Exposition tritt üblicherweise mit einer Latenz von sechs bis 48 Stunden eine Hypersensitivitätsreaktion auf, die je nach Sensibilisierungsgrad und Effektorzellen mehr oder weniger stark ausgeprägt ist. Bei ausreichend langer Exposition gegenüber dem Allergen allerdings kann die Sensibilisierungsphase direkt in die Auslösephase übergehen; ein neu eingesetztes Arzneimittel kann somit ab dem fünften Applikationstag eine klinisch manifeste allergische Reaktion induzieren. In seltenen Fällen treten Hypersensitivitätsreaktionen aber auch noch ein bis zwei Tage nach Absetzen des Arzneimittels auf. Bei schweren Arzneimittelreaktionen hingegen variiert die Zeit von der Erst-Exposition bis zum Auftreten von Symptomen erheblich (Tabelle 2).
Tabelle 1. Leicht ausgeprägte kutane Arzneimittelreaktionen
| Makulöses/makulopapulöses (morbilliformes) Arzneimittelexanthem | Fixes Arzneimittelexanthem (FAE) | Symmetrical drug-related intertriginous and flexural exanthema (SDRIFE) | |
|---|---|---|---|
| Hautveränderungen | Initial meist makulöse, im Verlauf häufig makulopapulöse HV in symmetrischer Verteilung, die zur Konfluenz neigen; an Extremitäten geleg. urtikariell imponierende HV | Meist solitäre Läsion, selten multilokuläres Auftreten; relativ scharf begrenzte, rundliche, rötlich-bräunliche HV; geleg. zentrale Epidermolyse/Blase; oft postinflammatorische Hyperpigmentierung, Wiederauftreten stets in loco, bei wiederholten Reexpositionen sind schwere, potenziell lebensbedrohliche Verläufe mit multilokulären/generalisiert bullösen Manifestationsformen (GBFDE) möglich | Symmetrisches, relativ scharf begrenztes, makulöses Erythem |
| Lokalisation/Verteilung | Beginn am Rumpf, im Verlauf zentrifugale Ausbreitung; Gesicht nur selten betroffen SH i. d. R. ausgespart | Lippen/MSH, Gesicht, Hände und Füße, Genitalienregion | Große Beugen, Gluteal- und Genitalregion |
| Systemische Symptome/pathologische Laborparameter | Evtl. leichtes Fieber | I.d.R. keine | Selten hohes Fieber u./o. Krankheitsgefühl |
| Latenz* | 5-10 Tage | 5-10 Tage | 5-10 Tage |
| Mortalität | Praktisch nie | Praktisch nie (Ausnahme: GBFDE) | Praktisch nie |
| Häufige Auslöser | Aminopenicilline, Cephalosporine, Sulfamethoxazol, Antikonvulsiva | Sulfonamide, NSAR, Paracetamol, Tetrazykline, Barbiturate, Pseudoephedrine | β-Lactam-Antibiotika (v. a. Aminopenicilline) |
- Abk.: HV, Hautveränderungen; SH, Schleimhaut; GBFDE, generalisiertes bullöses fixes Arzneimittelexanthem; MSH, Mundschleimhaut.
- von Erst-Exposition bis Auftreten der Symptomatik.
Tabelle 2. Schwere/bedrohliche Arzneimittelreaktionen
| Erythema exsudativum multiforme (EEM)-artig | Stevens-Johnson-Syndrom (SJS)/Toxische epidermale Nekrolyse (TEN) | Drug reaction with eosinophilia and systemic symptoms (DRESS) | Akute generalisierte exanthematische Pustulose (AGEP) | |
|---|---|---|---|---|
| Hautveränderungen | Typische Kokarden-artige HV1, evtl. mit zentralem Bläschen (target lesions); evtl. erosive SH-Läsionen, v. a. der MSH | Atypische Kokarden-artige1 u./o. lividrote, makulöse, teils konfluierende Läsionen; Blasen/großflächige Hautablösungen (SJS < 10 %, SJS/TEN Übergangsform 10–30 %, TEN > 30 % der KOF), Nikolski-Zeichen positiv | Initial ödematöses, morbilliformes Exanthem, im Verlauf oftmals ausgeprägte erythematöses Exanthem (Erythrodermie) und exfoliative Dermatitis, geleg. Pusteln | Zahlreiche kleine, sterile, nicht-follikulär gebundene Pusteln (< 5 mm) auf ödematös-erythematösem Grund; eruptives Auftreten (binnen Stunden); Pruritus, brennende Missempfindungen |
| Lokalisation/Verteilung der Hautveränderungen | Akrofaziale Betonung inkl. palmoplantar, Extremitäten-Streckseiten; evtl. gesamtes Integument mit (EEM majus- artig) od. ohne SH-Beteiligung (EEM minor-artig) | Gesicht, Hals u. Rumpf, palmoplantar; schwere SH-Beteiligung mit Erosionen/Ulzerationen; bei TEN nahezu immer SH-Beteiligung, v. a. konjunktivale und MSH | Generalisiert, symmetrisch; häufig faziales Ödem; SH nur selten bzw. gering betroffen | Häufig initial nur fazial und intertriginös, im Verlauf gesamtes Integument, v. a. Rumpf u. Intertrigines befallen; oft auch Purpura, Petechien, Bläschen; selten SH-Beteiligung |
| Klinische Zeichen/systemische Symptome/pathologische Laborparameter | Geleg. Fieber, Krankheitsgefühl u./o. Arthralgien | Fieber, ausgeprägtes Krankheitsgefühl, Anämie und/oder Leukopenie | Fieber > 38,5°C; Hepatitis, gelegl. interstitielle Nephritis; Juckreiz, seltener brennende Missempfindungen; periphere Lymphadenopathie; ausgeprägte Lymphozytose mit Eosinophilie u./o. atypischen Lymphozyten, Thrombozytopenie; HHV-Reaktivierungen (v. a. HHV6, aber auch HHV7, EBV, CMV) | Fieber > 38°C; Juckreiz oder brennende Missempfindungen; Leukozytose mit meist ausgeprägter Neutrophilie, mäßige Eosinophilie |
| Mögliche Komplikationen | I. d. R. keine | Akute Niereninsuffizienz, selten Hepatitis | Pneumonitis, Myokarditis u./o. ZNS-Beteiligung; Autoimmunkrankheiten als mögliche Spätfolge | Hepatitis, akute Niereninsuffizienz |
| Latenz* | 5–14 Tage | 4–28 Tage | 10–60 Tage und mehr | < 4 Tage |
| Mortalität | Selten | SJS bis 9 %, SJS/TEN bis 29 %, TEN bis 49 % | Bis 10 % | Mortalität 2 bis 5 % |
| häufige Auslöser | Sulfonamide, Antikonvulsiva, Allopurinol (häufigste Ursache sind virale Infektionen) | Carbamazepin, Allopurinol, Sulfonamid-Antibiotika, Lamotrigin, Nevirapin, NSAR (Oxicam-Typ), Phenobarbital, Phenytoin | Carbamazepin, Phenobarbital, Lamotrigin, Allopurinol, Sulfasalazin, Antibiotika (Sulfonamide, Fluorchinolone, β-Laktame), Abacavir, Nevirapin | Aminopenicilline, Fluorchinolone, Makrolide, Sulfonamid-Antibiotika, (Hydroxy)Chloroquin, Terbinafin, Diltiazem, seltener Carbamazepin |
- Abk.: KOF, Körperoberfläche; GIT, Gastrointestinaltrakt; HHV, humanes Herpes-Virus; HV, Hautveränderungen; SH, Schleimhaut; MSH, Mundschleimhaut; NSAR, nichtsteroidale Antirheumatika.
- *von Erst-Exposition bis Auftreten der Symptomatik.
- 1Typische Kokarden bestehen aus einem von zwei konzentrischen Ringen umgebenen zentralen Erythem (3-Zonen-Aufbau) und sind gegenüber der umgebenden Haut scharf abgegrenzt, während atypische Kokarden sich weniger gut demarkieren, einen weniger deutlichen zonalen Aufbau (2-Zonen-Aufbau) aufweisen und zur Konfluenz neigen 23.
Neben diesem klassischen Weg einer durch Arzneimittel ausgelösten Spättypreaktion scheint es noch eine weitere Möglichkeit der Aktivierung von T-Zellen zu geben. Das sogenannte p-i-Konzept (pharmakologische Interaktion von Medikamenten mit Immunrezeptoren) postuliert eine direkte Bindung eines nicht prozessierten und nicht an ein Hapten-gebundenen Arzneimittels an einen zufällig passenden T-Zell-Rezeptor oder an ein MHC-Molekül. Hieraus resultiert eine T-Zell-Stimulation, die einer Typ-IV-Reaktion vergleichbar ist und die entsprechende klinische Symptome induziert. Im Gegensatz zur Typ-IV-Reaktion ist beim p-i-Konzept eine vorausgegangene Arzneimittel-spezifische Sensibilisierung nicht notwendig.
Das klinische Bild der Spättypreaktion kann stark variieren (Abbildung 1a–g). Ursache für dieses Phänomen ist unter anderem die Heterogenität der T-Zell-Antwort und die damit einhergehenden unterschiedlichen sezernierten Zytokinmuster bzw. freigesetzten zytotoxischen Proteine. Dieser Erkenntnis wurde 2003 durch eine Subklassifikation der T-Lymphozyten-vermittelten Typ-IV-Reaktion in die vier Untergruppen Typ IVa bis IVd Rechnung getragen (Tabelle 3) 4.
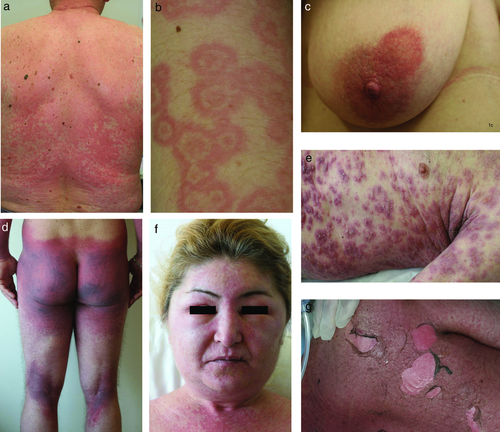
Tabelle 3. Spättypreaktionen Typ Iva–IVd (modifiziert nach 4)
| Typ IVa | Typ IVb | Typ IVc | Typ IVd | |
|---|---|---|---|---|
| Prädominierende Effektorzellen | Th1-Zellen | Th2-Zellen | Zytotoxische T-Zellen | T-Zellen |
| Zytokine/zytotoxische Proteine | IFN-γ, TNF-α | IL-4, IL-5, IL-13 | Perforin, Granzyme B, Granulysin | CXCL8/IL-8, GM-CSF, IL-5, (IL-17, IL-22?), Granulysin |
| Antigenpräsentation | Durch APZ oder direkte T-Zell-Stimulation | Durch APZ oder direkte T-Zell-Stimulation | Durch APZ oder direkte T-Zell-Stimulation | Durch APZ oder direkte T-Zell-Stimulation |
| Weitere Effektorzellen | Monozyten und Makrophagen | Eosinophile Granulozyten | T-Zellen | Neutrophile Granulozyten |
| Beispiele | Kontaktdermatitis (in Kombination mit Typ IVc), Tuberkulin-Reaktion | Makulopapulöses Exanthem mit Eosinophilie | Makulopapulöses und bullöses Exanthem (SJS/TEN), Kontaktdermatitis (in Kombination mit Typ IVa), Hepatitis | AGEP, Morbus Behçet |
- Abk.: APZ, Antigen-präsentierende Zellen; T-Zell, T-Lymphozyten.
Die Rückbildungsphase nach Absetzen des ursächlichen Agens dauert bei leicht- bis mittelgradig ausgeprägten makulopapulösen Exanthemen etwa acht bis zehn Tage, schwerer verlaufende Hautreaktionen benötigen oft mehrere Wochen bis zur vollständigen Abheilung. Hautveränderungen und zeitlicher Verlauf der Spättypreaktion unterscheiden sich somit deutlich von denen der Soforttypreaktion (Typ I), bei der Urticae häufig binnen Minuten bis zu zwölf Stunden nach Allergenexposition auftreten und gegebenenfalls gemeinsam mit weiteren Symptomen wie Angioödemen, Dyspnoe, Schluck- und gastrointestinalen Beschwerden sowie Kreislaufdysregulation das klinische Bild bestimmen.
Risikofaktoren für allergische- und Intoleranzreaktionen vom Spättyp
Verschiedene Faktoren können das Risiko für die Entwicklung einer Arzneimittelreaktion signifikant erhöhen (Tabelle 4). So gelten Dosis, Dauer der Applikation, Geschlecht, immungenetische Prädisposition und der aktuelle Aktivierungsstatus des Immunsystems als relevante Faktoren für Sensibilisierungswahrscheinlichkeit und die Intensität der Reaktion.
Tabelle 4. Risikofaktoren für die Entwicklung von Arzneimittelreaktionen
| Patienten-assoziierte Risikofaktoren |
|---|
▸ weibliches Geschlecht ▸ vorausgegangene Arzneimittel-Hypersensitivitätsreaktionen* ▸ bestehende Infektionskrankheiten, insbes. virale Infektionen (HIV, HHV) ▸ immungenetische Faktoren (HLA-Typ) ▸ Kreuzsensibilisierungen ▸ Leber- u./o. Niereninsuffizienz |
| Arzneimittel-assoziierte Risikofaktoren |
▸ Therapie mit multiplen Arzneimitteln (> 5 Medikamente) ▸ Applikationsroute des Medikamentes → topische Applikation> s.c.> i.m.> oral ▸ Intermittierende/wiederholte Therapie mit mittelhohen Dosen (Langzeitbehandlungen ohne Unterbrechung der Therapie erhöhen das Risiko nicht) |
- *Trifft nicht für SJS/TEN zu.
Ein ebenfalls erhöhtes Risiko haben Menschen mit bestimmten HLA-Allelen. In Abhängigkeit der ethnischen Herkunft werden so beispielsweise Abacavir (HLA-B*57:01), Allopurinol (HLA-B*58:01), Amoxicillin/Clavulansäure (HLA-DRB1*15:01), Carbamazepin (HLA-B*15:02/HLA-A*31:01) und Sulfamethoxazol (HLA-B*38) nicht vertragen und verursachen bei diesen Patienten nahezu obligat schwere Arzneimittelreaktionen vom Spättyp 5. Tabelle 5 gibt anhand beispielhaft ausgewählter Arzneimittel einen Überblick über die Komplexität der Assoziation von schweren Hypersensitivitätsreaktionen und HLA-Allelen.
Tabelle 5. Assoziation von schweren Hypersensitivitätsreaktionen mit HLA-Allelen
| Auslösendes Arzneimittel | Hypersensitivitäts-Reaktionen | HLA-Allele | Ethnizität |
|---|---|---|---|
| Abacavir | Abacavir-Hypersensitivitäts -Syndrom | HLA-B*57:01 | Europäisch-stämmige, Afro-Amerikaner, Hispanier |
| Allopurinol | SCAR |
|
Europäisch-stämmige und Han-Chinesen |
| HLA-B*58:01 | Japaner, Thailänder | ||
| Amoxicillin-Clavulansäure | DILI |
|
Europäisch-stämmige |
| Carbamazepin |
|
|
Europäisch-stämmige |
|
|
Han-Chinesen | |
| SJS/TEN | HLA-B*15:02 | Inder | |
|
|
Japaner | |
|
|
Koreaner | |
| SJS/TEN | HLA-B*15:02 | Malaien, Thailänder, Vietnamesen | |
| SJS/TEN, DRESS | HLA-B*46:01 | Vietnamesen | |
| Sulfamethoxazol | SJS/TEN | HLA-B*38:01/:02/:11 | Europäisch-stämmige |
| SJS/TEN |
|
Thailänder |
- Abk.: SCAR, Severe cutaneous adverse reactions (AGEP, DRESS und SJS/TEN); DILI, Drug-induced liver injury/Arzneimittelinduzierte Leberschäden; SJS/TEN, Stevens-Johnson-Syndrom/Toxische epidermale Nekrolyse; DRESS, Drug reaction with eosinophilia and systemic symptoms; MPE, makulopapulöses Exanthem.
Tabelle 6. Alarmzeichen für schwere Arzneimittelreaktionen
| Allgemeinsymptome* |
|---|
|
| Hautveränderungen |
|
| Veränderungen von Laborparametern |
|
- *Cave: Allgemeinsymptome können durch Grunderkrankungen bedingt sein, derentwegen der Patient behandelt wird.
Aber auch eine Enzym-Mutation kann Ursache für medikamenteninduzierte Hypersensitivitätsreaktionen sein. So geht die durch Missense-Mutation des Cytochrom P450 Gens bedingte Variante CYP2C9*3 mit einer deutlich verminderten Metabolisierungskapazität für Phenytoin und dadurch mit einer signifikant erhöhten Rate schwerer kutaner Nebenwirkungen einher 6.
Infekte generell, aber insbesondere virale Infektionen induzieren eine Aktivierung des Immunsystems und dadurch eine gesteigerte Bereitschaft zur Entwicklung von Arzneimittelreaktionen. Bekanntestes Beispiel hierfür ist die als nahezu obligat geltende Entwicklung eines makulopapulösen Exanthems bei Einnahme eines Aminopenicillins bei akuter Epstein-Barr-Virus-Infektion (infektiöse Mononukleose) oder das gehäufte Auftreten von Exanthemen bei einer nicht therapierten HIV-Infektion.
Alarmzeichen für schwere Arzneimittelreaktionen
Schwere Arzneimittelreaktionen wie das DRESS-Syndrom (Drug Reaction with Eosinophilia and Systemic Symptoms) und die toxische epidermale Nekrolyse (TEN) sind lebensbedrohliche Erkrankungen (Tabelle 2) und müssen frühestmöglich erkannt und adäquat – in der Regel intensivmedizinisch – behandelt werden. Oftmals kündigen sie sich bereits in der Initialphase durch charakteristische Symptome an, die als Alarmzeichen gelten (Tabelle 6).
Diagnostik
Eine allergologische Abklärung sollte bei begründetem Verdacht erfolgen, da eine erneute Exposition gegenüber dem auslösenden Arzneimittel – insbesondere nach einer vorausgegangenen schweren Reaktion – fatale Folgen für den Patienten haben kann, während die unnötige Meidung eines Medikamentes oder einer Arzneimittelgruppe, wie zum Beispiel die Penicilline, eine Einschränkung der Therapieoptionen bedeutet. Darüber hinaus ist die Verwendung von Ausweichmedikamenten oft mit deutlich höheren Kosten verbunden.
Optimalerweise wird die Abklärung binnen sechs Monaten nach dem Ereignis, aber frühestens sechs Wochen nach vollständiger Abheilung der Hautläsionen durchgeführt. Generell gilt, dass kurz vor dem erstmaligen Auftreten der Hautveränderungen applizierte Medikamente wahrscheinlicher Ursache der unerwünschten Arzneimittelwirkung (UAW) sind als Arzneimittel, die schon länger angewandt wurden. Aber auch ein über viele Jahre appliziertes und bislang problemlos vertragenes Medikament kann, insbesondere wenn die Einnahme zeitweise unterbrochen wurde, Auslöser einer UAW sein.
Bei der Anamneseerhebung – gegebenenfalls unter Zuhilfenahme von Validierungs-Scores für das DRESS-Syndrom und die akute generalisierte exanthematische Pustulose (AGEP) 3 – und einer Skizzierung des zeitlichen Ablaufs der Applikation der potenziell verantwortlichen Medikamente mittels eines Zeitstrahldiagramms (Abbildung 2), sollten auch ärztliche Berichte, Verlaufsdokumentationen, Narkoseprotokolle und evtl. vom Patienten selbst angefertigte Fotos berücksichtigt werden.
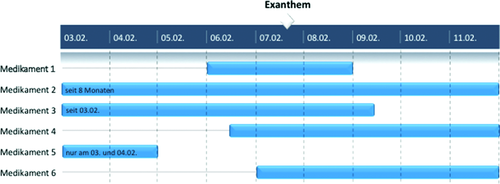
Klinische Untersuchung
Eine gründliche dermatologische Untersuchung unter Einschluss der hautnahen Schleimhäute und der Adnexstrukturen (Haare und Nägel) ist bei allen vermuteten arzneimittelinduzierten Erkrankungen unverzichtbar. Hierbei müssen neben der Morphe der Läsionen auch deren Größe und Form, Lokalisation (stamm-, beugen- oder akralbetont, lichtexponierte Körperregionen) und das Verteilungsmuster (symmetrisch, beugenbetont) erfasst werden.
Zur Differenzierung zwischen einer Soforttyp- und einer Spättypreaktion sind zeitlicher Verlauf und Morphe der Hautveränderungen von entscheidender Bedeutung, da diese das diagnostische Vorgehen bestimmen. An der Haut gehen Soforttypreaktionen oft mit Urticae und Angioödemen einher, während Spättypreaktionen überwiegend in Form makulöser/makulopapulöser Hautveränderungen manifest werden. Sind bei Vorstellung des Patienten keine Hautläsionen mehr vorhanden, so sollte bei der Anamneseerhebung erfragt werden, ob die Hautveränderungen solchen glichen, wie sie bei Kontakt mit Brennnesseln oder nach Mückenstichen auftreten, da diese typischerweise urtikariell und flüchtig und damit Ausdruck einer Soforttypreaktion sind. Eine Abheilung der Läsionen mit Schuppung weist hingegen auf eine Spättypreaktion hin.
In-vivo- und In-vitro-Testverfahren
Zum Nachweis einer Spättypreaktion werden Intrakutan- bzw. Scratch- und Epikutantests sowie gegebenenfalls Provokationstestungen mit den verdächtigten Arzneimitteln und/oder Ausweichpräparaten durchgeführt. Hauttestungen sollten mit den von der ENDA/EAACI Drug Allergy Interest Group empfohlenen Konzentrationen erfolgen, da diese standardisiert sind 7. Die Erfolgsaussichten für richtigpositive Ergebnisse sind abhängig vom getesteten Arzneimittel und dessen Konzentration, der Manifestationsform der Hypersensitivitätsreaktion sowie der Zeit, die seit dem Auftreten der Reaktion vergangenen ist. Intrakutan- bzw. Scratch-Testungen dürfen bei vorausgegangenen schweren Hypersensitivitätsreaktionen nur in Ausnahmefällen durchgeführt werden, da selbst Applikationen geringer Konzentrationen des verantwortlichen Agens ein Rezidiv auslösen können 3, 8. Bei fixen Arzneimittelreaktionen sollte eine Hauttestung, falls möglich, zusätzlich auch in loco, also dort, wo die Hautveränderung aufgetreten ist, erfolgen.
Als In-vitro-Testverfahren für die Abklärung von Spättypreaktionen stehen aktuell der Lymphozytenproliferationstest (LTT), der Enzyme-Linked Immunosorbent Spot (ELISpot) Assay sowie der Enzyme-Linked Immunosorbent Assay (ELISA) zur Verfügung, mit denen antigenspezifische T-Lymphozyten bzw. die von ihnen nach Stimulation produzierten Zytokine nachgewiesen werden können 9, 10. Wegen des relativ hohen technischen Aufwands und der damit verbundenen Fehleranfälligkeit werden die Tests aber nur von spezialisierten Labors durchgeführt und sind bis heute überwiegend wissenschaftlichen Fragestellungen vorbehalten. Zudem sind Sensitivität und Spezifität der Tests stark von den untersuchten Arzneimitteln abhängig 11.
Eine Bestimmung spezifischer IgE-Antikörper macht keinen Sinn, da diese nur bei Soforttypallergien von Bedeutung sind.
Provokationstestung
Ist eine Identifikation des für die Reaktion verantwortlichen Arzneimittels durch Anamnese, Hauttestungen und/oder In-vitro-Testverfahren nicht möglich, kann eine Provokationstestung indiziert sein. Hierbei sollten die verdächtigten Medikamente möglichst in der Form (oral, subkutan, intravenös, inhalativ) appliziert werden, in der sie die (vermutete) Hyperreaktivität induziert haben. Ist dies nicht möglich, kann bei Verfügbarkeit entsprechender Zubereitungsformen alternativ auch eine orale Provokationstestung durchgeführt werden. Stets sollte eine individuelle Nutzen-Risiko-Abwägung erfolgen und beachtet werden, dass potenziell durch das Arzneimittel ausgelöste schwere Hypersensitivitätsreaktionen (Tabelle 2), Schwangerschaft (bei einigen Arzneimitteln auch Stillzeit), mangelnde Compliance und unzureichendes Verständnis des Patienten für das Testverfahren Kontraindikationen darstellen 12. Im Gegensatz zu Soforttypreaktionen ist für die Auslösung von Spättypreaktionen oftmals die tatsächliche Tagesdosis notwendig. Es hat sich deshalb bewährt, den Patienten bei zuvor unkomplizierten Reaktionen (Tabelle 1) die erste Dosis nach vorausgegangener Kontrolle des Hautzustandes unter ärztlicher Kontrolle einnehmen zu lassen und ihm eine weitere bzw. weitere Dosen für die Einnahme zu einem späteren Zeitpunkt (beispielweise acht Stunden nach Einnahme der Erstdosis) mitzugeben.
Während Ausweichtestungen mit Medikamenten, die alternativ zu dem für die Reaktion verantwortlichen Arzneimittel eingesetzt werden sollen, sinnvoll sind, werden allergologische Testungen, die diesen Zweck nicht erfüllen und für die kein entsprechender anamnestischer Anhalt für eine mögliche Unverträglichkeit besteht (prophetische Testungen), ausdrücklich nicht empfohlen.
Routine-Laboruntersuchungen (Differenzialblutbild, Leber- und Nierenparameter) sollten im akuten Stadium durchgeführt werden, um eventuelle systemische Beteiligungen zu erfassen. Eosinophilie, Neutrophilie, Zytopenie und/oder pathologische Leber- und Nierenwerte weisen auf eine systemische Beteiligung im Rahmen einer schweren Arzneimittelreaktion hin und erfordern ein sofortiges Absetzen der in Frage kommenden Medikamente. Besteht Unklarheit darüber, ob es sich bei den Hautveränderungen tatsächlich um eine Arzneimittelreaktion handelt, hilft oftmals die histologische Untersuchung eines aus der Läsion entnommenen Biopsats weiter.
Für alle diagnostischen Maßnahmen gilt, dass weder negative Haut- und In-vitro-Tests noch negative Resultate der Expositionstestungen eine Arzneimittelallergie bzw. -intoleranz sicher ausschließen.
Nachgewiesene Arzneimittelallergien und Unverträglichkeitsreaktionen müssen ebenso wie mögliche Kreuzreaktivitäten und Ausweichpräparate in einem Allergie-Pass eingetragen werden, der dem Patienten ausgehändigt wird. Besteht lediglich ein begründeter Verdacht auf eine solche Reaktion, so sollte dies entsprechend vermerkt werden. Es empfiehlt sich, eine Kopie des Ausweises in der Krankengeschichte des Patienten abzulegen, um im Falle eines Verlustes des Allergie-Passes Zugriff auf die Eintragungen zu haben.
Differenzialdiagnosen
Vor allem bei Kindern sollte bei Auftreten eines makulösen oder papulovesikulösen Exanthems differenzialdiagnostisch stets zunächst an einen viralen Infekt gedacht werden. Weitere wichtige Differenzialdiagnosen sind in Tabelle 7 aufgeführt.
Tabelle 7. Wichtige Differenzialdiagnosen des makulösen/makulopapulösen Arzneiexanthems
|
Therapie
Symptomatische Therapie
Die primäre Therapie besteht im Absetzen des verdächtigten Arzneimittels. Kommen mehrere Medikamente in Frage, so sollte zunächst das am wahrscheinlichsten ursächliche Arzneimittel gemieden werden. Nach dem Absetzen bleibt eine Besserung oft zunächst aus oder es kommt gar zu einer vorübergehenden Verschlechterung des Krankheitsbildes. Je nach Schwere der Reaktion und Halbwertszeit des Medikamentes kann ein vollständiger Rückgang der Symptomatik mehrere Wochen dauern.
Zur symptomatischen Therapie leicht- bis mittelgradig ausgeprägter Arzneimittelreaktionen haben sich topische Glukokortikoide bewährt. Reichen diese nicht aus, kann eine ergänzende Therapie mit systemisch wirksamen Kortikosteroiden in einer Dosierung von 0,5 bis 1,0 mg/kg Körpergewicht (KG)/d angezeigt sein. Zur Behandlung des Juckreizes helfen auch bei T-Zell-vermittelten Reaktionen oftmals Antihistaminika, da auch Mastzellen an der Entwicklung von Typ-IV-Reaktionen beteiligt sind.
Schwere Hypersensitivitätsreaktionen hingegen bedürfen in der Regel einer intensivmedizinischen Therapie, bei blasenbildenden Arzneimittelreaktionen wie Stevens-Johnson-Syndrom/toxische epidermale Nekrolyse (SJS/TEN) mit großflächigen Hautablösungen optimalerweise in einem Zentrum für Schwerstbrandverletzte. Neben topischen Behandlungen von Haut- und Schleimhauterosionen – eine eventuelle okuläre Beteiligung muss frühestmöglich erkannt und adäquat durch einen Augenarzt behandelt werden – erfolgt die Therapie supportiv und mittels immunsuppressiver/-modulatorischer Medikamente.
Während neuere Daten eine gute Wirksamkeit von Ciclosporin A bei der Behandlung von SJS/TEN belegen, haben Studien mit intravenös verabreichten Immunglobulinen (IVIG) kein eindeutiges Ergebnis hinsichtlich der Reduktion der Mortalität erbracht 13-15. Werden IVIG eingesetzt, so scheint eine Dosierung von mindestens 2 g/kg KG niedrigeren Dosen überlegen zu sein 16. Eine Kombination mit systemisch applizierten Glukokortikoiden ist gemäß einigen Studien vorteilhaft, andere haben diesen Ansatz nicht bestätigen können 16, 17.
Während bei der AGEP eine symptomatische Therapie mit Antipyretika, Antihistaminika und evtl. topischen Glukokortikosteroiden der Klasse III oder IV aufgrund des in der Regel komplikationslosen Verlaufs meist ausreichend ist, erfordert die Behandlung eines DRESS-Syndroms (drug reaction with eosinophilia and systemic symptoms) mit Beteiligung innerer Organe neben diesen Maßnahmen eine systemische Immunsuppression. Hierfür werden Kortikosteroide in einer Dosierung von 0,5 bis 2,0 mg/kg KG Prednisonäquivalent eingesetzt. Detaillierte Darstellungen zur Therapie schwerer Arzneimittelreaktionen finden sich in den Publikationen von Paulmann et al. 3 sowie Schwartz et al. 18.
Durchbehandeln
Besteht lediglich ein leichtgradig ausgeprägtes makulopapulöses Exanthem, dessen Ursache ein nur vorübergehend eingesetztes Arzneimittel ist, kann eine Fortführung der Therapie bei fehlenden Alternativen unter engmaschigen klinischen und Laborkontrollen (Differenzialblutbild, Chemogramm) erwogen werden. Gelegentlich tritt hierunter eine Toleranz ein, anderenfalls kann eine begleitende Therapie mit einem systemisch applizierten Glukokortikoid und gegebenenfalls einem Antihistaminikum durchgeführt werden.
Toleranzinduktion
Ist ein Arzneimittel für die Behandlung einer Erkrankung unverzichtbar, kann eine Toleranzinduktion mittels schrittweiser Dosissteigerung versucht werden 19. Hierbei sollte auf etablierte Protokolle zurückgegriffen werden, mit denen mindestens zehn Patienten erfolgreich behandelt wurden. Protokolle mit langsamen Dosissteigerungen scheinen solchen mit raschen überlegen zu sein.
Behandelt werden sollten ausschließlich Patienten mit unkomplizierten Spättypreaktionen, wie etwa makulopapulösen oder fixen Arzneimittelexanthemen, für die Therapie schwerer Reaktionen ist ein solches Vorgehen kontraindiziert. Je nach Arzneimittel dauert die Behandlung zwischen wenigen Stunden und einigen Wochen. Während des gesamten Prozedere ist eine engmaschige Überwachung notwendig, um eventuell auftretende schwere Arzneimittelreaktionen rechtzeitig zu erfassen. Der Patient muss darüber informiert werden, dass eine Toleranz nur so lange bestehen bleibt, wie das Medikament regelmäßig appliziert wird. Im Vergleich zu Toleranzinduktionen bei Soforttypreaktionen sind die Erfolgsaussichten bei Hypersensitivitätsreaktionen vom Spättyp allerdings deutlich geringer 19.
Prophylaxe
Bei Patienten, bei denen aufgrund der Vorgeschichte eine leicht- bis mittelgradige allergische oder pseudoallergische Reaktion wahrscheinlich ist und für die kein alternatives Arzneimittel zur Verfügung steht, kann vor Gabe des entsprechenden Medikamentes eine prophylaktische Therapie mit einem Glukokortikoid (z. B. 50 mg Prednisolon p.o. täglich) für ein- bis fünf Tage versucht werden; Durchbrüche wurden allerdings beschrieben. Gemäß eines Fallberichts kann bei vorausgegangener Reaktion auf Röntgenkontrastmitteln, die teilweise sehr langsam eliminiert werden, eine solche Behandlung versuchsweise auch nach Applikation des potenziell reaktionsauslösenden Wirkstoffs für weitere zwei- bis fünf Tage fortgeführt werden 20.
Auslöser kutaner Arzneimittelreaktionen vom Spättyp
Bis auf wenige Ausnahmen können nahezu alle Arzneimittel Unverträglichkeitsreaktionen vom Spättyp hervorrufen, wobei das entsprechende Potenzial hierfür deutlich variiert. Nachfolgend sind die am häufigsten verantwortlichen sowie die oft zu Unrecht verdächtigten Medikamente aufgeführt. Arzneimittel, die nur sehr selten Spättypreaktionen induzieren, sind in Tabelle 8 zusammengefasst.
Tabelle 8. Arzneimittel, die sehr selten Auslöser von Spättypreaktionen sind
|
Betalactam-Antibiotika (Penicillin, Aminopenicilline, Cephalosporine, Carbapeneme, Monobactame)
Die Prävalenz der durch Betalactam- bzw. Antibiotika generell induzierten Spättyp-Reaktionen liegt deutlich über den von dieser Medikamentengruppe hervorgerufenen Soforttypreaktionen. Hierfür sind vor allem Aminopenicilline verantwortlich, deren Aminobenzyl-Seitenkette in den meisten Fällen die allergene Determinante darstellt. Während parenterale Applikationen von Beta-Lactam-Antibiotika eher Soforttyp-Allergien hervorrufen, soll eine orale Verabreichung signifikant häufiger eine Allergie vom Spättyp induzieren. Makulöse/makulopapulöse Läsionen sind die häufigsten Hautveränderungen, Kreuzreaktionen mit Cephalosporinen kommen weit seltener vor, als allgemein vermutet. So werden bei einer Spättyp-, wie auch bei einer Soforttyp-Allergie gegenüber Aminopenicillinen, die für die orale Applikation zur Verfügung stehenden Cephalosporine Cefadroxil, Cefuroxim, Cefixim und Cefpodoxim in der Regel problemlos vertragen, da diese keine Aminobenzyl-Seitenketten besitzen 21. Aztreonam kann mit Ceftazidim kreuzreagieren, da beide Beta-Lactam Antibiotika eine Aminothiazol-Gruppe besitzen; Kreuzreaktivitäten zwischen Aztreonam und anderen Beta-Lactam Antibiotika existieren nicht 22. Ebenfalls ein sehr geringes Risiko für Kreuzreaktionen mit anderen Betalactam-Antibiotika weisen Carbapeneme auf.
Cotrimoxazol
Auch bei diesem Antibiotikum treten Spättyp- sehr viel öfter als Soforttypreaktionen auf und reichen von milden makulopapulösen Exanthemen über generalisierte bullöse fixe Arzneimittelexantheme bis hin zu lebensbedrohlichen Reaktionen wie dem SJS/TEN. Cotrimoxazol gehört zu den häufigen Auslösern kutaner, aber auch schwerer systemischer Arzneimittelreaktionen. Mit dem HI-Virus infizierte Personen, die mit Cotrimoxazol prophylaktisch oder wegen einer manifesten Infektion behandelt werden, haben ein besonders hohes Risiko Hypersensitivitätsreaktionen zu entwickeln. Kreuzreaktivitäten zwischen den aromatischen Sulfonamid-Antibiotika und anderen Sulfonamid-haltigen Arzneimitteln existieren entgegen weitläufiger Meinung praktisch nicht 23.
Fluorchinolone/Gyrasehemmer (Ciprofloxacin, Gemifloxacin, Levofloxacin, Moxifloxacin, Norfloxacin)
Sie lösen überwiegend Soforttyp- und selten Spättypreaktionen aus. Aufgrund ihres zunehmenden Einsatzes werden Hypersensitivitätsreaktionen während der letzten Jahre häufiger beobachtet. Sowohl makulopapulöse und fixe Arzneimittelexantheme als auch photoallergische/phototoxische und schwere Hypersensitivitätsreaktionen wie die AGEP und das SJS/TEN sind für diese Substanzgruppe beschrieben 24. Das im deutschsprachigen Raum bisher nicht zugelassene und zur fünften Generation zählende Gemifloxacin ist unter den Fluorchinolonen der häufigste Auslöser makulopapulöser Hautveränderungen 25, Ciprofloxacin steht an zweiter Stelle. Kreuzreaktionen innerhalb dieser Medikamentengruppe kommen vor, weshalb nach schweren Haut- und systemischen Reaktionen auf die Gabe von weiteren Fluorchinolonen verzichtet werden sollte.
Makrolide (Azithromycin, Clarithromycin, Erythromycin, Roxithromycin)
Makrolide gelten hinsichtlich Hypersensitivitätsreaktionen als relativ sichere Arzneimittel, zu Spättypreaktionen kommt es unter Therapie mit diesen Medikamenten sehr selten.
Tetrazykline
Antibiotika dieser Gruppe wirken photosensibilisierend und sind daher vor allem als Ursache phototoxischer Reaktionen bekannt. Darüber hinaus ist das Auftreten von SJS/TEN, systemischer Hypersensitivitätsreaktionen und fixer Arzneimittelexantheme beschrieben.
Minocyclin ruft etwa fünfmal häufiger UAW hervor als Doxycyclin und dies, obwohl letzteres sehr viel häufiger verordnet wird. Zudem sind die durch Minocyclin induzierten UAW meist deutlich schwerer ausgeprägt.
Clindamycin
Durch Clindamycin ausgelöste Hautveränderungen manifestieren sich überwiegend in Form makulöser/makulopapulöser Exantheme, schwere Arzneimittelreaktionen sind selten.
Vancomycin
Vancomycin ist eine relativ häufige Ursache für Hypersensitivitätsreaktionen vom Spättyp, die oftmals mit exanthematischen Hautveränderungen und peripherer Eosinophilie einhergehen. Neben makulopapulösen Exanthemen und dem DRESS-Syndrom sind unter anderem Erythema-exsudativum-multiforme (EEM)-artige Hautveränderungen und SJS/TEN als verzögert auftretende Reaktionen in Einzelfallberichten beschrieben. Da aber bekannt ist, dass das Medikament auch lineare IgA-Dermatosen induzieren kann, die sich gelegentlich unter dem Bild eines SJS/TEN manifestieren, ist unklar, ob es sich bei den beschriebenen SJS/TEN tatsächlich um diese Krankheitsbilder gehandelt hat.
Häufig tritt bei zu schneller Infusion des Medikamentes ein makulöses Erythem (Flush) im Kopf-/Halsbereich sowie den oberen Thoraxabschnitten auf, das als red person's syndrome (früher red man's syndrome) bezeichnet wird und nichtallergischer Genese ist. Die Flush-artigen Hautveränderungen sind ungefährlich und bilden sich binnen Stunden spontan zurück.
Analgetika
Nichtsteroidale Antirheumatika (NSAR) sind nach den Antibiotika die häufigste Ursache für urtikarielle Reaktionen im Rahmen einer Analgetika-Pseudoallergie, zellvermittelte exanthematische Spättypreaktionen hingegen sind selten. Oxicame (Piroxicam, Meloxicam) stehen als Ursache an erster Stelle, Phenylbutazon und dessen Metabolit Oxyphenbutazon sowie der Cyclooxygenase-2-Inhibitor Celecoxib gelten als sehr seltene Auslöser derartiger Komplikationen. Kreuzreaktionen zwischen NSAR im Rahmen einer T-Zell-vermittelten Allergie sind eine Rarität. Relativ häufig hingegen sind NSAR – insbesondere Metamizol und das ansonsten eher selten Hypersensitivitätsreaktionen induzierende Paracetamol – Ursache fixer Arzneimittelexantheme.
Röntgenkontrastmittel
Auch Spätreaktionen auf Röntgenkontrastmittel manifestieren sich überwiegend in Form mild oder moderat ausgeprägter makulöser oder makulopapulöser Exantheme, die wenige Stunden bis zu sieben Tagen nach Exposition auftreten und etwa 1–3 % der exponierten Patienten betreffen. Die Hautveränderungen sind meist selbstlimitierend und heilen in der Regel binnen drei bis sieben Tagen spontan ab.
Aufgrund der teilweise sehr langen Halbwertszeiten und der sehr langsamen Elimination der Substanzen – Röntgenkontrastmittel können gelegentlich noch mehr als eine Woche nach Applikation radiologisch nachgewiesen werden – sind Sensibilisierung und Entwicklung einer Spättypreaktion auch nach Erst- und einmaliger Applikation möglich.
Kreuzreaktivitäten zwischen Kontrastmitteln ähnlicher Struktur sind häufig und Sensibilisierungen gegenüber diesen scheinen in etwa einem Drittel der Fälle durch andere chemische Entitäten zu erfolgen. Nicht-ionische rufen häufiger als ionische und dimere häufiger als monomere Kontrastmittel Hypersensitivitätsreaktionen hervor; somit besteht bei Verwendung ionischer, monomerer Kontrastmittel das geringste Risiko für eine Hypersensitivitätsreaktion. Auslöser der Reaktionen ist nahezu immer das gesamte Kontrastmittelmolekül und nicht, wie oft fälschlich postuliert, das daran gebundene Iod 26.
Lokalanästhetika
Lokalanästhetika (LA) werden anhand ihrer Intermediärkette in solche vom Amid- und solche vom Estertyp unterteilt. Aufgrund der strukturellen Diversitäten der Moleküle und deren unterschiedlicher Abbauwege sind Kreuzreaktionen zwischen den beiden Typen eine Rarität, Kreuzreaktivitäten innerhalb der beiden Gruppen aber häufig. Insgesamt sind Spättypreaktionen eher selten und treten in Abhängigkeit der Applikationsart als lokalisierte Kontaktallergien oder auch in Form disseminierter Typ-IV-Reaktionen auf. Amid-LA lösen seltener Allergien aus als solche vom Estertyp und sollten deshalb bevorzugt werden (Tabelle 9).
Tabelle 9. Lokalanästhetika vom Amonioamid (Amino)- und Aminoester (Ester)-Typ
| Aminoamide* | Aminoester |
|---|---|
|
|
- Gedankenstütze: Die Namen der Aminoamid-Lokalanästhetika schreiben sich mit zwei „i“.
Neben dem Lokalanästhetikum selbst sind auch die darin enthaltenen Konservierungsstoffe, vor allem die Parabene Methyl- und Propylparahydroxybenzoat (E218/E216), wie auch das in Adrenalin-haltigen Lokalanästhetika als Antioxidans eingesetzte Natriumdisulfit (E223) von allergologischer Relevanz.
Urikostatika und Urikosurika
Allopurinol ist in Europa und Israel die häufigste Ursache arzneimittelinduzierter SJS/TEN, Patienten mit dem HLA-B*5801-Allel sind besonders gefährdet 27. Schwere Hypersensitivitätsreaktionen treten in mehr als 90 % der durch Allopurinol ausgelösten Fälle innerhalb von acht bis neun Wochen nach Therapiebeginn auf, wobei auch bei diesem Medikament Spättypreaktionen in Form harmloser makulopapulöser Hautveränderungen deutlich überwiegen. Ebenfalls schwere Hypersensitivitätsreaktionen sind für Febuxostat beschrieben, besser verträglich zu sein scheinen die Urikosurika Benzbromaron und Probenecid.
Psycho- und neurotrope Arzneimittel
Die aromatischen Antiepileptika Carbamazepin, Phenytoin, Phenobarbital und Lamotrigin sind unter den Antikonvulsiva die häufigsten Auslöser allergischer Hypersensitivitätsreaktionen vom Spättyp. Carboxamide (z. B. Carbamazepin), Hydantoine (z. B. Phenytoin), Barbiturate (z. B. Phenobarbital) und Lamotrigin weisen Kreuzreaktivitäten auf, die nicht auf Strukturähnlichkeiten beruhen. Die chemische Struktur trizyklischer Antidepressiva hingegen ähnelt derjenigen der Carboxamide, weshalb auch Kreuzreaktionen zwischen diesen Wirkstoffgruppen nicht auszuschließen sind.
Antiretrovirale Arzneimittel/Virustatika
Unter einer antiretroviralen Therapie treten häufig auch kutane Reaktionen vom Spättyp auf. Ursache hierfür ist vermutlich die durch die HIV-Infektion bedingte Dysregulation des Immunsystems sowie eine veränderte Arzneimittelmetabolisierung, unter anderem auch im Rahmen einer häufig bestehenden Polypharmakotherapie. In der überwiegenden Zahl der Fälle treten Hautveränderungen während der ersten sechs Wochen nach Therapiebeginn auf und manifestieren sich meist in Form leicht- bis mittelgradig ausgeprägter makulopapulöser Exantheme.
Für Patienten, bei denen in der Vergangenheit unter Behandlung mit Sulfonamid-Antibiotika ein Exanthem aufgetreten ist, besteht ein deutlich erhöhtes Risiko für die Entwicklung einer allergischen Reaktion vom Spättyp bei Einnahme des Nicht-nukleosidischen-Reverse-Transkriptase-Inhibitors (NNRTI) Nevirapin. Der NNRTI Abacavir ist der häufigste Auslöser eines DRESS-Syndroms bei HIV-positiven Patienten. Eine Assoziation mit dem HLA-Typus sowie Kreuzreaktivitäten zwischen NNRTI sind bekannt.
Die zur Behandlung von Infektionen mit Herpesviren eingesetzten Virustatika Aciclovir, Valaciclovir, Ganciclovir und Famciclovir rufen nur sehr selten Spättypreaktionen hervor.
Antimykotika
Terbinafin löst relativ häufig Spättypreaktionen aus, die von leicht ausgeprägten makulösen Exanthemen bis hin zu den seltener auftretenden schweren Haut- und systemischen Reaktionen wie der AGEP reichen. Für das Imidazol-Antimykotikum Fluconazol ist die Auslösung fixer Arzneiexantheme mehrfach beschrieben.
Tuberkulostatika
Größere Studien, die die Inzidenz von Spättypreaktionen im Rahmen einer tuberkulostatischen Therapie untersucht haben, existieren nicht. Hypersensitivitätsreaktionen manifestieren sich überwiegend während der ersten beiden Monate nach Behandlungsbeginn in Form leicht ausgeprägter makulopapulöser Exantheme. Pyrazinamid gilt als dessen häufigster Auslöser, die Entwicklung eines DRESS-Syndroms soll besonders eng mit Rifampicin assoziiert sein.
Antikoagulanzien und Thrombozytenaggregationshemmer
Bis zu 7,5 % der mit niedermolekularen Heparinen therapierten stationären Patienten und etwa 20 % der mit dieser Arzneimittelgruppe behandelten Schwangeren entwickeln eine allergische Hypersensitivitätsreaktion vom Spättyp. Weibliches Geschlecht, eine bestehende Schwangerschaft, ein Body-Mass-Index über 25 sowie eine Behandlung mit einem niedermolekularen Heparin-Präparat über mehr als neun Tage gelten als Risikofaktoren 28. Kreuzreaktivitäten sind sehr häufig. Der synthetische Faktor-Xa-Inhibitor Fondaparinux hingegen weist ein niedriges Risiko für Kreuzreaktivitäten auf und besitzt zudem nur ein geringes Sensibilisierungspotenzial. Alternativ können auch nicht-fraktionierte Heparine eingesetzt werden. Nadroparin löst häufiger als jedes andere niedermolekulare Heparin bei Schwangeren Hypersensitivitätsreaktionen aus und sollte deshalb bei dieser Patientinnengruppe nicht verwendet werden 28.
Spättypreaktionen auf Heparine manifestieren sich initial meist am Ort der Applikation und sind bei einer Generalisation der Hautveränderungen dort in der Regel am stärksten ausgeprägt. Generalisierte Exantheme ohne deutliche Betonung an den Applikationsarealen schließen eine Allergie auf Heparine weitgehend aus.
Allergische Reaktionen auf Clopidogrel treten meist 5–7 Tage nach Therapiebeginn in Form generalisierter makulöser/makulopapulöser, seltener auch lokalisierter Exantheme in Erscheinung. Kreuzreaktivitäten mit den Thrombozytenaggregationshemmern Ticlopidin und Prasugrel scheinen häufig zu sein. Eine erfolgreiche Desensibilisierung soll durch eine dreiwöchige Behandlung mit Prednison in absteigender Dosierung unter gleichzeitiger Fortführung der Clopidogrel-Therapie in nahezu 100 % der Fälle möglich sein 29.
Insuline und orale Antidiabetika
Insulinallergien sind selten und treten überwiegend als Typ-I-Reaktionen auf. Spättypreaktionen auf das Insulinmolekül selbst sind in der Literatur nur vereinzelt beschrieben. Insulinpräparate enthalten aber neben dem eigentlichen Wirkstoff auch Konservierungsstoffe, vor allem Phenol und Metacresol. Misch- und langwirksame Insuline sind zudem mit Verzögerungszusätzen wie Protaminsulfat und Zink versehen. Da vor allem diese Stoffe Ursache allergischer Spättypreaktionen sein können, müssen neben den Insulinen selbst stets auch deren Zusatzstoffe gesondert mitgetestet werden.
Orale Antidiabetika lösen nur sehr selten Spättypreaktionen aus.
Antihypertonika, Antiarrhythmika und Diuretika
Antihypertonika und Antiarrhythmika sind seltene Ursachen von Spättypreaktionen. Der Calciumantagonist Diltiazem gehört zu den häufigen Auslösern der AGEP (Tabelle 2), unter einer Therapie mit Betablockern kommt es gelegentlich zur Erstmanifestation einer latenten oder auch zu einer Verschlechterung einer manifesten Psoriasis vulgaris, die differenzialdiagnostisch von einer psoriasiformen Arzneimittelreaktion abgegrenzt werden muss.
Sehr selten induzieren ACE-Inhibitoren und Sartane Hautveränderungen, und wenn, dann überwiegend in Form makulopapulöser Exantheme.
Diuretika sind von geringer allergologischer Relevanz. Schleifen- und Thiaziddiuretika besitzen jedoch photosensibilisierende Eigenschaften und sind daher als Ursache phototoxischer Reaktionen bekannt.
Biologika und Zytokine
Durch den zunehmenden Einsatz und die kontinuierliche Ausweitung des Indikationsspektrums der Biologika nimmt auch die Inzidenz der unerwünschten Nebenwirkungen zu; die Zahl der durch sie hervorgerufenen ausgeprägten Spättypreaktionen ist allerdings gering 30. Hypersensitivitätsreaktionen wie kutane Vaskulitiden, Arzneimittel-induzierter Lupus erythematodes, Vitiligo, psoriasiforme Hautveränderungen, makulöse Ekzeme sowie EEM-artige Hypersensitivitätsreaktionen und SJS/TEN sind beschrieben. Sehr viel häufiger treten Lokalreaktionen, zum Beispiel nach Gabe von Anakinra, Ustekinumab, Adalimumab und Etanercept, jedoch am Applikationsort auf.
Unter den Zytokinen ist Interferon-α eine relativ häufige Ursache für die Entwicklung ekzematöser Hautveränderungen am Injektionsort, bei pegylierten Interferonen wird das mit dem Zytokin konjugierte Polyethylenglykol (Macrogol) als verantwortliches Allergen vermutet 31. Eine Fortführung der Therapie ist häufig mit nicht-pegyliertem Interferon möglich 32.
Weitere Auslöser von Spättypreaktionen
Auch Statine, Protonenpumpeninhibitoren, Glukokortikoide und das Muskelrelaxans Tolperison können, wenn auch sehr selten, Spättypreaktionen in Form von Exanthemen hervorrufen. Additiva wie Konservierungsmittel, Antioxidantien (z. B. Natriumdisulfit), Stabilisatoren, Verdickungsmittel, Permeabilitätsverstärker, Farbstoffe (v. a. Tartrazin bzw. E102) etc. sind Bestandteile vieler Medikamente sowie auch Nahrungsmittel und gelegentlich Ursache für makulöse/makulopapulöse Hautveränderungen.
Zusammenfassung
Bei der überwiegenden Mehrzahl der durch Arzneimittel induzierten Spättypreaktionen handelt es sich um relativ milde verlaufende Dermatosen – meist makulopapulöse Exantheme – die nach Absetzen des auslösenden Medikamentes binnen weniger Tage komplikationslos abheilen. Schwere Arzneimittelreaktionen hingegen gehen oft mit systemischen Beteiligungen einher und können einen letalen Verlauf nehmen, weshalb eine möglichst rasche Identifikation und Absetzen des Medikamentes erforderlich sind. Kommen mehrere Arzneimittel als Ursache in Frage, so kann meist schon durch eine detaillierte Anamneseerhebung, gegebenenfalls unter Berücksichtigung von Arztberichten oder Narkoseprotokollen, eine Eingrenzung vorgenommen werden. Voraussetzung hierfür ist das Wissen über die allergologische Relevanz von Medikamentengruppen bzw. einzelner Arzneimittel.
Interessenkonflikt
Keiner.
Literatur
Fragen zur Zertifizierung durch die DDA
- Welche Aussage zur Chronologie und zu den Mechanismen der Spättypreaktion ist nicht korrekt?
- Die notwendige Zeit für die Entwicklung einer Sensibilisierung beträgt bei nicht schweren Arzneimittelreaktionen (z. B. makulopapulöses Exanthem) etwa fünf bis zehn Tage.
- Ausgeprägte Hautveränderungen im Rahmen einer Spättypreaktion brauchen häufig mehrere Wochen bis zur vollständigen Abheilung.
- Bei ausreichend langer Applikation eines erstmals eingesetzten Medikamentes kann die Sensibilisierungsphase direkt in die Auslösephase übergehen.
- Die Ursache für die unterschiedlichen klinischen Manifestationsformen einer Typ-IV-Reaktion sind die verschiedenen möglichen T-Zell-Aktivierungsmuster.
- Urtikaria und Angioödeme sind häufige Vorläufer eines makulopapulösen Exanthems.
- Welcher Faktor begünstigt die Entwicklung einer allergischen oder Intoleranzreaktion vom Spättyp nicht?
- ein durch einen viralen oder bakteriellen Infekt aktiviertes Immunsystems
- weibliches Geschlecht
- ein Body-Mass-Index von über 30
- die verlangsamte Metabolisierung eines Arzneimittels
- eine immungenetische Prädisposition für die Entwicklung allergischer Reaktionen
- Welche Aussage zur Abklärung von Arzneimittelreaktionen vom Spättyp trifft nicht zu?
- Die Bestimmung der Konzentrationen spezifischer IgE-Antikörper, die gegen Penicilline gerichtet sind, sollte bei Verdacht auf eine Amoxicillin-Allergie stets erfolgen.
- Intra- und Epikutantests werden, soweit keine Kontraindikationen bestehen, regelmäßig im Rahmen der Diagnostik eingesetzt.
- Die Erfragung der vorherrschenden Effloreszenz im Rahmen der Anamneseerhebung erlaubt oftmals eine Differenzierung zwischen Sofort- und Spättypreaktion.
- Der Lymphozytenaktivierungstest (LTT) ist ein aufwendiges In-vitro-Testverfahren, das nicht standardisiert ist und die Routinediagnostik allenfalls ergänzen kann.
- Bei einer Expositionstestung sollte das verdächtigte Medikament möglichst in der Form appliziert werden, in der es vor Auftreten der Reaktion verabreicht wurde.
- Welche Aussage zu Beta-Lactam-Antibiotika ist richtig?
- Aminopenicilline gelten als sichere Antibiotika und sind nur selten Auslöser von Spättypreaktionen.
- Cephalosporine müssen generell bei einer vermuteten oder nachgewiesenen Penicillinallergie gemieden werden.
- Aztreonam weist lediglich eine potenzielle Kreuzreaktivität mit Ceftazidim auf und kann deshalb bei Allergien auf verschiedene Beta-Lactam-Antibiotika problemlos eingesetzt werden.
- Aminobenzyl-Seitenketten sind Bestandteil aller Beta-Lactam-Antibiotika.
- Erythema-exsudativum-multiforme-artige Exantheme und die akute exanthematische Pustulose sind die am häufigsten durch sie ausgelösten Krankheitsbilder. Makulöse/makulopapulöse Exantheme lösen sie nur relativ selten aus.
- Welche Aussage zu NSAR ist nicht richtig?
- Im Gegensatz zu Soforttyp- werden Spättypreaktionen selten durch NSAR ausgelöst.
- Unter den NSAR ist Paracetamol der häufigste Auslöser fixer Arzneimittelexantheme.
- Kreuzreaktivitäten zwischen NSAR im Rahmen von Spättypreaktionen kommen regelmäßig vor.
- Oxicame (Piroxicam, Meloxicam) sind unter den NSAR die häufigsten Auslöser T-Zell-vermittelter Reaktionen.
- Celecoxib ist eine seltene Ursache von Spättypreaktionen.
- Welches Symptom gilt nicht als Alarmzeichen für eine schwere Arzneimittelreaktion?
- Fieber > 38,5°C
- atypische Kokarden
- zentrofaziales Ödem und/oder diffuse (erythematöse) Schwellungen
- Eosinophilie (> 1,5 × 109 Zellen/l) und/oder Neutrophilie
- generalisierter Pruritus
- Welche Arzneimittelgruppe löst nur sehr selten makulöse/makulopapulöse Arzneimittelreaktionen aus?
- Antibiotika
- nichtsteroidale Antirheumatika
- Röntgenkontrastmittel
- Antiepileptika (z. B. Carbamazepin)
- Urikostatika (z. B. Allopurinol)
- Welche Aussage zu Spättypreaktionen auf Röntgenkontrastmitteln trifft nicht zu?
- Spättypreaktionen sind meist selbstlimitierend.
- Ionische-monomere Kontrastmittel weisen das höchste Risiko für Spättypreaktionen auf und sollten deshalb möglichst nicht verwendet werden.
- 1–3 % der mit Röntgenkontrastmitteln untersuchten Patienten entwickeln eine Spättypreaktion.
- Sie manifestieren sich meist in Form von leicht- bis mittelgradig ausgeprägten, makulösen oder makulopapulösen Exanthemen.
- Das Kontrastmittelmolekül selbst und nicht das daran gebundene Iod stellt das eigentliche Allergen dar.
- Welche Aussage zu Antikoagulantien ist richtig?
- Kreuzreaktivitäten zwischen Heparinpräparaten kommen nur sehr selten vor.
- Ein geschlechtsabhängiges Risiko für die Entwicklung einer Spättypreaktion besteht nicht.
- Der synthetische Faktor-Xa-Inhibitor Fondaparinux weist ein besonders hohes Sensibilisierungsrisiko auf.
- Generalisierte Exantheme ohne Akzentuierung der Hautveränderungen im Applikationsareal schließen Heparine als Ursache nahezu aus.
- Schwangere sollten bevorzugt mit Nadroparin behandelt werden, da dies bei dieser Patientinnengruppe am seltensten Spättypreaktionen hervorruft.
- Welche Aussage zu Lokalanästhetika trifft zu?
- Kreuzreaktivitäten zwischen Lokalanästhetika vom Amid- und Ester sind häufig.
- Das in Adrenalin-haltigen Lokalanästhetika als Antioxidans eingesetzte Natriumdisulfit kann Ursache einer Allergie vom Spättyp sein.
- Spättypreaktionen auf Lokalanästhetika gehören zu den häufigsten Arzneimittelallergien überhaupt.
- Lokalanästhetika vom Estertyp lösen sehr viel seltener als solche vom Amidtyp Spättypreaktionen aus.
- Die in Lokalanästhetika häufig enthaltenen Konservierungsstoffe Methyl- und Propylparahydroxybenzoat besitzen kein allergenes Potenzial und spielen deshalb in der allergologischen Diagnostik keine Rolle.
Liebe Leserinnen und Leser, der Einsendeschluss an die DDA für diese Ausgabe ist der 29. Dezember 2017. Die richtige Lösung zum Thema „Lepra“ in Heft 8 (August 2017): (1c, 2b,3c, 4a, 5d, 6d, 7c, 8c, 9e, 10d).
Bitte verwenden Sie für Ihre Einsendung das aktuelle Formblatt auf der folgenden Seite oder aber geben Sie Ihre Lösung online unter http://jddg.akademie-dda.de ein




