Hauterkrankungen bei Diabetes mellitus
Circa ein Drittel aller Diabetiker entwickeln im Laufe der Erkrankung Hauterscheinungen.
Bestimmte diabetische Hautmanifestationen können mit extrakutanen diabetischen Komplikationen wie Neuropathie und Vaskulopathie korreliert sein.
Hauterkrankungen bei Diabetes mellitus sind zum Teil mit einer deutlich erhöhten Morbidität und Mortalität verbunden.
Bei der molekularen Pathogenese diabetischer Hauterscheinungen spielen sowohl die pathologischen Glukosekonzentrationen, Bildung von reaktiven Sauerstoffradikalen und AGEs zusammen.
AGEs interagieren sowohl mit intrazellulären als auch mit extrazellulären Proteinen und binden zudem an RAGE, wodurch es zu einer proinflammatorischen Zellantwort kommt.
Depletion antioxidativer Enzymsysteme und Induktion ROS-generierender Enzyme führen zur vermehrten Bildung von oxidativem Stress bei Diabetes mellitus.
Diabetische Mikro- und Makroangiopathie sowie die diabetische Neuropathie sind zentrale pathogenetische Säulen der diabetischen Hauterscheinungen.
Im Laufe ihres Lebens leiden 15–25 % aller Diabetiker an einem diabetischen Fußsyndrom.
Die Klassifikation des diabetischen Fußsyndroms erfolgt nach Wagner und Armstrong, wobei Infektion und Angiopathie die Prognose verschlechtern.
Eine angiologische und orthopädische Mitbetreuung kann entscheidend zur Verbesserung der Langzeitprognose von Patienten mit diabetischem Fußsyndrom beitragen.
Die lokale Applikation von Wachstumsfaktoren sowie autologe Zelltransplantationen sind neue Methoden zur Behandlung von diabetischen Ulzera.
Der Charcot-Fuß kann ein Erysipel, eine tiefe Beinvenenthrombose oder einen akuten Gichtanfall imitieren.
Der Charcot-Fuß wird als inflammatorisches Syndrom angesehen, bei dem es infolge eines erhöhten Knochenmetabolismus zu Knochendestruktionen und Deformitäten kommt.
Bei klinischem Verdacht auf einen Charcot-Fuß ist zur Diagnosesicherung eine Röntgenaufnahme und ein MRT des Fußes indiziert.
Diabetiker besitzen bei Hautinfektionen ein fünffach erhöhtes Komplikationsrisiko und ein vierfach erhöhtes Hospitalisierungsrisiko im Vergleich zu Nichtdiabetikern.
Rezidivierende bakterielle Infekte der Haut sollten immer an einen Diabetes mellitus denken lassen.
Die durch Pseudomonas aeruginosa verursachte maligne Otitis externa kann zu Osteitis oder Meningitis führen und verläuft bei circa 50 % der Patienten tödlich.
Eine Tinea pedis kann Eintrittspforte für potenziell lebensgefährliche bakterielle Infektionen der Haut sein und sollte daher immer saniert werden.
Die diabetische Dermopathie manifestiert sich mit rundlich-ovalen, hyperpigmentierten und teils atrophischen Hautveränderungen an den Unterschenkelstreckseiten. Betroffene Patienten leiden oft an einer diabetischen Neuropathie, Nephropathie und Retinopathie.
Die Bullosis diabeticorum ist eine Ausschlussdiagnose. Im Verlauf sollte mehrfach eine direkte und indirekte Immunfluoreszenzdiagnostik insbesondere zum Ausschluss eines bullösen Pemphigoids durchgeführt werden.
10–65 % der Patienten mit Necrobiosis lipoidica sind Diabetiker.
Typische Prädilektionsstellen sind die Streckseiten der Unterschenkel, wo zentrifugal sich ausbreitende, orange-bräunliche, atrophe Plaques mit livid- oder braunroten Randsaum auftreten. Ulzera können nach Bagatelltraumen auftreten und weisen oft eine schlechte Heilungstendenz auf.
Die Differenzialdiagnose der Necrobiosis lipoidica beinhaltet das Granuloma anulare, das nekrobiotische Xanthogranulom, die zirkumskripte Sklerodermie, die Sarkoidose und bei ulzerierenden Formen das tubero-serpiginöse Syphilid.
Therapeutisch kommen initial topische Glukokortikoide, Bade-PUVA und topische Calcineurininhibitoren zum Einsatz.
Das Granuloma anulare kann mit Diabetes mellitus assoziiert sein, tritt jedoch überwiegend spontan auf.
Das isolierte Granuloma anulare ist oft selbstlimitierend. Die Behandlung disseminierter Formen dagegen oft langwierig.
Das Scleroedema adultorum Buschke ist nicht nur mit Diabetes mellitus, sondern auch mit Infekten und lymphoproliferativen Erkrankungen assoziiert.
Befall mehrerer Gelenke wird als wichtige Frühkomplikation des Typ-I-Diabetes mellitus angesehen und deutet auf ein erhöhtes Risiko extrakutaner Komplikationen hin.
Diabetische Mikroangiopathie, Akkumulation von AGEs und Aktivierung profibrotischer Signalwege führen zur diabetischen Cheiroarthropathie.
Nichtsteroidale Antiphlogistika und physiotherapeutische Maßnahmen können bei der diabetischen Cheiroarthropathie eine symptomatische und funktionelle Besserung erzielen.
Eine Acanthosis nigricans kommt bei Diabetikern mit erhöhtem BMI häufig vor. Bei rasantem Wachstum und Mundschleimhautbefall muss an ein zugrundeliegendes Malignom gedacht werden.
Neben einer Gewichtsreduktion und optimalen Einstellung des Blutzuckerspiegels können bei Acanthosis nigricans Retinoide, Harnstoff- und Salicylsäure-haltige Externa, Calcipotriol, Metformin sowie operative-ablative Verfahren hilfreich sein.
Neuropathie, Xerosis cutis und Medikamente tragen zum chronischen Pruritus bei Diabetikern bei.
Neben Antihistaminika können beim diabetischen Pruritus schmerzmodulierende Substanzen wie Gabapentin, Pregabalin oder Antidepressiva eingesetzt werden.
Bei Vorliegen eines Typ-I-Diabetes mellitus und einer nicht-segmentalen Vitiligo sollte an ein autoimmun polyglanduläres Syndrom gedacht werden.
Topische Glukokortikoide und Calcineurininhibitoren sowie die UVB 311 nm-Lichttherapie sind diejenigen Therapien mit der größten therapeutischen Evidenz bei der nicht-segmentalen Vitiligo.
Häufig leiden Patient mit einem APS-2 oder -3 an Diabetes mellitus und nicht-segmentaler Vitiligo.
Charakteristische Hauterscheinungen beim HAIR-AN-Syndrom sind schwere Akne, androgenetische Alopezie, Seborrhoe und Hirsutismus.
Subkutan injiziertes Insulin kann in seltenen Fällen zu schweren IgE-vermittelten anaphylaktischen Reaktionen führen.
Sulfonylharnstoffe sind die Antidiabetika, die bei Diabetikern am häufigsten zu Exanthemen führen.
Zusammenfassung
Diabetes mellitus ist eine der häufigsten Erkrankungen der westlichen Industrienationen mit weltweit circa 300 Millionen Betroffenen. Die diabetische Stoffwechsellage führt zu Veränderungen praktisch aller Zelltypen und Organe des Körpers. Komplikationen an der Haut zählen hierbei zu den häufigsten Veränderungen. Da Hauterscheinungen einem Diabetes mellitus vorangehen können, besitzen sie eine diagnostische Relevanz. Andere Hautveränderungen und -erkrankungen entwickeln sich erst im Laufe eines Diabetes mellitus, sind mitunter mit Komplikationen innerer Organe assoziiert oder treten als unerwünschte Wirkung einer antidiabetischen Therapie auf. Besonders das Auftreten eines diabetischen Fußsyndroms geht mit einer signifikant erhöhten Morbidität und Mortalität von Diabetes-Patienten einher und führt zu einem bedeutsamen Anstieg direkter und indirekter Kosten im Gesundheitssystem. In diesem Übersichtsartikel werden die häufigsten Hauterkrankungen bei Diabetes mellitus sowie deren Pathophysiologie und aktuelle Therapie dargestellt.
Einleitung
Diabetes mellitus ist eine der häufigsten Krankheiten der westlichen Industrienationen. Die Prävalenz im Jahre 2010 betrug weltweit 6,4 % mit circa 285 Millionen betroffenen Erwachsenen und dürfte bis 2025 auf 324 Millionen steigen . Nosologisch wird der Diabetes mellitus traditionsgemäß in zwei pathophysiologisch unterschiedliche Typen unterteilt: Beim Typ-I-Diabetes mellitus kommt es infolge einer autoimmunologisch bedingten Zerstörung der β-Zellen des Pankreas zum Versiegen der endogenen Insulinproduktion. Betroffen sind überwiegend Kinder und Jugendliche. Eine Insulinsubstitution ist meist von Anfang an erforderlich. Der Typ-II-Diabetes mellitus ist demgegenüber durch Insulinresistenz gekennzeichnet. Die Inzidenz dieser Diabetes-Form steigt mit dem Lebensalter und korreliert mit dem „Body Mass Index“ (BMI). Initial ist der Typ-II-Diabetes nicht insulinpflichtig. Daneben werden noch weitere Subtypen von Diabetes mellitus unterschieden, z. B. eine angeborene Defizienz der β-Zellen des Pankreas, Störungen in der Insulin-Signaltransduktion, Diabetes mellitus im Rahmen von Erkrankungen des exokrinen Pankreas und syndromatischer Polyendokrinopathien .
Epidemiologisch kommt es bei circa 30 % aller Diabetiker im Laufe des Lebens zu Hauterscheinungen . Diese treten meistens im Verlauf der Erkrankung auf, in einigen Fällen können Hauterkrankungen einem Diabetes mellitus jedoch vorausgehen oder Teilsymptom eines hereditären oder erworbenen Syndroms sein. Generell besteht keine eindeutige Korrelation zwischen der Inzidenz oder dem Ausmaß von Hauterscheinungen bei Diabetes mellitus und dem Schweregrad der diabetischen Stoffwechsellage. Bestimmte Hauterkrankungen bzw. Manifestationen können allerdings auf extrakutane diabetische Komplikationen (z. B. diabetische Neuropathie oder Vaskulopathie) hinweisen . Klinisch am bedeutendsten sind solche Hauterkrankungen bei Diabetes mellitus, welche mit einer erhöhten Morbidität und Mortalität der betroffenen Patienten einhergehen sowie mit einem erhöhten Kostenaufwand für unser Gesundheitssystem. Die direkten Kosten für die Behandlung von Patienten mit Diabetes mellitus in Deutschland beliefen sich im Jahre 2007 auf geschätzte 42 Milliarden € . Schließlich können Hauterscheinungen Folge einer eingeleiteten antidiabetischen Therapie sein.
Pathophysiologie der allgemeinen diabetischen Stoffwechsellage mit Fokus auf die Haut
Diabetes mellitus schädigt durch sehr unterschiedliche Pathomechanismen die Hautfunktion in komplexer Weise.
Untersuchungen an in-vitro-Zellkultur-Systemen konnten zeigen, dass es beim Diabetes mellitus zum einen direkt durch pathologische Glukosekonzentrationen, zum anderen indirekt, durch Bildung sogenannter advanced glycation end-products (AGEs) zu negativen Wirkungen auf nahezu alle Zellparameter kommt. Pathologische Glukosekonzentrationen hemmen die Proliferation, Migration und Proteinbiosynthese von Keratinozyten und Fibroblasten . In Endothelzellen bewirken sie Apoptose und hemmen die Stickstoffmonoxid-Synthase (NOS) und damit die NO-Synthese. Dies führt in vivo zu einer verminderten Vasodilatation . Pathologische Glukosekonzentrationen unterdrücken zudem die Chemotaxis und Phagozytose von Zelltypen der angeborenen Immunabwehr . AGEs entstehen aus einer nichtenzymatischen Reaktion (Glykation) von Glukose und Proteinen, Lipiden und Nukleinsäuren . AGEs interagieren mit einer Reihe von intrazellulären und extrazellulären Proteinen, z. B. Kollagen-Typ I, Superoxid-Dismutase 1 oder epidermal growth factor receptor und attenuieren dadurch deren biologische Funktion. AGEs binden außerdem an RAGE (Receptor for AGEs). Dadurch kommt es zu Aktivierung des kanonischen nukleären Faktor-κB (NF-κB)-Signalweges mit Induktion proinflammatorischer Zytokine . Sowohl pathologische Glukosekonzentrationen als auch AGEs führen zu einer vermehrten Bildung von intrazellulärem oxidativen Stress, inklusive der Bildung reaktiver Sauerstoffspezies (ROS). Dies kommt u. a. durch Depletion antioxidativer Schutzenzyme wie Glutathion oder der mitochondrialen Superoxid-Dismutase zustande, zum anderen durch Induktion ROS-generierender Enzyme wie z. B. Nikotinamid-Adenin-Dinukleotid-Phosphat-Oxidase .
Die oben skizzierten Pathomechanismen münden in eine diabetische Mikro- und Makroangiopathie, in deren Folge es zu einer Gewebshypoxie kommt, die auch die Nerven schädigt . Folge der diabetischen Neuropathie ist eine Beeinträchtigung sensomotorischer und autonomer Nervenfunktionen mit resultierender verringerter Schmerzwahrnehmung, vermehrter Verletzlichkeit gegenüber exogenen Traumata, Durchblutungsstörungen, Anhidrose und Xerosis cutis .
Komplikationen an der Haut bei Diabetes mellitus
Diabetisches Fußsyndrom
Das diabetische Fußsyndrom ist eine der wichtigsten Komplikationen bei Diabetes mellitus. Die Therapie dieser Erkrankung stellt eine interdisziplinäre Herausforderung dar . Im Laufe ihres Lebens sind 15–25 % aller Diabetiker von einem diabetischen Fußsyndrom betroffen. Die Amputationsrate bei Vorliegen dieser Erkrankung liegt bei circa 25 %. Etwa 50 % aller Diabetiker versterben innerhalb von drei Jahren nach Amputation . Die jährlichen Kosten des diabetische Fußsyndroms werden europaweit auf 4 500–16 835 € pro Patient geschätzt und sind vom Vorhandensein einer peripheren arteriellen Verschlusserkrankung oder einer Infektion abhängig .
Die Pathogenese des diabetischen Fußsyndroms ist komplex und beinhaltet neben der diabetischen Mikro- und Makroangiopathie, der diabetischen Neuropathie, auch koexistierende Deformitäten des Fußskelettes (Hallux valgus, Krallenzehen u. a.) und das Tragen von ungeeignetem Schuhwerk . Meist geht dem diabetischen Fußsyndrom ein Bagatelltrauma voraus . Die Wundheilung ist auf zellulärer Ebene in allen Phasen beeinträchtigt. Chemotaxis und Phagozytose von Zellen der angeborenen Immunabwehr sind vermindert, Produktion antimikrobieller Peptide reduziert, Migration und Proliferation von epidermalen Keratinozyten sowie die Matrixsynthese durch Fibroblasten gestört . Ein geändertes Zytokinprofil mit Erhöhung proinflammatorischer Zytokine, z. B. Tumor-Nekrose-Faktor (TNF), auf der einen Seite, und die Verminderung von Wachstumsfaktoren auf der anderen Seite, tragen zur gestörten Wundheilung bei (Abbildung ).
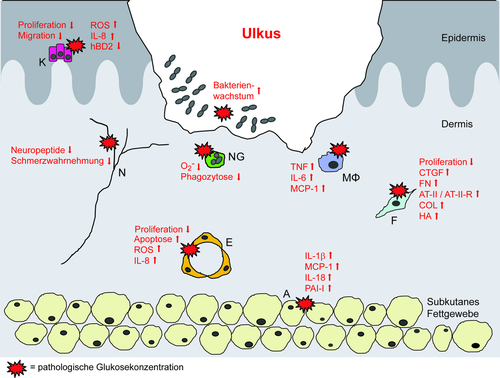
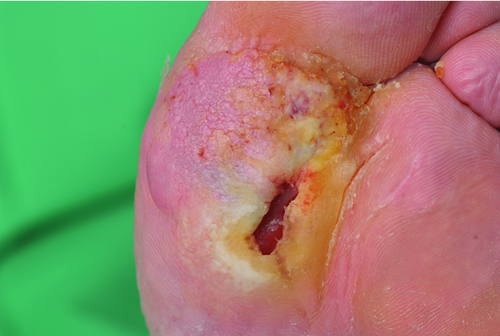
Klinisch zeichnet sich das diabetische Fußsyndrom durch ein Ulkus aus, welches infolge der diabetischen Neuropathie und der damit verbundenen verringerten Schmerzempfindung vorrangig an druckbelasteten Stellen lokalisiert ist . Vorwölbung des 2. und 3. Metatarsalköpfchens und Fehlbelastungen führen zu Hyperkeratosen und im Verlauf zu einem scharf begrenzten Ulkus mit hyperkeratotischem Rand und geringer Granulationsneigung (Abbildung ). Das rein neuropathische Ulkus (Malum perforans) muss hiervon abgegrenzt werden. Beim neuropathischen Ulkus ist die Neuropathie von entscheidender pathogenetischer Bedeutung, während die Durchblutung normal bleibt. Der Fuß ist typischerweise warm, die Fußpulse tastbar und die Schweißbildung reduziert . Die Gefahr einer Osteomyelitis steigt mit zunehmender Tiefe des Ulkus . Beim neuroischämischen Ulkus ist der Fuß dagegen kalt und die Fußpulse fehlen. Es besteht eine Atrophie der Haut und Hautanhangsgebilde. Eine Claudicatio intermittens kann bei gleichbestehender Neuropathie fehlen.
Die Klassifikation des diabetischen Fußsyndroms erfolgt nach den Leitlinien der Deutschen Diabetes Gesellschaft und der Empfehlung der Arbeitsgemeinschaft Fuß der DDG (Tabelle ), wobei koexistierende Infektionen und eine Angiopathie die Prognose beeinflussen .
Tabelle 1. Klassifikation des diabetischen Fußes nach Wagner und Armstrong
| Wagner Grad | 0 | 1 | 2 | 3 | 4 | 5 |
|---|---|---|---|---|---|---|
| Armstrong Stadium | Prä- oder postulzerative Läsion | Oberflächige Wunde | Wunde bis zur Ebene von Sehne oder Kapsel | Wunde bis zur Ebene von Knochen oder Gelenk | Nekrose von Fußteilen | Nekrose des gesamten Fußes |
| A | Ohne Infektion und Ischämie | |||||
| B | Mit Infektion | |||||
| C | Mit Ischämie | |||||
| D | Mit Infektion und Ischämie | |||||
Die Therapie des diabetischen Fußsyndroms erfordert ein interdisziplinäres Vorgehen . Neben regelmäßigen Wunddébridements zur Entfernung von avitalem Gewebe, der Applikation von lokalen Antiseptika (z. B. hydrophiles Polyhexanid-Gel) sowie Wundauflagen, die an die jeweilige Wundphase angepasst sind, sollten die diabetische Stoffwechsellage optimiert und die akrale Durchblutung gefördert werden. Es ist ratsam frühzeitig eine angiologische Diagnostik durchzuführen und, falls indiziert, Rekanalisationseingriffe wie z. B. eine perkutane transluminale Angioplastie, Stenteinlage oder ein Bypass durchzuführen . Eine Revaskularisation ist in der Lage das Risiko einer Amputation zu reduzieren. Falls diese operativ nicht möglich ist, kann eine Therapie mit Alprostadil oder Iloprost zur Verbesserung der arteriellen Durchblutung durchgeführt werden . Bestehen Kontraindikationen gegen ein chirurgisches Débridement unter Vollnarkose ist zudem ein biochirurgisches Débridement mit medizinischen Maden eine Alternative . Große Wunddefekte können mittels Spalthauttransplantationen gedeckt werden. Durch den Einsatz einer Vakuumtherapie können die Chancen eines vitalen Transplantats erhöht werden. Bei Infektionszeichen sollten nach entsprechender Diagnostik (tiefe Abstriche, apparative Bildgebung mittels Magnetresonanzsonographie [MRT] bei Verdacht auf Osteomyelitis) systemische Antibiotika unter Berücksichtigung des Resistogramms angeordnet werden . Weitere Maßnahmen sind Bettruhe und die Verschreibung von orthopädischen Schuhen zur Entlastung von druckbelasteten Stellen . Fehlgestellte Fußknochen können chirurgisch-orthopädisch korrigiert werden.
In der Literatur sind zudem weitere Therapieoptionen beschrieben, die die Wundheilung beim diabetischen Fußsyndrom verbessern sollen. Hierzu gehören die lokale Applikation von Wachstumsfaktoren wie epidermal growth factor, basic fibroblast growth factor, platelet-derived growth factor, granulocyte macrophage colony-stimulating factor (GM-CSF) sowie „künstliche Haut“ (autologe Transplantation von Fibroblasten und/oder Keratinozyten) . Ultima Ratio bei Versagen der obigen Maßnahmen ist die Amputation des betroffenen Fußes, möglichst unter operativer Schonung der gewichtstragenden Strukturen .
Charcot-Fuß
Der Charcot-Fuß (Syn.: Acroosteolysis ulceromutilans, diabetische Neuroosteoarthropathie) betrifft primär nicht die Haut, kann aber ein Erysipel, eine tiefe Venenthrombose oder einen akuten Gichtanfall imitieren und sollte daher dem Dermatologen bekannt sein . Das Risiko einer Fußamputation ist hoch, falls die Erkrankung verspätet erkannt wird .
Der Charcot-Fuß wird als inflammatorisches Syndrom mit multifaktorieller Genese angesehen. Pathogenetisch werden eine gemischte (sensomotorische und autonome) diabetische Neuropathie, exogene Traumata und ein gestörter Knochenmetabolismus diskutiert . Die Neuropathie führt zu vermehrter Durchblutung, erhöhtem Knochenmetabolismus und Knochenabbau, in dessen Folge es zu Knochendestruktionen, Dislokationen und Deformitäten kommt . Patienten mit nicht-diabetischen Neuropathien können ebenfalls einen Charcot-Fuß entwickeln, allerdings stellt die diabetische Neuropathie die häufigste Ursache dieser Erkrankung dar. Sowohl Knochen, Gelenke als auch Weichteilgewebe des Fußes sind beim Charcot-Fuß betroffen. Im Initialstadium ist der betroffene Fuß warm, geschwollen und erythematös. Es bestehen geringe bis mäßige Schmerzen. Die Fußpulse sind typischerweise tastbar . Im Spätstadium kommt es zu einer Kollabierung der Mittelfuß-Knochen (rocker bottom foot, Tintenlöscherfuß) (Abbildung ). Diese Deformität kann zu Ulzerationen an den fehlbelasteten Arealen führen. Für die Diagnosestellung ist neben der Anamnese und Klinik die bildgebende Diagnostik wichtig. Konventionelle Röntgenaufnahmen des Fußes zeigen Knochenfrakturen und Gelenkdeformitäten. In Frühstadien ist allerdings ein MRT, das eine höhere Sensitivität und Spezifizität besitzt, Methode der ersten Wahl . Es dient auch zur Abgrenzung einer Osteomyelitis. Eine Skelettszintigraphie mit Technetium-99m, eine Szintigraphie mit Radioisotop-markierten Leukozyten oder eine Positronen-Emissions-Tomographie können insbesondere zur differenzialdiagnostischen Abgrenzung einer Osteomyelitis ebenfalls hilfreich sein .
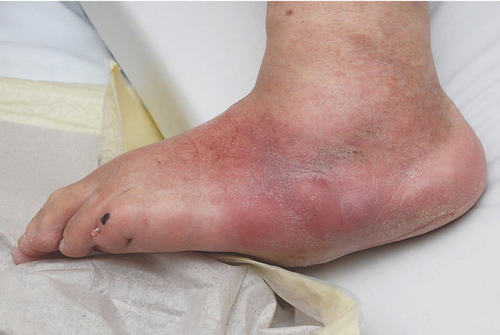
Therapeutisch ist eine zügige und komplette Entlastung des Fußes mittels eines total contact cast die wichtigste Maßnahme. Dadurch soll eine weitere Progression und Frakturbildung vermieden werden . Nach Abheilung, die mehrere Monate dauern kann, sollte eine Entlastung des Fußes durch orthopädische Schuhe erfolgen .
Infektiöse Erkrankungen
Bakterielle und mykotische Infektionen der Haut treten häufiger bei Patienten mit Diabetes mellitus als bei Gesunden auf. Kommt es zu einem infektiösem Haut- und Weichteilinfekt ist das Komplikationsrisiko bei Diabetikern fünffach höher als bei Kontrollpersonen . Pathogenetisch prädisponiert zum einen die Neuropathie dazu, dass mechanische Traumata nicht registriert werden, wodurch indolente Eintrittspforten entstehen, zum anderen begünstigt die diabetische Stoffwechsellage ein vermehrtes Keimwachstum in der Eintrittspforte und führt zu Störungen sowohl der angeborenen als auch der adaptiven Immunabwehr . Bei rezidivierenden oder therapieresistenten Hautinfektionen sollte daher immer an Diabetes mellitus gedacht werden .
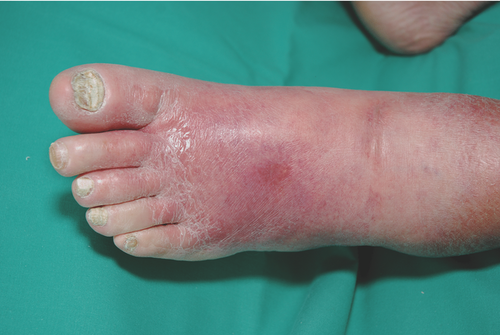
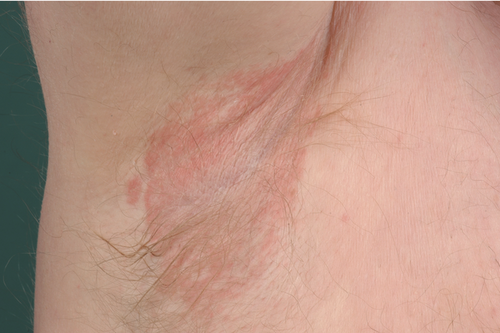
Bakterielle Infektionen der Haut treten bei Diabetikern gehäuft auf . Charakteristisch sind Erythrasma, Impetigo contagiosa, Follikulitiden, multiple Abszesse, Furunkel und Karbunkel. Erysipele und Phlegmone zeichnen sich nicht selten durch einen schwereren Verlauf aus (Abbildungen , ) . Therapeutisch kommen antiseptische oder antibiotische Lokaltherapeutika sowie bei Zeichen einer fortschreitenden Beteiligung der Weichteilgewebe oder systemischen Infektionszeichen eine zügige Resistogramm-basierte systemische Antibiose zum Einsatz.
Eine Besonderheit einer bakteriellen Infektion der Haut im Bereich des HNO-Traktes stellt die maligne Otitis externa bei Diabetes mellitus dar. Sie wird durch Pseudomonas aeruginosa verursacht, kann zur Osteitis oder Meningitis führen und verläuft bei circa 50 % der Betroffenen tödlich . Die nekrotisierende Fasziitis betrifft Diabetiker häufiger als Nicht-Diabetiker. Der Verlauf dieser Erkrankung ist bei Diabetikern nicht selten fulminant und mit einer hohen Mortalität verbunden. Die häufigsten Auslöser sind Staphylococcus aureus, Streptococcus pyogenes, anaerobe Streptococcus- und Bacteroides-Spezies, wobei oft Mischinfektionen bestehen . Innerhalb von 24–48 Stunden entwickelt sich aus einem initialen Erythem eine lividrote unscharf begrenzte Verfärbung, teils mit Blasen, gefolgt von einer weitreichenden Gewebezerstörung in der Tiefe. Eine zügig eingeleitete systemische Antibiose und chirurgische Débridements verbunden mit intensivmedizinischer Überwachung sind nötig, wobei die Mortalität trotz optimaler Therapie bei 20–30 % liegt .
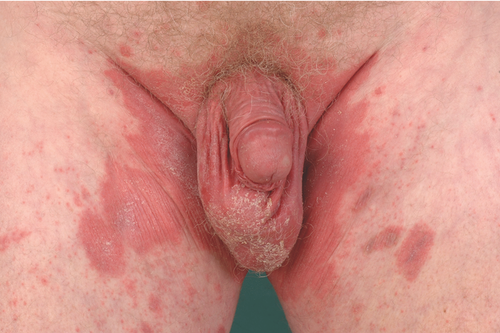
Mukokutane Infektionen durch Candida-Spezies treten bei Diabetikern ebenso gehäuft auf und treten als Mundsoor, Angulus infectiosus/Perlèche, Balanoposthitis und Vulvovaginitis candidomycetica, Candida-Paronychie, intertriginöse Candidose in Erscheinung (Abbildung ) . Klinisch entwickeln sich weißliche abstreifbare Beläge an der Mundschleimhaut, Erytheme und Rhagaden an den Mundwickeln, Erytheme, Schuppung und Rhagaden in den Interdigitalräumen oder scharf begrenzte, erythematöse und schuppende Plaques in den Achseln, inguinal und submammär mit typischen Satellitenläsionen. Anogenitaler Befall äußert sich oft mit chronischem lokalisierten Pruritus . Ob es bei Diabetikern zu einem gehäuften Auftreten von Infektionen mit Dermatophyten kommt, wird in der Literatur demgegenüber kontrovers diskutiert. Therapeutisch kommen bei der Behandlung mukokutaner Candida-Infektionen bei Diabetikern primär lokale Antimykotika zur Anwendung. Bei therapieresistenten Fällen kann eine systemische antimykotische Therapie erforderlich sein, wobei Wechselwirkungen und Kontraindikationen dieser Substanzen zu beachten sind. Da es bei Diabetikern gehäuft zu bakteriellen Infektionen der Haut kommt, sollten Eintrittspforten im Rahmen einer Tinea pedis immer adäquat behandelt werden. Unterstützend ist bei Diabetikern eine regelmäßige podologische Pflege sowie regelmäßige Fußinspektionen zu empfehlen .
Mit Diabetes mellitus assoziierte Hauterscheinungen und -erkrankungen
Rubeosis diabetica
Unter Rubeosis diabetica versteht man eine flushartige Rötung des Gesichts, die durch eine Störung des Vasomotorentonus mit resultierender Blutstauung im dermalen Gefäßplexus zustande kommt. Eine kausale Therapie ist bislang nicht bekannt .
Purpura diabeticorum
Bei Diabetikern treten nicht selten purpuriforme Flecken besonders an den Unterschenkeln auf. Pathogenetisch wird eine erhöhte Gefäßfragilität durch die diabetische Mikroangiopathie vermutet. Da keine kausale Therapie bekannt ist, sollten mechanische Traumata vermieden werden .
Diabetische Dermopathie (Binkley-Syndrom)
Die diabetische Dermopathie gehört zu den häufigsten Hautmanifestationen bei Diabetes mellitus, wird aber nur selten diagnostiziert, da die Hautveränderungen symptomlos sind. Klinisch imponieren rundlich bis ovale, hyperpigmentierte und teils atrophe Läsionen an den Streckseiten der Unterschenkel . Pathogenetisch werden die Hautveränderungen mit der diabetischen Mikroangiopathie in Zusammenhang gebracht . Dermatohistopathologisch finden sich Hämosiderinablagerungen in der Dermis, eine basale Hyperpigmentierung der Epidermis sowie verdickte Gefäße mit Hyalinablagerungen . Bemerkenswert ist die Assoziation dieser kutanen Manifestation des Diabetes mellitus mit einer Neuropathie, Nephropathie und Retinopathie. Daher sollte die Diagnose der diabetischen Dermopathie zu einem gezielten Screening der betroffenen Patienten für die zuvor erwähnten diabetischen Komplikationen führen . Therapeutisch existiert bislang keine wirksame Therapie gegen die diabetische Dermopathie .
Bullosis diabeticorum
Hier handelt es sich um rezidivierende umschriebene pralle Blasen auf nichtentzündlicher Haut, welche meist an den Streckseiten der Extremitäten und an den Fußrücken bei älteren Patienten mit Diabetes mellitus auftreten . Die Pathogenese dieser Hautveränderungen bleibt unklar. Der Inhalt der Blasen ist typischerweise steril, in der Dermatohistopathologie zeigen sich subepidermale Blasen . Eine spontane Heilung soll innerhalb 2–4 Wochen stattfinden. Symptomatisch können antiseptische Lokaltherapeutika oder topische Glukokortikoide der Wirkklasse II–III kurzfristig benutzt werden . Wichtig ist der definitive Ausschluss einer autoimmunbullösen Erkrankung, insbesondere eines bullösen Pemphigoids. Zur Differenzialdiagnostik einer Bullosis diabeticorum sollte daher immer eine direkte und indirekte Immunfluoreszenzdiagnostik, ggf. mehrmals, durchgeführt werden.
Necrobiosis lipoidica
Die Necrobiosis lipoidica kann als Prototyp einer mit Diabetes mellitus assoziierten Hauterkrankung angesehen werden. Obwohl sie nur bei circa 0,3–1,2 % aller Diabetiker auftritt, leiden 10–65 % aller Patienten mit Necrobiosis lipoidica an Diabetes mellitus . Die Necrobiosis lipoidica tritt jedoch auch bei anderen immunvermittelten Entzündungserkrankungen gehäuft auf. Klinisch charakteristisch sind initial erythematöse Papeln, die sich im Verlauf zu meist flachen, orangeroten Plaques mit zentraler Atrophie und Teleangiektasien mit einem unregelmäßigen, aufgeworfenen, livid- oder braunroten Randsaum entwickeln (Abbildung ) . Die Streckseiten der Unterschenkel sind meistens betroffen, die Erkrankung kann aber auch Fußrücken und Knöchel, in seltenen Fällen auch andere Körperteile betreffen. Bei circa 30 % der Patienten treten zentral schlecht heilende Ulzera auf, meist nach Bagatelltraumen . Die Läsionen sind oft asymptomatisch, allerdings können bei Ulkusbildung Schmerzen entstehen . Die Erkrankung verläuft chronisch und korreliert nicht mit dem Ausmaß der diabetischen Stoffwechsellage.
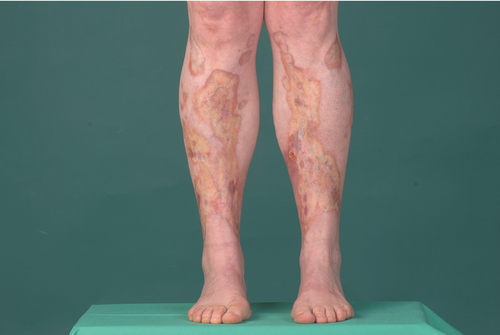
Die Pathogenese der Necrobiosis lipoidica ist lückenhaft verstanden. Eine Mikroangiopathie scheint eine wesentliche Rolle zu spielen . Histologisch sieht man in der gesamten Dermis bis ins subkutane Fettgewebe reichende nekrobiotische Kollagenbündel mit randständigen Histiozyten in Palisadenanordnung. Die Basalmembranen sind verdickt, die dermalen Gefäße thrombosiert . Im Gegensatz zu Granuloma anulare zeigt die Necrobiosis lipoidica eine Beteiligung der gesamten Dermis.
Differenzialdiagnostisch müssen Granuloma anulare, nekrobiotisches Xanthogranulom, zirkumskripte Sklerodermie und Sarkoidose abgegrenzt werden . Bei ulzerierenden Formen sollte differenzialdiagnostisch auch an ein tubero-serpiginöses Syphilid gedacht werden.
Die Therapie der Necrobiosis lipoidica ist schwierig. Randomisierte kontrollierte Studien zur Therapie dieser Erkrankung fehlen . Im Initialstadium kommen topisch hochpotente Glukokortikoide, auch unter Okklusion oder intraläsional, in Frage. Hier ist auf die Gefahr der Aggravierung einer schon bestehenden Atrophie zu achten . In kleineren Fallserien und Kasuistiken wurde über einen Erfolg durch lokale Bade-Psoralen plus UVA (PUVA)-Therapie sowie topische Calcineurininhibitoren berichtet. Kasuistiken und kleinere Fallserien deuten auf eine gewisse therapeutische Wirksamkeit von Pentoxifyllin, Thrombozytenaggregationshemmern, Chloroquin, Clofazimin, Ciclosporin, Mycophenolatmofetil, Prostaglandin E1 und Anti-TNF-Biologics bei der Erkrankung hin . In einer Fallserie mit 18 Patienten wurde zudem über positive Wirkungen von Fumarsäureestern bei Necrobiosis lipoidica berichtet . Bei schlecht heilenden Ulzera kann GM-CSF hilfreich sein.
Granuloma anulare
Das Granuloma anulare wird seit Jahrzehnten als eine typische mit Diabetes mellitus assoziierte Hauterkrankung angesehen. Neuere Studien bezweifeln jedoch diesen Zusammenhang. Die Erkrankung tritt in lokalisierter Form meistens spontan auf. Andere Assoziationen sind Autoimmunthyreoiditis, lymphoproliferative Erkrankungen sowie Infektionserkrankungen .
Klinisch kommt es zu anulär angeordneten dermalen Papeln oder subkutanen Knoten, die hautfarben oder lividrot sind. Die Hautveränderungen können sich zentrifugal ausbreiten mit zentraler Abblassung und Betonung der Ränder . Prädilektionsstellen sind Finger- und Handrücken, Fußrücken, Ellenbogen und Knie. Die Erkrankung ist in der Mehrzahl der Fälle auf eine oder wenige Stellen lokalisiert, kann jedoch in seltenen Fällen disseminieren und nahezu das gesamte Integument befallen (Granuloma anulare disseminatum) (Abbildung ).
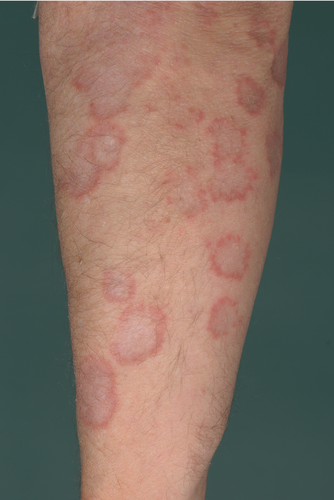
Histologisch finden sich degenerierte Kollagenfasern im Zentrum der Läsionen, die von palisadenartig angeordneten Makrophagen umgeben sind. Die obere bis mittlere Dermis ist in der Regel betroffen .
Während das isolierte Granuloma anulare vom Verlauf typischerweise selbstlimitiert ist, ist die Behandlung der disseminierten Form nicht selten schwierig. Im Gegensatz zur lokal begrenzten Form sind hier topische Glukokortikoide und topische Calcineurininhibitoren oder eine Kryotherapie wenig hilfreich. Hier kann die UVA1- oder Bade-PUVA-Therapie eine Alternative darstellen . Da 8-Aminochinolin-Derivate (Chloroquin und Hydroxychloroquin), Dapson und Clofazimin erfolgreich bei granulomatösen Erkrankungen der Haut eingesetzt werden, können diese auch beim disseminierten Granuloma anulare im Rahmen eines Heilversuchs eingesetzt werden . Einzelfallberichte existieren zudem über den Einsatz von Tranilast und Nicotinamid. Weitere Kasuistiken und Fallserien berichten über systemische Retinoide und Fumarsäureester, Ciclosporin sowie Anti-TNF-Biologics bei der Erkrankung . Da Diabetiker eine erhöhte Inzidenz von bakteriellen Infekten aufweisen, ist das Nutzen-Risiko-Verhältnis immunsuppressiver Therapien gerade bei off-label-Indikation immer sorgfältig abzuwägen.
Scleroedema adultorum Buschke
Das Scleroedema adultorum Buschke tritt gehäuft bei Kindern und jungen Frauen im Anschluss an Infekte auf. Bei älteren Menschen besteht jedoch eine auffällige Assoziation mit Diabetes mellitus (Scleroedema adultorum diabeticorum) und lymphoproliferativen Erkrankungen, insbesondere mit Paraproteinämien . Klinisch kommt es zu einer schnell fortscheitenden prallelastischen und typischerweise nicht eindrückbaren Verdickung der Haut meist am oberen Rücken, am Nacken und an den Armen (Abbildung ). Mitunter ist die Haut erythematös, die Follikelostien erweitert (Peau d‘orange-Zeichen) . Die Beweglichkeit der Arme, aber auch des Brustkorbes kann eingeschränkt sein. Letzteres kann zu einer restriktiven Lungenfunktionsstörung führen . Dermatohistopathologisch sind die Kollagenbündel verdickt und vermehrt, dermal finden sich Muzinablagerungen (v. a. Hyaluronsäure und Glykosaminoglykane) . Wichtige Differenzialdiagnosen sind die systemische Sklerodermie, die eosinophile Fasziitis sowie das Skleromyxödem.
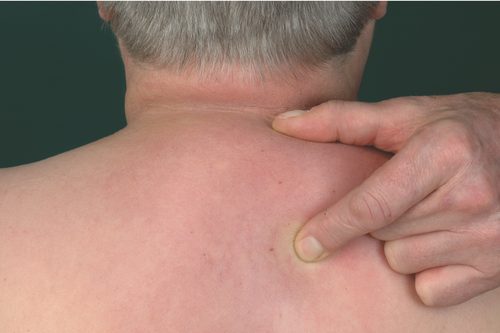
Die Therapie des Scleroedema diabeticorum stellt eine Herausforderung dar. Systemische Glukokortikoide (z. B. als intravenöse Dexamethason-Pulstherapie) alleine oder in Kombination mit Cyclophosphamid sind aufgrund der diabetischen Stoffwechsellage problematisch und können Infekte begünstigen. Anzustreben ist immer eine optimale Einstellung des Diabetes mellitus sowie eine regelmäßige Physiotherapie zum Erhalt der Mobilität der oberen Extremitäten und des Brustkorbes . Der therapeutische Effekt von PUVA, Prostaglandin E1, Methotrexat, Cyclosporin ist ungewiss .
Diabetische Cheiroarthropathie
Bei 8–50 % aller Patienten mit Diabetes mellitus kommt es zu einer eigentümlichen Verdickung der Haut verbunden mit einer verminderten Mobilität der Finger überwiegend beim Strecken. Charakteristisch ist das sogenannte prayer sign, d. h. die Unfähigkeit, die Palmae gegenseitig in Kontakt zu bringen, sowie das tabletop sign, d. h. die Unfähigkeit, die Palmae komplett auf einem Tisch legen zu können . Dermatohistopathologisches Korrelat beider Phänomene sind verdickte und desorganisierte Kollagenfasern sowie Muzinablagerungen in der Dermis, in Verbindung mit einer Verdickung der periartikulären Strukturen. Als Ursachen der diabetischen Cheiroarthropathie werden die diabetische Mikroangiopathie sowie AGEs diskutiert. Dadurch kommt es zu einer Ischämie und Aktivierung profibrotischer Signalwege in der Dermis. Die Glykation von Kollagen und anderer Matrixproteine verändert die biomechanischen Eigenschaften und den Metabolismus dieser Moleküle . Der Befall mehrerer Gelenke bei der diabetischen Cheiroarthropathie wird als wichtige Frühkomplikation bei Kindern mit Typ-I-Diabetes mellitus aufgefasst. Zum einen korreliert die diabetische Cheiroarthropathie mit dem Ausmaß der diabetischen Stoffwechsellage, zum anderen haben betroffene Patienten ein erhöhtes Risiko für das gleichzeitige Bestehen einer Mikrovaskulopathie, diabetischen Retinopathie und/oder Nephropathie. Die Diagnose der diabetischen Cheiroarthropathie wird primär klinisch gestellt. Sonographie oder MRT können eine Verdickung der Strecksehnen objektivieren .
Wichtige Differenzialdiagnosen sind die Dupuytrensche Kontraktur, das Karpaltunnelsyndrom, Tenosynovitiden und die Sklerodaktylie im Rahmen einer systemischen Sklerose. Bislang gibt es keine wirksame medikamentöse Therapie gegen die diabetische Cheiroarthropathie. Therapeutisch haben Aldosereduktasehemmer enttäuscht. Symptomatisch können im Intervall nichtsteroidale Antiphlogistika versucht werden. Physiotherapeutische Maßnahmen zur Erhaltung der Gelenkmobilität sowie eine optimale glykämische Kontrolle können die Symptome bessern .
Acanthosis nigricans
Eine Acanthosis nigricans kommt bei Diabetikern mit pathologisch erhöhtem BMI sehr häufig vor. Klinisch imponiert in den intertriginösen Arealen eine grau bis rehbraune, samtartige Verdickung und Hyperpigmentierung. Im Verlauf kommt es zu papillomatösen Exkreszenzen und Plaques (Abbildung ). Während die obigen Hautveränderungen bei adipösen Diabetikern (Pseudoacanthosis nigricans) typischerweise nur langsam voranschreiten, sollte jede rasch verlaufende Acanthosis nigricans, insbesondere wenn die Mundschleimhaut befallen ist, die Aufmerksamkeit auf ein zugrundeliegendes Malignom richten (Acanthosis nigricans maligna).
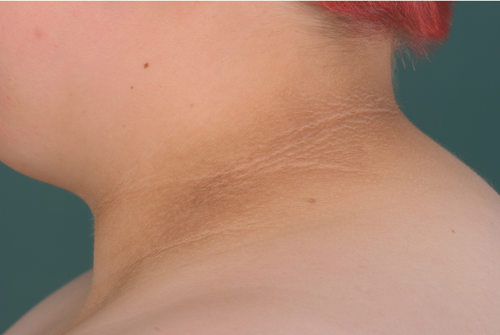
Histologisch findet man eine Hyperkeratose und Papillomatose sowie eine milde Akanthose der Epidermis. Die Anzahl der Melanozyten ist unverändert und die bräunliche Farbe kommt primär durch eine Verdickung der Epidermis zustande. Pathogenetisch kommt es durch die Insulinresistenz und hohe Konzentrationen von insulin growth factor (IGF)-1 zur verstärkten Aktivierung des IGF-1-Rezeptors mit konsekutiver Proliferation epidermaler Keratinozyten . Wahrscheinlich spielen mechanische Triggerfaktoren wie Reibung eine zusätzliche Rolle bei der Entstehung dieser Hauterkrankung. Kurativ ist bei Diabetikern mit Acanthosis nigricans in erster Linie eine Gewichtsreduktion und optimale Einstellung des Blutzuckerspiegels. In Einzelfällen können topische und systemische Retinoide, Harnstoff- und Salicylsäure-haltigen Externa, Calcipotriol, systemisch Metformin oder auch operative-ablative Verfahren hilfreich sein (CO2- oder Alexandrit-Laserung und Dermabrasio) .
Diabetischer Pruritus
Chronischer Pruritus tritt bei Diabetikern mit einer Häufigkeit von 3–49 % auf und kann zur erheblichen Beeinträchtigung der Lebensqualität führen . Pathogenetisch werden für den diabetischen Pruritus die diabetische Polyneuropathie (Small-Fiber-Neuropathie mit Schädigung der myelinisierten Ad- und nicht-myelinisierten C-Fasern), eine Xerosis cutis (durch Alter und Hypohidrose bei diabetischer autonomer Neuropathie aggraviert) sowie bestimmte Medikamente (Glimepirid, Metformin und Tolbutamid) verantwortlich gemacht . In Hautbiopsien von Patienten mit Diabetes wurde eine verminderte Nervenfaserdichte nachgewiesen .
Klinisch imponiert ein generalisierter Pruritus ohne primäre Hautveränderungen. Bei Chronifizierung kann es sekundär zum klinischen Bild einer Prurigo nodularis kommen . Bei Diabetikern mit lokalisiertem Pruritus sollten demgegenüber Hautinfektionen (z. B. intertriginöse Candidose) ausgeschlossen werden .
Ziel einer jeglichen Therapie des diabetischen Pruritus ist die optimale medikamentöse Einstellung der diabetischen Stoffwechsellage. Symptomatisch können hochdosierte Antihistaminika oder aufgrund der neuropathischen Komponente des diabetischen Pruritus schmerzmodulierende Substanzen wie Gabapentin, Pregabalin oder Antidepressiva erwogen werden . Zur Basistherapie eignen sich rückfettende harnstoffhaltige Externa, ggf. in Kombination mit prurituslindernden Substanzen (z. B. Kampfer, Menthol oder Polidocanol) .
Vitiligo
Eine Vitiligo findet sich gehäuft bei Typ-I-Diabetikern (ca. 1–7 %) während die Prävalenz dieser Erkrankung in der Normalbevölkerung bei 0,5 % liegt . In der Mehrzahl entwickelt sich bei Diabetikern eine nicht-segmentale Vitiligo als Ausdruck einer genetisch prädisponierten autoimmunvermittelten Entzündungserkrankung der Haut. Meistens tritt die Vitiligo bei Diabetikern solitär auf, kann jedoch bei Vorliegen weiterer Autoimmunerkrankungen Hinweis auf ein autoimmun polyglanduläres Syndrom (APS) sein. Hier handelt es sich definitionsgemäß um eine heterogene Gruppe von Autoimmunerkrankungen, in deren Verlauf es zu einer Insuffizienz von mindestens zwei endokrinen Drüsen kommt (s. u.) . Betrachtet man die Haut als größte hormonproduzierende Drüse des menschlichen Körpers mit nicht nur parakriner, sondern auch nachgewiesener endokriner Sekretionsfunktion, erscheint es gerechtfertigt, z. B. bei Vorliegen eines Typ-I-Diabetes mellitus und einer Vitiligo von einem APS-4 zu sprechen.
Die Diagnose einer Vitiligo wird primär klinisch gestellt. Die Therapie ist komplex und richtet sich gemäß der jüngst veröffentlichten europäischen Leitlinie nach dem Ausmaß der betroffenen Körperoberfläche . Bei limitiertem Befall (bis 10 % der Körperoberfläche) kommen je nach Lokalisation der Vitiligoherde topische Klasse-II-Kortikosteroide (Körperherde) bzw. Calcineurininhibitoren off-label (Gesicht) in Frage, für welche die größte therapeutische Evidenz basierend auf randomisiert kontrollierten Studien besteht. Bei ausgedehntem Befall ist eine Lichttherapie mit UVB-311 nm Mittel der Wahl, u. U. kombiniert mit systemischen Antioxidantien. Bei Nichtansprechen der obigen Therapien kann bei limitiertem Befall eine gezielte Lichttherapie mit dem 308 nm-Excimer-Laser oder der 308 nm-Excimer-Lampe durchgeführt werden. Chirurgische Maßnahmen kommen bei stabiler Erkrankung (keine Veränderungen der Depigmentierungsherde seit 1 Jahr) in Frage. Hier stehen verschiedene operative Verfahren zur Verfügung, insbesondere die autologe Melanozytentransplantation. Supportiv sollten ein UVA/B-Vollschutz und bedarfsweise eine Camouflage jedem Patienten empfohlen werden .
Hauterscheinungen bei Diabetes mellitus im Rahmen von Syndromen
Autoimmun polyglanduläre Syndrome
Insbesondere die Koinzidenz einer nicht-segmentalen Vitiligo und eines Diabetes mellitus sollte an ein APS denken lassen. Besonders beim APS-2 (Morbus Addison und Autoimmunthyreoiditis oder Diabetes mellitus Typ I sind zur Diagnosestellung obligat) und APS-3 findet man nicht selten eine Vitiligo oder andere autoimmun vermittelte Entzündungserkrankungen der Haut, die auf die gemeinsame Immunpathogenese hindeuten .
HAIR-AN-Syndrom
Bei Zeichen eines peripheren Hyperandrogenismus sollte bei Hautmanifestationen und Vorliegen eines Diabetes mellitus an ein HAIR-AN-Syndrom gedacht werden. Dieses Akronym steht für Hyperandrogenismus, Insulin-Resistenz und Acanthosis nigricans. Charakteristische Merkmale des peripheren Hyperandrogenismus der Haut sind eine schwere und therapierefraktäre Akne, androgenetische Alopezie, Seborrhoe und ein Hirsutismus. Therapeutisch kommen neben einer Gewichtsoptimierung, orale Antikontrazeptiva, Antiandrogene und in einigen Fällen Metformin in Frage .
Therapie-assoziierte Hauterscheinungen
Lipodystrophien an Injektionsstellen von Insulin
Fettgewebsatrophien an Insulininjektionsstellen können Monate bis Jahre nach Beginn der Injektionen auftreten. Mitunter sind sie deutlich entfernt von den eigentlichen Injektionsstellen (Abbildung ). Die Pathogenese dieser Therapiekomplikation ist unklar. Hinweise auf eine Autoimmunpathogenese könnten die Präsenz zirkulierender Insulinautoantikörper, Ablagerungen von IgM und C3 sowie das therapeutische Ansprechen auf topische Glukokortikoide sein . Oft bilden sich die Lipoatrophien spontan nach Jahren zurück, wenn die Injektionsstellen und Insulinart gewechselt werden. Bei ausgeprägtem Befund kann eine autologe Fettgewebstransplantation erwogen werden.
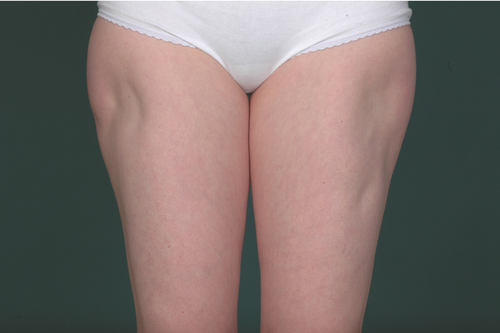
In seltenen Fällen kann es nach subkutanen Insulininjektion zu einer Hypertrophie des Fettgewebes kommen. Vermutet wird eine Stimulation subkutaner Adipozyten durch das injizierte Insulin. Durch Verminderung der systemischen Resorption des injizierten Insulins kann die medikamentöse Einstellung der diabetischen Stoffwechsellage problematisch werden. Auch daher sollte immer ein regelmäßiger Wechsel der subkutanen Injektionsstelle erfolgen .
Arzneimittelreaktionen auf Insulin oder orale Antidiabetika
Lokale allergische Reaktionen gegen Insulin oder sonstige Bestandteile der Injektionslösung (z. B. Konservierungsstoffe) sind an den subkutanen Injektionsstellen beschrieben . In seltenen Fällen kann es zu einer lebensbedrohlichen IgE-vermittelten anaphylaktischen Reaktion gegen Insulin kommen. Unter Einnahme von oralen Antidiabetika kann es ferner zu Arzneimittelexanthemen, Urticaria, Erythema exsudativum multiforme, Pruritus und Erythema nodosum kommen . Phototoxische und photoallergische Reaktionen sind ebenfalls beschrieben. Insbesondere Sulfonylharnstoffe der ersten Generation, welche strukturell mit Sulfonamiden verwandt sind, führen am häufigsten zu Exanthemen.
Interessenkonflikt
Keiner.
Literatur
Fragen zur Zertifizierung durch die DDG
- Welche Aussage ist falsch?
- Circa 30 % der Diabetiker haben im Laufe ihres Lebens assoziierte Hauterscheinungen.
- Die Prävalenz von Diabetes mellitus weltweit im Jahr 2010 war 6,4%.
- Das Granuloma anulare disseminatum ist mit einer erhöhten Mortalität verbunden.
- Einige der Hauterscheinungen bei Diabetes mellitus können vor der Manifestation der Erkrankung auftreten.
- Bestimmte diabetische Hautmanifestationen sind mit extrakutanen diabetischen Komplikationen wie Neuropathie und Angiopathie korreliert.
- Welche Aussage trifft nicht zu? Die Necrobiosis lipoidica …
- betrifft meistens die Streckseiten der unteren Extremitäten.
- führt bei circa 30 % der Patienten zu schmerzhaften Ulzera.
- wird aufgrund der klinisch sichtbaren Gelbfärbung der Haut den eosinophilen Dermatosen zugerechnet.
- kann mit topischen Steroiden und PUVA behandelt werden.
- zeigt typische histologische Veränderungen in der gesamten Dermis.
- Welche Aussage zum diabetischen Fußsyndrom trifft nicht zu?
- Circa 15–25 % der Diabetiker werden in ihrem Leben ein diabetisches Ulkus haben.
- Die Amputationsrate liegt bei 25 %.
- Die Morbidität beträgt 5 %.
- In der Pathogenese spielen Neuropathie, Angiopathie, das beeinträchtigte Immunsystem und Deformitäten des Fußskeletts wichtige Rollen.
- Meist geht dem diabetischen Fußsyndrom ein Bagatelltrauma voraus.
- Welche Angabe zum Prozedere bei der Diagnostik und Therapie des diabetischen Fußsyndroms ist falsch?
- Die Klassifikation erfolgt laut einer DDG-Leitlinie nach Wagner und Armstrong.
- Eine angiologische Diagnose gehört nicht zur Beurteilung des diabetischen Fußsyndroms, da Revaskularisierungsmaßnahmen laut Studien keinen Effekt auf das Risiko einer Amputation haben.
- Anpassung von orthopädischen Schuhen zur Entlastung von druckbelasteten Stellen und regelmäßige podologische Pflege gehören zu den unterstützenden Maßnahmen beim diabetischen Fußsyndrom.
- MRT ist der Goldstandard zur Diagnostik einer Osteomyelitis.
- Bei fehlenden operativen Revaskularisierungsmöglichkeiten können Infusionen mit Alprostadil oder Iloprost die akrale Durchblutung fördern.
- Welche Aussage zu infektiösen Erkrankungen bei Diabetes mellitus ist falsch?
- Sie sind mit einem fünffachen Komplikationsrisiko und einem vierfachen Hospitalisierungsrisiko assoziiert.
- Eine unbehandelte Interdigitalmykose dient oft als Eintrittspforte für Weichteilinfektionen wie Zellulitis und Erysipel.
- Meistens sind gramnegative Keime die Ursache einer nekrotisierenden Fasziitis.
- Die maligne externe Otitis wird durch Pseudomonas aeruginosa verursacht. Als Komplikation kann eine Meningitis auftreten.
- Rezidivierende bakterielle und mykotische Infekte der Haut sollten an einen Diabetes mellitus denken lassen.
- Welche Aussage zum diabetischen Pruritus trifft nicht zu?
- Lokalisierter Pruritus im Genitoanalbereich kommt sehr oft durch Candida-Spezies zustande.
- Die diabetische Neuropathie spielt eine wichtige pathogenetische Rolle.
- Gabapentin ist beim diabetischen Pruritus wirkungslos.
- Eine verminderte Nervenfaserdichte ist in Hautbiopsien von Patienten mit Diabetes beschrieben worden.
- Glimepirid und Metformin können Auslöser von Pruritus bei diabetischen Patienten sein.
- Welche Aussage zur Therapie-assoziierten Hauterscheinungen bei Diabetes ist zutreffend?
- Eine Lipohypertrophie an Insulin-Injektionsstellen hat keinen Einfluss auf die systemische Resorption von Insulin.
- Die IgE-vermittelte Hypersensitivität gegen Insulin ist eine seltene aber potenziell lebensbedrohliche Reaktion.
- Phototoxische und photoallergische Reaktionen sind am häufigsten mit Metformin beschrieben worden.
- Lokale Reaktionen an Injektionsstellen sind immer auf eine Insulinunverträglichkeit zurückzuführen.
- Fettgewebeatrophien sind eine Frühkomplikation der antidiabetischen Therapie.
- Welche Aussage zum Charcot-Fuß trifft nicht zu? Die wichtigsten Differenzialdiagnosen sind …
- Erysipel.
- tiefe Beinvenenthrombose.
- Gichtanfall.
- akute Ischämie.
- Zellulitis.
- Welche Angabe zur diabetischen Cheiroarthropathie ist nicht richtig?
- Sie sollte von einer Dupuytrenschen Kontraktur und systemischen Sklerodermie abgegrenzt werden.
- Betroffene Patienten weisen kein erhöhtes Risiko für eine diabetische Neuropathie und Angiopathie auf.
- Histologisch zeigen sich verdickte Kollagenfasern und Muzinablagerungen.
- Mittels Sonographie oder MRT kann eine Verdickung der periartikulären Weichteilstrukturen festgestellt werden.
- Akkumulation von AGEs und Aktivierung profibrotischer Signalwege scheinen eine pathogenetische Rolle zu spielen.
- Welche Aussage zum Scleroedema adultorum trifft nicht zu? Die Erkrankung kommt außer bei Diabetes mellitus noch gehäuft vor bei …
- Paraproteinämien.
- bakteriellen Infekten durch Streptokokken.
- rheumatoider Arthritis.
- viralen Infekten.
- multiplem Myelom.
Liebe Leserinnen und Leser,
der Einsendeschluss an die DDA für diese Ausgabe ist der 17. Oktober 2014.
Die richtige Lösung zum Thema „Die nichtsyndromalen lchthyosen – aktueller Stand“ in Heft 2 (Februar 2014) ist: (1b, 2c, 3b, 4e, 5d, 6c, 7b, 8c, 9b, 10b).
Die richtige Lösung zum Thema „Mykologie – ein Update. Teil 1: Dermatomykosen: Erreger, Epidemiologie und Pathogenese“ in Heft 3 (März 2014) ist: (1a, 2d, 3a, 4d, 5c, 6a, 7d, 8a, 9c, 10c).
Die richtige Lösung zum Thema „Lupus erythematodes. Teil II: Klinisches Bild, Diagnostik und Therapie“ in Heft 4 (April 2014) ist: (1b, 2d, 3c, 4e, 5b, 6b, 7c, 8b, 9d, 10d).
Bitte verwenden Sie für Ihre Einsendung das aktuelle Formblatt auf der folgenden Seite oder aber geben Sie Ihre Lösung online unter http://jddg.akademie-dda.de ein.




