Einblicke in die Mechanochemische Glasbildung von Zeolithischen Imidazolat-Gerüstverbindungen
Abstract
Gläser von metallorganischen Gerüstverbindungen (MOF-Gläser), die für ihr Potenzial bei der Gastrennung, in der Optik und als Festkörperelektrolyte bekannt sind, profitieren von der Verarbeitbarkeit ihres (unterkühlten) flüssigen Zustands. Traditionell werden MOF-Gläser durch Erhitzen von MOF-Kristallen über ihren Schmelzpunkt und anschließendes Abkühlen des flüssigen MOF auf Raumtemperatur unter einer inerten Atmosphäre hergestellt. Diese Technik des Schmelzquenchens ist zwar effektiv, erfordert aber aufgrund der hohen Temperaturen einen hohen Energieaufwand. Außerdem schränkt es den Spielraum für die Entwicklung neuer Materialien ein, da nur die thermisch hochstabilen Kombinationen von Metallionen und Linkern in Frage kommen. Eine Alternative, das mechanische Mahlen bei Raumtemperatur, hat sich als geeignet erwiesen, MOF-Kristalle in amorphe Phasen umzuwandeln. Die spezifischen Bedingungen, unter denen diese amorphen Phasen ein glasähnliches Verhalten zeigen, sind jedoch noch nicht bekannt. In dieser Studie untersuchen wir die mechanochemische Amorphisierung und Verglasung einer Vielzahl von zeolithischen Imidazolat-Gerüstverbindungen (ZIFs) mit verschiedenen Linkern und unterschiedlichen Metallionen (Zn2+, Co2+ und Cu2+) bei Raumtemperatur. Unsere Ergebnisse zeigen, dass ZIFs, die schmelzbar sind, durch Kugelmahlen erfolgreich in Gläser umgewandelt werden können. Bemerkenswerterweise können auch einige nicht schmelzbare ZIFs mit Hilfe der Kugelmahltechnik verglast werden, wie die Herstellung des ersten ZIF-Glases mit Cu2+-Ionen zeigt.
Einführung
Metallorganische Gerüstverbindungen (Metal–Organic Frameworks, MOFs) sind Hybridmaterialien, die aus Metallionen und organischen Liganden bestehen, die zu einem kontinuierlichen Netzwerk verbunden sind.1 Derzeit sind in der Literatur fast 100.000 kristalline MOFs beschrieben2 und viele von ihnen weisen ein großes Potenzial für Anwendungen in verschiedenen Bereichen auf. Neben den allgegenwärtigen kristallinen MOFs erfreuen sich flüssige3 und glasartige MOFs,4, 5 die als vierte Generation von Koordinationspolymeren (Coordination Polymers, CPs) kategorisiert werden,6 an steigender Aufmerksamkeit. In letzter Zeit hat das Interesse an glasartigen Materialien aufgrund der entsprechenden Vorteile bei der Verarbeitung und Formgebung dieser Materialien stark zugenommen. Die erleichterte Verarbeitbarkeit von und die Abwesenheit von Korngrenzen in isotropen flüssigen und glasartigen MOF-Phasen im Vergleich zu ihren kristallinen Verwandten eröffnen neue Wege für Anwendungen, die von der Gastrennung7 bis hin zur Festkörperionik8, 9 reichen. Darüber hinaus wurden MOF-Gläser als attraktive Materialien für die Verwendung als Leuchtstoffe10 und für die Lagerung radioaktiver Abfälle vorgeschlagen.11
Die Familie der zeolithischen Imidazolat-Gerüstverbindungen (Zeolitic Imidazolate Frameworks, ZIFs) stellt die am besten untersuchte Untergruppe der schmelzbaren und glasbildenden MOFs dar. ZIFs basieren auf tetraedrisch koordinierten Übergangsmetallionen (z. B. Zn2+ oder Co2+), die durch Imidazolat-Linker zu einem typischerweise dreidimensionalen Netzwerk verbunden sind.12 Interessanterweise bilden unter der Vielzahl an MOFs nur wenige ZIFs eine Schmelze, wenn sie unter einer inerten Atmosphäre erhitzt werden, bevor sie sich thermisch zersetzen.4, 13 Während des Schmelzens werden die Metall-Linker-Bindungen dynamisch gebrochen und neu gebildet, wodurch ZIF-Flüssigkeiten entstehen.3 Wenn die ZIF-Flüssigkeiten abgekühlt werden, verglasen sie und bilden schmelzgequenchte Gläser (Melt-Quenched Glasses, MQGs).14 In der Praxis erfordert das Schmelzen eines ZIF relativ hohe Temperaturen (in der Regel >400 °C) und damit einen erheblichen Energieverbrauch.4 Darüber hinaus schränkt die Notwendigkeit, ZIF-Gläser über die flüssige ZIF-Phase zu erhalten, die Auswahl der glasbildenden ZIFs drastisch ein, da viele der bei substituierten Imidazolat-Linkern verwendeten funktionellen Gruppen empfindlich gegenüber hohen Temperaturen sind (z. B. Halogenid-Substituenten oder Nitrogruppen12, 15). Der prototypische Glasbildner ZIF-4 zum Beispiel besitzt eine sehr hohe Schmelztemperatur von 590 °C,3, 16 was zu einem teilweise zersetzten MQG führt.4, 17
Das Kugelmahlen ist eine etablierte Technik zur Synthese von mikrokristallinen MOF-Pulvern. Bei dieser Methode wird in der Regel ein Metalloxid in einer Vibrationsmischmühle zusammen mit dem organischen Linker in seiner protonierten Form in Gegenwart einer kleinen Menge von Zusatzstoffen und Lösungsmittelmolekülen, welche als Templat fungieren, gemahlen.18-20 Im Gegensatz dazu führt das postsynthetische Kugelmahlen (Post-Synthetic Ball-Milling, PSBM) von MOF-Mikrokristallen, das ohne Lösungsmittel durchgeführt wird, zu einer schnellen Amorphisierung der Materialien. Die mechanische Einwirkung während des PSBM trägt dazu bei, koordinative Bindungen zu brechen und neu zu bilden, was letztlich zur Bildung amorpher Feststoffe führt.21 Für eine Reihe von dichten Koordinationspolymeren (CPs) und Netzwerken (CNs) auf der Grundlage von Triazolat-, Dicyanamid- oder Cyanid-Linkern wurde gezeigt, dass die durch PSBM erhaltenen amorphen Phasen einen Glasübergang aufweisen.22, 23 Bei ZIFs wurde gezeigt, dass verschiedene Methoden der mechanischen Störung24 das Schmelzen von ZIFs und die Glasbildung begünstigen. Zum Beispiel fördern die Anwendung von hohem hydrostatischem Druck25 oder hochfrequenter Vibration26 das Schmelzen von ZIFs (d. h. das dynamische Aufbrechen der Metall-Linker-Bindung). Frühere Forschungsarbeiten haben gezeigt, dass PSBM eine schnelle Amorphisierung von kristallinen ZIFs verursachen kann, darunter ZIF-4 (Zn(im)2; cag-Topologie; im−=Imidazolat), ZIF-zni (Zn(im)2 ; zni-Topologie) und ZIF-8 (Zn(mim)2; sod-Topologie; mim−=2-Methylimidazolat).27-30 Es ist jedoch unklar, ob die amorphisierten ZIFs ein glasartiges Verhalten aufweisen. Kürzlich wurde eine mechanochemische Synthese durch Kugelmahlen zur Herstellung von ZIF-62 (Zn(im)2−x(bim)x; cag-Topologie im kristallinen Zustand; bim−=Benzimidazolat) durch Reaktion von ZnO mit Imidazol und Benzimidazol in Gegenwart geringer Mengen von N,N-Dimethylformamid (DMF) eingesetzt.31, 32 Je nach Zusammensetzung der Reaktionsmischung war das gewonnene Material entweder kristallin (für 0.05≤x≤0.30) oder amorph (für 0.35≤x≤1).33 Interessanterweise zeigte das durch Kugelmahlen hergestellte amorphe ZIF-62 einen kalorimetrischen Glasübergang, was belegt, dass glasartiges ZIF-62 mechanochemisch bei Raumtemperatur hergestellt werden kann, indem die Konzentration von bim− in der Kugelmahlsynthese erhöht wird. Die Technik zur Herstellung eines ZIF-62-Glases durch Kugelmahlen mittels einer beträchtlichen Erhöhung des Anteils an sperrigen Linkern (d. h. 0,35≤x(bim)− ≤1) ist jedoch mit Einschränkungen verbunden, wie z. B. der Möglichkeit einer Porositätsblockade in den Gläsern und einem erheblichen Anstieg der Glasübergangstemperatur (Tg), was eine höhere Verarbeitungstemperatur erfordert.
Während das Kugelmahlen üblicherweise für die Synthese von kristallinen ZIFs oder deren Umwandlung in amorphe Zustände eingesetzt wird, ist die Möglichkeit, eine direkte Verglasung von ZIFs bei Raumtemperatur zu ermöglichen, noch unerforscht. In diesem Artikel berichten wir über eine detaillierte Studie über den Nutzen von lösungsmittelfreiem PSBM für die Verglasung von kristallinen ZIFs mit unterschiedlicher chemischer Zusammensetzung, Netzwerktopologie und Porosität bei Raumtemperatur (Abbildung 1). Um das Potenzial von PSBM für die ZIF-Glasbildung zu bewerten, untersuchen wir mehrere schmelzbare und glasbildende ZIFs17, 34, 35 (ZIF-4(Zn/Co), ZIF-zni(Zn/Co), ZIF-62(Zn/Co), ZIF-UC-5 und TIF-4), aber auch ZIFs, von denen bekannt ist, dass sie in reiner Form nicht schmelzen (ZIF-7636 und ZIF-84, 37) und ZIFs, die bisher nicht im Hinblick auf die Glasbildung untersucht wurden (ZIF-7012 und ZIF-Cu-1 (Cu(im))238) (Abbildung 2). Diese Materialien umfassen Vertreter mit den für ZIFs typischen tetraedrischen Baueinheiten Zn2+ und Co2+ sowie einen ZIF auf der Basis von Cu2+ mit drastisch abgeflachten pseudo-tetraedrischen Einheiten. Es ist wichtig anzumerken, dass ZIFs auf der Basis von Cu2+ bisher nicht im Hinblick auf das Schmelzen und die Glasbildung untersucht worden sind. Röntgenpulverdiffraktometrie (XRPD), Differential-Scanning-Kalorimetrie (DSC), simultane thermogravimetrische und differentielle thermische Analysen (TG/DTA), Röntgentotalstreuung und daraus abgeleitete Paarverteilungsfunktionen (PDFs), Rasterelektronenmikroskopie (REM) und CO2-Gassorptionsmessungen liefern wichtige Einblicke in die thermischen und strukturellen Eigenschaften der ZIFs nach unterschiedlichen PSBM-Zeiten (zwischen 5 und 60 min). Wir stellen fest, dass PSBM mehrere dieser ZIFs in Gläser (MIGs=milling-induced glasses) umwandelt, was durch die Herstellung des ersten ZIF-Glases mit Cu2+-Baueinheiten hervorgehoben wird, während andere ZIFs zwar amorphisieren, aber kein glasartiges Verhalten zeigen. Unsere Ergebnisse bieten einen ersten Anhaltspunkt für die Herstellung von ZIF-Gläsern durch mechanisches Mahlen bei Raumtemperatur, zeigen aber auch einige Grenzen der Methode auf.

Schematische Darstellung des traditionellen Weges zur ZIF-Glas-Herstellung (rote Linie) und des in dieser Arbeit verfolgten mechanochemischen Verglasungsansatzes (blaue Linie).
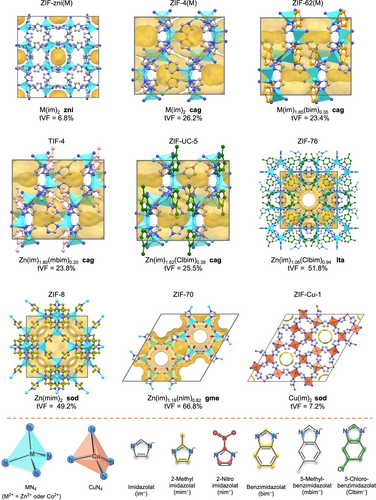
Kristallstrukturen (oben) und Baueinheiten (unten) der in dieser Arbeit untersuchten ZIFs. ZIF-zni (CCDC-Code IMIDZB) entlang der kristallographischen c-Achse betrachtet, ZIF-4 (CCDC-Code IMIDZB11), ZIF-62 (CCDC-Code SIWJAM), TIF-4 (CCDC-Code QOSYAZ) und ZIF-UC-5 (CCDC-Code GULVIV) entlang der kristallographischen b-Achse betrachtet. ZIF-76 (CCDC-Code GITWEM) und ZIF-8 (CCDC-Code FAWCEN03) entlang der kristallographischen a-Achse betrachtet. ZIF-70 (CCDC-Code GITVEL) und ZIF-Cu-1 (CCDC-Code CUIMDZ01) entlang der kristallografischen c-Achse betrachtet. Die Wasserstoffatome sind aus Gründen der Übersichtlichkeit weggelassen. Die theoretischen Porenanteile (tVFs) wurden mit der Mercury-Software bei einem Sondenradius von 1.6 Å und einem Gitterabstand von 0.2 Å berechnet und sind blassgelb dargestellt. Vor der Berechnung der tVFs wurden Lösungsmittelmoleküle entfernt und Linker-Fehlordnung so weit wie möglich aufgelöst, ohne die Raumgruppensymmetrie zu verändern. Wenn H-Atome in den angegebenen Kristallstrukturen nicht enthalten waren, wurden sie vor der Berechnung der tVF an geometrischen Positionen positioniert. Die Zusammensetzungen der ZIFs wurden durch 1H NMR-Spektroskopie von in Säure aufgelösten Proben ermittelt.
Ergebnisse und Diskussion
Synthese und Strukturelle Charakterisierung der Kristallinen ZIFs
Zwölf verschiedene kristalline ZIFs wurden durch Anpassung etablierter solvothermaler Reaktionsverfahren synthetisiert (siehe Hintergrundinformationen, Abschnitt 1).12, 36, 38, 39 Unter diesen wurden ZIF-4(M), ZIF-zni(M) und ZIF-62(M) entweder mit Zn2+ oder Co2+ als Metallzentren hergestellt (M2+), während TIF-4, ZIF-UC-5, ZIF-76, ZIF-8 und ZIF-70 Zn2+ als anorganische Baueinheit verwenden und ZIF-Cu-1 mit Cu2+ als Metallzentrum hergestellt wurde (Abbildung 2). Die ZIFs umfassen eine Vielzahl von funktionalisierten Linkern sowie Netzwerktopologien mit unterschiedlichen Porositäten. Die theoretischen Porenanteile (theoretical Void Fractions, tVFs) der ZIFs, die auf der Grundlage der bereits publizierten Kristallstrukturen berechnet wurden, reichen von etwa 7 % (ZIF-zni und ZIF-Cu-1) bis zu etwa 67 % (ZIF-70). Nach dem Waschen und dem Lösungsmittelaustausch wurden die desolvatisierten Zn- und Co-ZIF-Materialien durch 6-stündiges Erhitzen auf 170 °C unter dynamischem Vakuum gewonnen, während ZIF-Cu-1 wegen seiner niedrigeren Zersetzungstemperatur bei 110 °C aktiviert wurde. Die Identität und Reinheit der kristallinen ZIFs wurde durch strukturlose Profilanpassungen (Pawley-Methode) von Röntgenpulverdiffraktogrammen unter Verwendung von Referenzdaten aus der Literatur überprüft (Abbildungen S1–12, Tabelle S3). Alle Verbindungen sind phasenrein, mit Ausnahme von ZIF-UC-5, das nach einer zweiphasigen Rietveld-Verfeinerung etwa 5 wt % ZIF-76 als parasitäre Phase enthält (Abbildung S7). Die letztgenannte Probe wird daher als ZIF-76/UC-5 bezeichnet. Die vollständige Entfernung der Lösungsmittel aus den Poren der ZIFs wurde durch die Daten der 1H-Kernspinresonanz (1H NMR) und der Fourier-Transformations-Infrarot-Spektroskopie (FTIR) nachgewiesen (siehe Hintergrundinformationen, Abschnitt 3–4). Die 1H NMR -Spektroskopie von säureaufgeschlossenen Proben wurde durchgeführt, um die Linker-Verhältnisse der Mischlinker-Materialien ZIF-62(M), TIF-4, ZIF-70, ZIF-76 und ZIF-76/UC-5 zu bestimmen, was zu den in Abbildung 2 (Abbildungen S35–36 und S41–44) genannten chemischen Zusammensetzungen führt.
Amorphisierung durch Postsynthetisches Kugelmahlen
Die aktivierten mikrokristallinen ZIF wurden mit PSBM bei 25 Hz in einer Schwingmühle für 5, 10 bzw. 15 Minuten behandelt, wobei ein 10-mL-Mahlbecher aus Edelstahl mit zwei 8-mm-Edelstahlkugeln und ca. 50 mg ZIF verwendet wurde. Die gewonnenen PSBM-Materialien werden mit ZIF-X-5min/10min/15min entsprechend der PSBM-Zeit bezeichnet. Für ZIF-8 wurden zusätzlich 30 min und 60 min kugelgemahlene Proben hergestellt (ZIF-8-30min und ZIF-8-60min). Die Röntgenpulverdiffraktogramme fast aller kugelgemahlenen ZIFs zeigen bereits nach 5 Minuten PSBM nur diffuse Streuung ohne scharfe Bragg-Reflexe, was eine schnelle Amorphisierung der Materialien belegt (Abbildungen 3 und S14–20). Die einzige Ausnahme bilden die ZIF-zni(M)-Proben, die nach 5 Minuten PSBM immer noch Reflexe aufweisen, die der kristallinen ZIF-zni-Phase zuzuordnen sind, auch wenn die Intensität der Reflexe abnimmt und die Peakbreite zunimmt (Abbildungen 3 und S16). Mit zunehmender PSBM-Zeit nehmen die Bragg-Reflexe der ZIF-zni-Phasen weiter an Intensität ab, aber die Proben sind nach 15 Minuten PSBM immer noch nicht vollständig amorphisiert. Die Restkristallinität der ZIF-zni(Zn)-Proben wurde durch Profilanpassung der XRPD-Daten geschätzt (Abbildungen S21–24). Es ist zu beobachten, dass innerhalb der ersten 10 Minuten PSBM der Kristallinitätsgrad der Probe auf 49 % reduziert wird, während nach 15 Minuten PSBM ein Kristallinitätsgrad von 36 % verbleibt. Die höhere Beständigkeit von ZIF-zni gegenüber der Amorphisierung durch PSBM lässt sich durch die höhere Dichte von ZIF-zni (ρ=1.56 g cm−3)40 im Vergleich zu den anderen hier untersuchten ZIFs auf Zn- und Co-Basis (0.78 g cm−3≤ρ≤1.32 g cm−3)17 erklären, da bekanntlich eine höhere Dichte mit einem höheren Elastizitätsmodul und einer höheren Härte korreliert.41
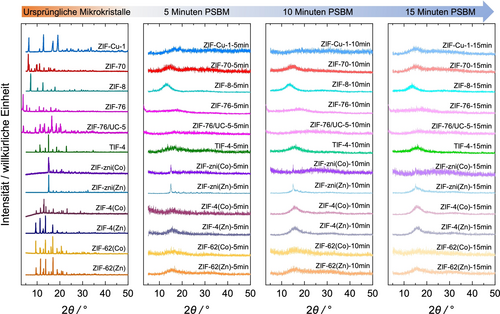
Röntgenpulverdiffraktogramme der unbehandelten polykristallinen ZIF-Materialien und nach 5, 10 und 15 Minuten PSBM.
In Übereinstimmung mit früheren Strukturuntersuchungen von amorphisierten ZIFs27, 42 zeigen die aus Röntgentotalstreuungsdaten abgeleiteten PDFs ausgewählter unbehandelter und 5-minütig kugelgemahlener ZIF-Proben, dass die lokale Struktur (<6 Å) der kristallinen Phase (d. h. Metallionen, die von vier Imidazolat-basierten Linkern umgeben sind) in den amorphen PSBM-Proben erhalten bleibt (Abbildungen S30–34). Daher sind die PDFs der amorphen PSBM ZIFs weitgehend identisch mit denen der aus der Literatur bekannten ZIF-MQGs. Im Einklang mit dem Verlust der langreichweitigen Ordnung sind die erhöhte strukturelle Heterogenität und Verzerrungen in den kugelgemahlenen ZIFs an der Verbreiterung verschiedener Schwingungsbanden in den FTIR-Spektren im Vergleich zu den Banden der kristallinen Ausgangsmaterialien erkennbar (Abbildungen S47–58). Insbesondere die asymmetrischen Streckschwingungsbanden der MN4-Polyeder (M2+=Zn2+, Co2+, Cu2+), die sich bei ca. 300 cm−1 in den Fern-IR-Spektren befinden, weisen in den PSBM-Proben im Vergleich zu ihren kristallinen Gegenstücken deutlich breitere Profile auf, die bereits 5 Minuten nach dem Kugelmahlprozess zu beobachten sind. Diese Banden spiegeln die Breite der entsprechenden MN4 -Schwingungen der MQG-Referenzproben wider (Abbildungen S59–67 und Tabelle S4). Eine Ausnahme ist wiederum bei ZIF-zni(Zn) zu beobachten, das eine allmähliche Verbreiterung im Laufe des PSBM-Prozesses aufweist, was mit der oben beschriebenen allmählichen Abnahme der Kristallinität übereinstimmt. REM-Bilder zeigen, dass die solvothermal synthetisierten ZIFs, die zunächst durch große Kristalle (bis zu mehreren hundert Mikrometern Größe) gekennzeichnet sind, nach einer 5-minütigen PSBM-Behandlung eine deutliche Fragmentierung in kleinere Partikel von 1 bis 10 μm Größe erfahren (Abbildungen S106–108 und Tabelle S10). Längere Kugelmahlzeiten führen nur zu einer geringfügigen weiteren Verringerung der Partikelgröße.
CO2 Physisorptionsdaten und Porositätsanalyse
Da festgestellt wurde, dass N2 bei 77 K in einigen der hier untersuchten ZIFs kaum adsorbiert wird,13, 17, 43 wurde die Entwicklung der Porosität der ZIFs mit der PSBM-Zeit durch isotherme CO2-Sorption bei 195 K untersucht (Abbildungen S68–75 und Tabelle S5). CO2 hat einen kleineren kinetischen Durchmesser als N2 und kann in sehr enge Mikroporen eindringen.17 Der maximale Gasdruck, der für die Datenerfassung verwendet wurde, beträgt 95 kPa, was einem relativen Druck p/p0 von etwa 0.50 entspricht und die vollständige Füllung der Mikroporen der Materialien gewährleistet. Die maximalen CO2-Kapazitäten bei 95 kPa ( ) aller untersuchten ZIFs nehmen mit zunehmender PSBM-Zeit progressiv ab, mit Ausnahme von ZIF-zni(Zn) (Abbildung 4a). Die verringerten CO2 Kapazitäten deuten darauf hin, dass sich die Materialien während der PSBM-induzierten Amorphisierung verdichten. Wie erwartet nimmt die Verdichtungsrate mit zunehmender Mahldauer ab, was darauf hindeutet, dass die wichtigsten strukturellen Veränderungen, während der Amorphisierung in den ersten Minuten des Mahlens auftreten. Die poröseren ZIFs (d. h. ZIF-4(M), ZIF-8 und ZIF-76) weisen mit zunehmender Mahldauer eine stärkere Verdichtung auf (stärkerer Verlust an Porosität) als das weniger poröse ZIF-62(M) (Abbildung 4b). Dies steht im Einklang mit den größeren Kompressionsmodulen und der höheren mechanischen Festigkeit von ZIF-62(M) im Vergleich zum isoretikularen, aber poröseren ZIF-4(M).44 Überraschenderweise nimmt die Porosität von ZIF-zni(Zn) mit PSBM zu. erreicht nach 10 Minuten PSBM 181 % der Kapazität des ursprünglichen ZIFs und pendelt sich nach 15 Minuten PSBM bei 171 % der ursprünglichen Kapazität ein. Dieses ungewöhnliche Verhalten ist wahrscheinlich darauf zurückzuführen, dass die zni-Topologie eine der dichtesten bekannten ZIF-Topologien ist und die Zunahme der Unordnung durch PSBM zu einer Erhöhung der Porosität führt.45
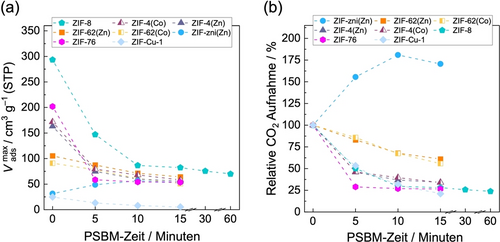
(a) Absolute CO2-Aufnahme ( ), gemessen bei 195 K, 95 kPa und (b) die entsprechende relative CO2-Aufnahme ( ) als Funktion der PSBM-Zeit der untersuchten ZIF-Proben. Die Linien sind nur eine Orientierungshilfe.
Mit Ausnahme von ZIF-8 und ZIF-Cu-1 ist die CO2-Kapazität für die mit 15 min PSBM behandelten Proben sehr ähnlich, was bedeutet, dass diese Materialien amorphe MOFs mit ähnlicher Porosität und Dichte bilden. Bemerkenswert ist, dass die CO2-Kapazitäten bei 95 kPa im Bereich von 50 bis 65 cm3 g−1 (STP) liegen, was den CO2-Kapazitäten der MQGs von ZIF-4, ZIF-62 und TIF-4 sehr ähnlich ist, die unter den gleichen Bedingungen bestimmt wurden.17 ZIF-8 ist resistenter gegenüber einem Gerüstkollaps als die anderen ZIFs, sodass nach 15 min PSBM eine wesentlich höhere Porosität beobachtet wird =82 cm3 g−1 ). Selbst nach 60 Minuten PSBM hat amorphisiertes ZIF-8 eine wesentlich höhere Sorptionskapazität als die anderen ZIFs, die nur 15 Minuten PSBM ausgesetzt waren =70 cm3 g−1). Wir vermuten, dass die Methylgruppen an Position 2 des mim−-Linkers der Grund für die Bildung einer offeneren amorphen Gerüststruktur im Falle des kugelgemahlenen ZIF-8 im Vergleich zu den anderen ZIFs sein könnten, die Linker verwenden, die an Position 2 nicht substituiert sind.43
ZIF-Cu-1 unterscheidet sich stark von allen anderen hier untersuchten Materialien. Wie aufgrund seines niedrigen tVF zu erwarten, liegt die gravimetrische CO2-Kapazität =25 cm3 g−1 (STP)) des kristallinen ZIF-Cu-1 im Bereich der Kapazität des kristallinen ZIF-zni ( =31 cm g3−1 (STP)). Im Gegensatz zu ZIF-zni(Zn) erhöht das Mahlen die Porosität von ZIF-Cu-1 nicht, sondern verdichtet das Material allmählich, so dass nach 15 min PSBM nur noch etwa 5 cm3 g−1 (STP) beträgt, wodurch das amorphe ZIF-Cu-1-15min im Wesentlichen porenfrei wird. Da ZIF-zni(Zn) und ZIF-Cu-1 beide die gleichen Linker enthalten, kann der drastische Unterschied in der mahlbedingten strukturellen Entwicklung zwischen diesen beiden Materialien auf ihre anorganischen Bausteine zurückgeführt werden. Die fast perfekt tetraedrischen Zn2+ Zentren von ZIF-zni(Zn) (Geometrieindex τ4=0.97 und 0.95 für die beiden kristallographisch unabhängigen Zn2+ Ionen; τ4=1 für tetraedrisch und τ4=0 für quadratisch planar46) scheinen eine lockerere Packung der Baueinheiten in den amorphen Gerüsten zu ermöglichen, verglichen mit dem stark abgeflachten pseudo-tetraedrischen Cu2+ in ZIF-Cu-1 (τ4=0,47; Abbildung 5).
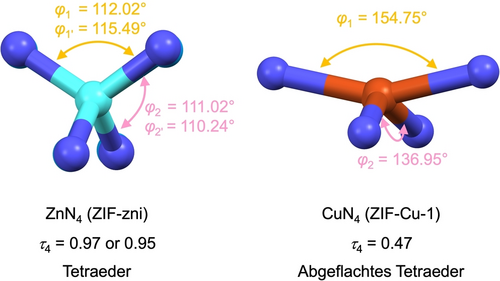
Koordinationsumgebung von Zn2+ in ZIF-zni (links, CCDC-Code IMIDZB) und Cu2+ in ZIF-Cu-1 (rechts, CCDC-Code CUIMDZ01). Die beiden größten N−M-N-Winkel (ϕ1 und ϕ2), die zur Berechnung des Geometrieindex (τ4) verwendet werden, sind in beiden Diagrammen dargestellt. Man beachte, dass ZIF-zni zwei kristallographisch unabhängige Zn2+-Ionen mit leicht unterschiedlichen Winkeln aufweist.
Thermische Eigenschaften
Zur Untersuchung der thermischen Stabilität und möglicher Phasen-/Glasübergänge der unbehandelten ZIFs und der entsprechenden PSBM-Proben wurden gleichzeitig thermogravimetrische und differentielle thermische Analysen (TG/DTA) zwischen 40 und 800 °C unter N2-Atmosphäre durchgeführt (Abbildungen S76–87). Die Zersetzungstemperatur (Td) aller ZIFs nimmt im Allgemeinen mit zunehmender PSBM-Zeit leicht ab (Tabelle S8). Die verringerte thermische Stabilität könnte auf erhöhte Defektkonzentrationen und ungünstige strukturelle Verzerrungen durch PSBM zurückzuführen sein.
Um die Proben auf thermische Phasenänderungen zu untersuchen, wurden zusätzliche zyklische DSC-Experimente (zwei Heizscans, ein Kühlscan) zwischen Umgebungstemperatur und Td unter N2-Atmosphäre durchgeführt (Abbildungen 6, S88–91 und S99). Interessanterweise zeigen die ZIFs, die als Glasbildner bekannt sind (ZIF-62(M), ZIF-4(M), ZIF-zni(Zn), ZIF-76/UC-5 und TIF-4), bereits im ersten Heizscan der DSC ein wohldefiniertes Glasübergangssignal nach nur 5 Minuten PSBM (Abbildungen 6 und S88). Diese PSBM-amorphisierten Materialien stellen also ZIF-MIGs dar, die beim Erhitzen in eine unterkühlte Flüssigkeit übergehen.47 Dies beweist, dass die Verglasung dieser Verbindungen durch Kugelmahlen bei Raumtemperatur statt durch Erhitzen über den Schmelzpunkt der Materialien und anschließendes Schmelzquenchen erreicht werden kann. Wir vermuten, dass die mechanische Energie, die durch Kompression und Scherung erzeugt wird, zusammen mit potenziellen momentanen Temperatur-Hotspots, den Glasbildungsprozess durch PSBM erreicht.48, 49 Bemerkenswert ist, dass die Tg-Werte der MIGs niedriger sind als die Tg-Werte der entsprechenden Gläser, die mit konventionellen Schmelzquenchmethoden (MQGs) hergestellt wurden. Interessanterweise nehmen die Tg-Werte der MIGs mit zunehmender PSBM-Zeit weiter ab, was durch eine zunehmende Anzahl von Strukturdefekten (z. B. unterkoordinierte Zn2+-Ionen, Linker mit nicht-abgesättigten Bindungen) bei längeren Mahlzeiten erklärt werden kann (Abbildungen 6 und S88).22, 50 Die niedrigeren Tg-Werte der MIGs deuten darauf hin, dass diese Gläser bei einer niedrigeren Temperatur als die entsprechenden MQGs geformt und prozessiert werden können. Außerdem gehen die MIGs bei Tg in den unterkühlten flüssigen Zustand über, während die MQGs erst durch Erhitzen der kristallinen Vorstufen auf den höheren Schmelzpunkt (Tm) erhalten werden müssen.
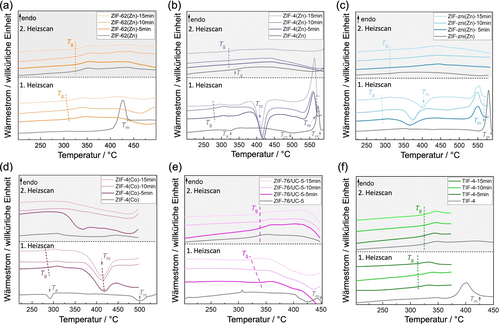
Erste und zweite Heizscans von DSC-Messungen von (a) ZIF-62(Zn), (b) ZIF-4(Zn), (c) ZIF-zni(Zn), (d) ZIF-4(Co), (e) ZIF-76/UC-5, (f) TIF-4 und den entsprechenden Proben nach 5, 10 und 15 Minuten PSBM. Die Heizrate für alle Messungen betrug +10 °C min−1. Die farbigen Pfeile und gestrichelten Linien zeigen die Amorphisierungstemperatur (Ta), die Glasübergangstemperatur (Tg), die Rekristallisationstemperatur (Trc) und die Schmelztemperatur (Tm) der ZIFs. Die grauen Bereiche stellen die zweiten Heizscans dar.
Beim zweiten DSC-Heizscan der MIGs konvergieren die Tg-Werte mit den für die entsprechenden MQGs bekannten Werten. Dies ist wahrscheinlich darauf zurückzuführen, dass die meisten der durch PSBM entstandenen Strukturdefekte durch thermische Relaxation im unterkühlten flüssigen Zustand repariert werden. Breite exotherme Merkmale in den DSC-Thermogrammen der ersten Heizscans der PSBM-Proben von ZIF-62(Zn) bei Temperaturen zwischen 400 °C und 500 °C unterstützen diese Schlussfolgerung.
Die DSC-Daten von ZIF-4(Zn/Co) und ZIF-zni(Zn/Co) weisen unterschiedliche thermische Eigenschaften auf (Abbildung 6b und c). Ähnlich wie kristallines ZIF-4(Zn), das nach der thermischen Amorphisierung zu ZIF-zni(Zn) rekristallisiert, rekristallisieren auch die MIGs ZIF-4(Zn)-5min, -10min und -15min nach dem Durchschreiten des Glasübergangs zum ZIF-zni(Zn)-Polymorph (bestätigt durch XRPD bei variabler Temperatur, Abbildungen S27–29). Interessanterweise nehmen die Rekristallisationstemperatur (Trc) und die entsprechende Enthalpie (ΔHrc) mit zunehmender Mahldauer leicht ab (Tabellen S8–S9). Die aus ZIF-zni(Zn) erhaltenen PSBM-Proben rekristallisieren nach dem Durchschreiten des Glasübergangs ebenfalls in dieselbe Phase; hier steigen jedoch Trc und ΔHrc mit der Mahldauer an. Diese thermischen Abweichungen stimmen mit den mahlbedingten Veränderungen der Porosität und Dichte überein, wobei ZIF-zni(Zn) eine Zunahme der Porosität und eine Abnahme der Dichte beim Mahlen erfährt, während ZIF-4(Zn) den entgegengesetzten Trend zeigt. Außerdem amorphisiert ZIF-zni(Zn) auch nach 15 Minuten PSBM nicht vollständig. Folglich unterstützen die verbleibenden kristallinen Partikel der ZIF-zni-Phase in den kugelgemahlenen Materialien die Rekristallisation, da diese als Kristallisationskeime dienen, wenn sie erhöhten Temperaturen ausgesetzt werden.
Generell kann festgestellt werden, dass das ΔHrc für alle kugelgemahlenen ZIF-4(Zn) und ZIF-zni(Zn) Materialien (ΔHrc=−7.2 bis–10.2 kJ mol−1) etwas kleiner ist als das des unbehandelten ZIF-4(Zn) (ΔHrc=−10.6 kJ mol−1). Dieser Befund deutet auf eine unvollständige Rekristallisation in den PSBM-Proben hin, so dass ein erheblicher Anteil der amorphen Phase verbleibt. Diese Hypothese wird durch die Beobachtung gestützt, dass die Schmelzenthalpie (ΔHm) der rekristallisierten ZIF-zni(Zn)-Phasen aus den PSBM-Materialien (ΔHm=5.0 bis 7.7 kJ mol−1) ca. 35 % bis 58 % niedriger ist als die von reinem ZIF-zni(Zn) (ΔHm=11.9 kJ mol−1). Dementsprechend weisen diese rekristallisierten Phasen der PSBM-Materialien auch wesentlich niedrigere Schmelztemperaturen (Tm=570 °C und 565 °C) im Vergleich zu den unbehandelten Materialien auf (Tm≥581 °C). Die niedrigeren Tm und ΔHm der PSBM-Proben lassen sich auf die Präsenz einer beträchtlichen Menge amorpher Restanteile, eine höhere Konzentration struktureller Defekte in den rekristallisierten Phasen und die durch PSBM bedingten kleineren Partikelgrößen zurückführen (Abbildungen S107–108).51-53 Bemerkenswert ist, dass ähnliche Variationen des Glasübergangs und des Rekristallisationsverhaltens für die Co2+-Derivate ZIF-4(Co) und ZIF-zni(Co) beobachtet werden, auch wenn die durch Rekristallisation entstandenen ZIF-zni(Co)-Phasen sich thermisch zersetzen, bevor sie schmelzen (Abbildungen 6d und S89).34, 54
Interessanterweise zeigen die PSBM-Proben von phasenreinem ZIF-76 in den ersten DSC-Heizscans deutliche Tg Signale zwischen 278 °C (15 min PSBM) und 347 °C (5 min PSBM) (Abbildung 7). Ähnlich dem Verhalten, das für die anderen zuvor besprochenen ZIF-Glasbildner beobachtet wurde, konvergiert Tg in den zweiten Heizscans aufgrund der thermischen Relaxation während des ersten Heiz-Kühl-Zyklus auf 357 °C. Man beachte, dass der glasartige Zustand von ZIF-76 mit der Schmelzquenchtechnik nicht erreicht werden kann, wenn das Material in phasenreiner Form vorliegt, da die ZIF-76-Mikrokristalle ihre Zersetzungstemperatur (Td) erreichen, bevor sie schmelzen können (Abbildung S83).36 Folglich kann ZIF-76 nur in einem Flussmittel aus schmelzbarem ZIF, wie dem chemisch ähnlichen, aber topologisch unterschiedlichen ZIF-UC-5, geschmolzen werden.36, 55, 56 Die Unfähigkeit des phasenreinen ZIF-76 zu schmelzen kann auf seine wesentlich höhere Porosität im Vergleich zu den ZIFs mit cag- oder zni-Topologie zurückgeführt werden, was zu einer erhöhten Aktivierungsenergie für die Dissoziation der Metall-Linker-Bindung führt.37 Die starke Verdichtung, die ZIF-76 während des PSBM erfährt (Abbildung 4a), scheint der Schlüssel zur Beobachtung des glasartigen Verhaltens und der Bildung eines unterkühlten flüssigen Zustands bei erhöhten Temperaturen zu sein. Diese Entwicklung ist vorteilhaft, da sie die Palette der chemischen Zusammensetzungen von ZIF-Gläsern erweitert. Bemerkenswert ist, dass der Anteil des sperrigen Linkers Clbim− in ZIF-76 etwa 50 % ausmacht, während er in ZIF-UC-5 nur etwa 20 % beträgt. Dies ist von Bedeutung, da der Anteil des sperrigen Linkers in ZIF-Gläsern nachweislich wichtige Materialeigenschaften beeinflusst, darunter die Viskosität der ZIF-Flüssigkeiten und die Gassorptionsselektivität der entsprechenden Gläser.17, 39

Erster und zweiter Heizscan von DSC-Messungen von phasenreinem ZIF-76 und den entsprechenden Proben nach 5, 10 und 15 Minuten PSBM. Die Heizrate für alle Messungen betrug +10 °C min−1. Die Grafik auf der rechten Seite dient zur Hervorhebung der Glasübergangssignale.
Motiviert durch die Feststellung, dass das nicht schmelzende ZIF-76 durch PSBM in ein Glas umgewandelt werden kann, haben wir auch die thermischen Eigenschaften von ZIF-8, ZIF-70 und ZIF-Cu-1 untersucht. Wir wollten herausfinden, ob auch bei diesen ZIFs nach einer PSBM-Behandlung Glasübergänge beobachtet und unterkühlte flüssige Zustände erreicht werden können. Das kristalline ZIF-8 wurde bereits aus experimenteller und theoretischer Sicht auf sein Schmelzverhalten hin untersucht,4, 37 während das thermische Phasenverhalten von ZIF-70 und ZIF-Cu-1 noch unerforscht ist.
Es wurde festgestellt, dass kristallines ZIF-8 bei erhöhten Temperaturen nicht schmilzt, was durch die stärkere Zn−N-Bindung des mim−-Linkers im Vergleich zum nicht substituierten im−-Linker sowie durch die größere Aktivierungsenergie für das Brechen der Zn−N-Bindung aufgrund der großen Porosität von ZIF-8 erklärt werden kann.4, 37, 43 In Übereinstimmung mit diesen Tatsachen weist keine der kugelgemahlenen ZIF-8-Proben einen kalorimetrischen Glasübergang auf, obwohl die amorphen ZIF-Materialien eine recht hohe thermische Stabilität (Td >486 °C) besitzen (Abbildungen S85 und S90). Es wird deutlich, dass die verdichteten amorphen ZIF-8-Phasen, die aus PSBM resultieren, nicht die dynamische Dissoziation und Assoziation von Zn−N-Bindungen durchlaufen, die für den Übergang von einem Glas zu einer unterkühlten Flüssigkeit erforderlich sind. Diese Beobachtung unterstreicht die entscheidende Rolle, die der nicht substituierte und kleinere im−-Linker spielt, welcher ein integraler Baustein aller berichteten glasbildenden ZIFs ist.
ZIF-70 besitzt eine chemische Zusammensetzung mit etwa 59 % des kleinen Linkers im− und etwa 41 % des sperrigeren Linkers nim−. Die TG/DTA-Analyse zeigt, dass kristallines ZIF-70 eine niedrige Td von 325 °C hat. Im Gegensatz zu allen anderen in dieser Arbeit untersuchten ZIFs zeigt ZIF-70 eine stark exotherme Zersetzung, was mit der geringen thermischen Stabilität des nim−-Linkers in Verbindung gebracht werden kann. Im DSC-Thermogramm kann vor der exothermen Zersetzung kein Schmelzsignal beobachtet werden. Der recht große Anteil der im−-Linker deutet jedoch darauf hin, dass das Material ähnlich wie ZIF-76 Potenzial zur Glasbildung durch PSBM hat. Dennoch zeigen auch die durch PSBM erhaltenen amorphen ZIF-70-Derivate eine stark exotherme Zersetzung, die bereits bei etwa 300 °C beginnt (Abbildung S86). Diese geringe thermische Stabilität des amorphen ZIF-70 führt dazu, dass es in der DSC-Analyse kein Glasübergangssignal zeigen kann, da Tg oberhalb von 300 °C zu erwarten wäre (Abbildung S91). Somit zeigt das amorphisierte und verdichtete ZIF-70 keine glasartigen Eigenschaften, was vermutlich auf seine geringe thermische Stabilität zurückzuführen ist.
Unseres Wissens nach sind die thermischen Eigenschaften des auf Cu2+-basierenden ZIF-Cu-1 noch nicht untersucht worden, obwohl über das Material mit sod-Topologie bereits vor mehr als 20 Jahren berichtet wurde.38 TG/DTA-Experimente zeigen, dass kristallines ZIF-Cu-1 einen zweistufigen Zersetzungsprozess durchläuft, wobei der erste Schritt erst bei 258 °C beginnt (Abbildung 8a). Daher ist Td von ZIF-Cu-1 im Vergleich zu den zuvor diskutierten ZIFs auf Basis von Zn2+ und Co2+ viel niedriger. Die Wärmeflusskurve beim ersten Zersetzungsschritt ist stark endotherm. Das Erhitzen von ZIF-Cu-1 kurz nach dem ersten Zersetzungsschritt bei 270 °C und das anschließende Abkühlen des Materials auf Raumtemperatur führt zu einem dunkel gefärbten, glasartigen Material, das beim Wiedererhitzen einen Glasübergang mit einer Tg von 172 °C aufweist (Abbildung S99). Die Beobachtung, dass die Partikel des ursprünglichen mikrokristallinen ZIF-Cu-1 zu einer millimetergroßen glasartigen Struktur verschmelzen, deutet darauf hin, dass ZIF-Cu-1 bei etwa 258 °C schmilzt und sich parallel dazu zersetzt. Da der Gewichtsverlust beim ersten Zersetzungsschritt etwa 22 % beträgt, weist die glasartige Phase von ZIF-Cu-1, die durch Schmelzquenchen gewonnen wird, starke Zersetzung auf. Interessanterweise zeigen die durch PSBM amorphisierten ZIF-Cu-1-Proben in DSC-Experimenten Glasübergangstemperaturen zwischen 166 °C und 170 °C, was sie als MIGs klassifiziert. Im Gegensatz zu den MIGs auf Zn- und Co-Basis zeigen die ZIF-Cu-1-Proben, die für 5–15 min bearbeitet wurden, einen leichten Anstieg von Tg bei längerer PSBM-Dauer. Dieses besondere Verhalten könnte auf die besondere Koordinationschemie von Cu2+ zurückzuführen sein (Abbildung 5). Bei weiterer Erwärmung rekristallisieren die MIGs in die ursprüngliche ZIF-Cu-1-Phase mit sod-Topologie, was durch exotherme Signale mit einem Beginn um 202 °C (Abbildung 8b) und das Wiederauftreten charakteristischer Reflexe in den Röntgenpulverdiffraktogrammen (Abbildung S20) belegt wird. Auf die Rekristallisation folgt eine thermische Zersetzung bei etwa 220 °C. Werden die MIGs jedoch nur auf 200 °C erhitzt, findet keine Rekristallisation statt, und in den zweiten DSC-Heizscans werden wieder Glasübergänge beobachtet (Abbildung 8c). Wichtig ist, dass die MIGs aus ZIF-Cu-1 die ersten ZIF-Gläser auf Cu2+-Basis sind, was die Vielfalt der ZIF-Glasfamilie über die bisher bekannten Materialien mit den Metallzentren Zn2+, Co2+ und Fe2+[57] hinaus erweitert. Angesichts der einzigartigen katalytischen, elektronischen und Redox-Eigenschaften von MOFs auf der Basis von Cu2+,58-60 erweitert die Erkenntnis, dass PSBM den Zugang zu MOF-Gläsern auf der Basis von Cu2+ ermöglicht, das Spektrum der möglichen Anwendungen dieser Materialklasse erheblich.
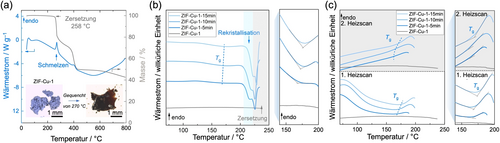
(a) TG/DTA-Daten von ZIF-Cu-1. Der Einschub zeigt mikroskopische Bilder des reinen mikrokristallinen ZIF-Cu-1-Pulvers und der glasartigen Phase, die durch Erhitzen von ZIF-Cu-1 auf 270 °C unter N2-Atmosphäre (d. h. bis zum Offset des endothermen DTA-Signals) und anschließendes Abkühlen auf Raumtemperatur erhalten wurde. (b) DSC-Messungen von ZIF-Cu-1 und seinen PSBM-Derivaten, aufgezeichnet bis zu einer Höchsttemperatur von 235 °C. (c) Zyklische DSC-Scans von ZIF-Cu-1 und seinen PSBM-Derivaten. Um eine Rekristallisation der PSBM-Proben zu vermeiden, wurde der erste Heizscan nur auf 190 oder 200 °C aufgeheizt. Die Heizrate betrug bei allen Messungen +10 °C min−1. Der Zoom auf der rechten Seite in den Feldern (b) und (c) dient zur Hervorhebung der Glasübergangssignale.
Unter den bekannten ZIF-Glasbildnern der Zusammensetzung M(im)2, mit M2+=Zn2+ (ZIF-4), Co2+ (ZIF-4), Fe2+ (MUV-24) und Cu2+ (ZIF-Cu-1), ist das Cu-Derivat einzigartig. Die metastabilen ZIF-4 (cag-Topologie) und MUV-24 (lla1-Topologie) rekristallisieren bei thermischer Behandlung zu Polymorphen mit zni-Topologie, und die M(im)2-Phasen mit zni-Topologie schmelzen (zersetzen sich im Fall von Co2+) bei Temperaturen zwischen 482 und 590 °C.57 Die Flüssigkeiten von Zn(im)2 und Fe(im)2 können auf Raumtemperatur gequencht werden, um die entsprechenden Gläser mit Glasübergangstemperaturen von 292 °C (Zn2+) oder 190 °C (Fe2+) zu erhalten. ZIF-Cu-1 besitzt die sod-Topologie, die aufgrund der einzigartigen abgeflachten tetraedrischen Koordinationsgeometrie des Cu2+-Ions bereits recht dicht ist (Abbildung 2). Eine Festphaseumwandlung zu einem Polymorph mit zni-Topologie wird für Cu(im)2 nicht beobachtet, wahrscheinlich weil die zni-Topologie mit der abgeflachten tetraedrischen Cu2+-Geometrie nicht realisiert werden kann. Stattdessen schmilzt ZIF-Cu-1 bei einer viel niedrigeren Temperatur (~260 °C) und zersetzt sich simultan. Mit Hilfe der PSBM-Technik kann jedoch eine nicht zersetzte, glasartige Form von ZIF-Cu-1 erhalten werden, die eine Glasübergangstemperatur (Tg) von ~166 °C aufweist. Daher sind die Tg-, Tm- und Td-Werte von ZIF-Cu-1 die niedrigsten in der Reihe M(im)2. Dies deutet auf eine größere Labilität der Cu−N-Bindung im Vergleich zu den Bindungen mit den anderen M2+-Ionen hin.
Schlussfolgerung
In unserer Studie untersuchten wir die Amorphisierung und Glasbildung von zwölf verschiedenen ZIFs mit einer Reihe von imidazolatartigen Linkern und Metallionen (Zn2+, Co2+ und Cu2+) durch lösungsmittelfreie PSBM. Wir beobachteten, dass ZIFs, die schmelzen und schmelzgequenchte Gläser bilden können, auch durch PSBM verglasen. Umgekehrt zeigen ZIFs, die sich vor dem Schmelzen thermisch zersetzen, unterschiedliche Reaktionen auf das Kugelmahlen; einige zeigen glasartige Eigenschaften, andere nicht. Die Abwesenheit von glasartigem Verhalten in ZIF-8 und ZIF-70 kann auf die außergewöhnlich starke Zn−N-Bindung mit dem mim−-Linker in ZIF-8 und die sehr geringe thermische Stabilität des nim−-Linkers in ZIF-70 zurückgeführt werden. Im Falle des nicht schmelzenden ZIF-76 ist eine Verglasung durch PSBM möglich, da die Imidazolat-Linker in diesem Material eine angemessene thermische Stabilität und eine ausreichend geringe Zn−N-Bindungsstabilität aufweisen. Die Bedeutung von PSBM bei der Bildung von ZIF-Gläsern wird besonders im Fall von ZIF-Cu-1 deutlich. Die geringere thermische Stabilität von ZIF-Cu-1 ist wahrscheinlich auf die labilen Cu−N-Bindungen und die Redoxaktivität der Cu2+-Zentren zurückzuführen, was zu simultanem Schmelzen und thermischer Zersetzung der kristallinen ZIF-Cu-1 Phase führt. Die Amorphisierung durch PSBM ermöglicht jedoch das Erreichen eines glasartigen Zustands in ZIF-Cu-1 unter Beibehaltung der Materialintegrität, wodurch das ersten ZIF-Glases auf Cu2+-Basis geschaffen wurde.
Unsere Forschung unterstreicht das große Potenzial von PSBM für die Entwicklung neuer glasartiger ZIFs. Während die kleine Partikelgröße der aus PSBM hergestellten Gläser ihre direkte Anwendung einschränken könnte, erleichtert der Prozess des Sinterns oder Umschmelzens durch Erhitzen der Materialien über ihre Glasübergangstemperatur die Partikelverschmelzung und ermöglicht die Bildung von Glasmonolithen.61, 62 Zukünftige Studien sollten die Anwendbarkeit von PSBM für die Herstellung glasartiger MOFs unter Verwendung alternativer Linkerstrukturen, wie Dicarboxylate, untersuchen.63, 64 Diese Erweiterung könnte entscheidend dazu beitragen, den Anwendungsbereich von MOF-Gläsern auszubauen, der traditionell durch die Notwendigkeit eingeschränkt ist, dass MOFs schmelzbar sein müssen – eine Eigenschaft, die nur eine begrenzte Anzahl von MOFs aufweist. So können wir uns vorstellen, dass mehrere nicht-schmelzbare ZIFs und andere MOFs ebenfalls durch PSBM verglast werden können. Darüber hinaus könnte die Herstellung von MOF-Gläsern durch Kugelmahlen bei Raumtemperatur nicht nur energieeffizienter sein31 sondern ermöglicht auch die Integration thermisch empfindlicher Stoffe, wie organische oder metallorganische Moleküle, in vielseitige MOF-Glaskomposite.65 Dieser Ansatz erweitert das Spektrum potenzieller Anwendungen und ebnet den Weg für die Entwicklung multifunktionaler MOF-Glasverbundwerkstoffe, die damit in vielfältigere Anwendungsbereiche vordringen können.
Unterstützende Informationen
Einzelheiten zur Materialsynthese, weitere Röntgenpulverdiffraktionsdaten (XRPD), XRPD bei variabler Temperatur mit Synchrotronstrahlung (VT-XRPD), Röntgentotalstreuung, simultane thermogravimetrische und differentielle thermische Analysen (TG/DTA), und Differential-Scanning-Kalorimetrie (DSC), FTIR- und 1H NMR-Spektroskopie, Rasterelektronenmikroskopie (REM), optische Mikroskopie sowie weitere Gasphysisorptionsdaten und Analyseverfahren.
Danksagung
Wir danken der Deutschen Forschungsgemeinschaft, DFG, (Projekt 447344931, HE 7628/7-1) für die finanzielle Unterstützung. W.L.X. dankt dem China Scholarship Council (CSC No. 202008110211). J.-B.W. dankt dem Fonds der Chemischen Industrie für ein Kekulè-Stipendium. Die Autoren danken DELTA Dortmund für die Bereitstellung von Strahlzeit an der Beamline BL9 und Dr. Christian Sternemann und Dr. Michael Paulus für ihre Hilfe bei den XRPD-Experimenten mit variabler Temperatur. Wir danken DESY (Hamburg, Deutschland), einem Mitglied der Helmholtz-Gemeinschaft HGF, für die Bereitstellung der experimentellen Einrichtungen. Die Röntgentotalstreuung dieser Forschung wurde an PETRA III an der Beamline P02.1 durchgeführt (Proposal I-20210316 und Rapid-Access 20010266). Wir danken Pascal Kolodzeiski, Dr. Jianbo Song, Dr. Athanasios Koutsianos, Dr. Roman Pallach und Dr. Louis Frentzel-Beyme für ihre Hilfe bei der Messung und Analyse der Röntgentotalstreuungsdaten. Wir danken Dr. Martin Etter für die Messung unserer Proben während der Rapid-Access-Beamtime (20010266). Guoqiang Li danken wir für seine Hilfe bei der Synthese von phasenreinem ZIF-76. Volker Brandt danken wir für die Aufnahme der REM-Bilder. Open Access Veröffentlichung ermöglicht und organisiert durch Projekt DEAL.
Interessenkonflikt
Die Autoren erklären, dass keine Interessenkonflikte vorliegen.
Open Research
Data Availability Statement
Die Daten, die die Ergebnisse dieser Studie unterstützen, sind in den Hintergrundinformationen zu diesem Artikel verfügbar.




