Vektorielle Katalyse mit oberflächenverankerten nano-metallorganischen Gerüsten in mikrofluidischen Reaktoren
Abstract
Vektorielle Katalyse – die Steuerung von mehrstufigen Reaktionen in einer programmierten Abfolge und durch definierte räumliche Lokalisierung in einem mikroskaligen Reaktor – ist ein grundlegendes Ziel in der bioinspirierten Katalyseforschung. Die Übertragung von Konzepten aus der natürlichen Kaskaden-Biokatalyse zu künstlichen hierarchischen chemischen Systeme bleibt jedoch eine Herausforderung. Hier zeigen wir die Integration von zwei verschiedenen oberflächenverankerten, nanometergroßen metallorganischen Gerüsten (MOFs) in einem mikrofluidischen Reaktor zur Modellierung der vektoriellen Katalyse. Die Katalysatoren wurden an definierten Abschnitten entlang des Mikrokanals immobilisiert, dies ermöglichte eine zweistufige Kaskadenreaktion mit vollständiger Umsetzung nach 30 Sekunden und hohen Umsatzfrequenzen (TOF≈105 h−1).
“Vektorielle Katalyse”, eine definierte mehrstufige Reaktionsfolge, zielt auf die lokale Integration von Multifunktionalität und den kontrollierten Zugang zum aktiven Zentrum ab, ermöglicht durch die räumliche Positionierung des Katalysators in Verbindung mit einem Transportgradienten.1 Dieses Konzept stammt aus der Natur, da Enzyme und ihre räumliche Anordnung die Reaktionsumgebungen über Längenskalen chemisch und strukturell kontrollieren, um hochspezifische mehrstufige Substratumwandlungen, über Zwischenprodukte, zum Endprodukt an verschiedenen aktiven Stellen zu realisieren.2 Die Nachahmung dieses Ansatzes beruht auf eindeutigen (im Gegensatz zu zufälligen) Eins-zu-Eins-Wechselwirkungen zwischen Reaktanten und spezifischen aktiven Zentren, wobei zusätzlich die Vorteile der kontinuierlichen Flusskatalyse genutzt werden.3 Dies wird erreicht, indem eine Reihe von Zentren in einem Kanal lokalisiert und ein Gradient entlang der axialen Richtung angelegt wird, um den Fluss anzutreiben – ein mikrofluidischer Reaktor.1
Eine solche Sequenzierung von Reaktionen erfordert eine präzise Organisation der reaktionsspezifischen Umgebung auf Nano- und Mikroebene, was für synthetische anorganische Materialien eine Herausforderung darstellt. Zu den Steuerungselementen gehören der gerichtete Massentransport, die induzierte Orientierung und Ausrichtung der Reaktanten in beschränkten Räumen und der entatische Zustand der aktiven Zentren. Diese Parameter rationalisieren die Verwendung einer modular aufgebauten Verbindungsklasse mit synthetischer Kontrolle über Hohlräume, Topologien und physikochemische Eigenschaften – metallorganische Gerüste (MOFs).4 Letztere werden durch die Kombination von anorganischen (Metall-Oxo)-Knoten und organischen Verbindungselementen gebildet, wodurch Koordinationsnetzwerke mit dauerhafter Porosität entstehen.5 Jüngste Studien zeigten, dass das flexible Design von Katalysatorsystemen von der molekularen Präzision der MOF-Porenstrukturen, ihrem definierten funktionalisierten Koordinationsraum und dem Einschluss aktiver Spezies profitiert, um die Reaktivität zu kontrollieren.6 Das Potenzial von MOFs für die biologisch nachahmende vektorielle Katalyse bleibt jedoch unausgeschöpft, da die meisten MOFs sich entweder auf eine einstufige Reaktion konzentrieren oder eine “chemisch inerte” Wirtsumgebung für die aktive Spezies bieten. Zu den Herausforderungen gehören oberflächenselektive Positionierung von MOFs und Transportbeschränkungen aufgrund ungenutzter innerer Porenvolumina.7
Dies veranlasste uns eine Strukturierungstechnik zur präzisen Positionierung nanoskaliger MOFs auf Substraten zu entwickeln, um ihre räumliche Ausrichtung zu steuern,8 die Substratdiffusion zu verbessern und die Umsatzfrequenz (TOF) im Vergleich zu ihren heterogenen mikrokristallinen Pulvern und quasi homogenen kolloidalen MOFs um mehrere Größenordnungen zu erhöhen.9
In dieser Arbeit berichten wir über MOF-basierte vektorielle Katalyse durch die Integration von nanometer-großen oberflächenverankerten MOFs (SA-NMOFs) als Lewis-Säure-Katalysatoren in einen mikrofluidischen Reaktor. Anhand eines Modellreaktoraufbaus überprüfen und validieren wir die Reaktionssequestrierung mit modularen anorganischen Materialien. Dabei wurde die zweistufige Hydrolyse von Benzaldehyddimethylacetal (BADMA) zu Benzaldehyd (BA), gefolgt von der Knoevenagel-Reaktion von BA mit Malononitril (MAN) zu 2-Benzylidenmalononitril (BACN) untersucht. Es wurden etablierte MOF-Katalysatoren ausgewählt,10-12 welche vielversprechende katalytische Eigenschaften für die angestrebte Reaktionsfolge aufweisen. Diese Katalysatoren wurden in Polydimethylsiloxan (PDMS)-basierten mikrofluidische Reaktoren mit einem definierten Fluss abgeschieden um deren programmierbaren Reaktionsraum zu nutzen (Abbildung 1). Bisherige Berichte über MOF-integrierte mikrofluidische Geräte sind begrenzt und konzentrieren sich auf MOF-basierte Sensoren oder Assays.13 Dagegen zeigen wir eine kontrollierte kovalente Verankerung von NMOFs an definierten mikroskaligen Kanalabschnitten, die eine positionsbasierte sequentielle Reaktivität ermöglicht. Die Funktionalität dieser SA-NMOF-dekorierten mikrofluidischen Reaktoren belegen wir durch die vollständige Umwandlung von BADMA zu BACN in 30 s mit hohen TOFs von ≈105 h−1, mehrere Größenordnungen überlegen verglichen mit kolloidalen MOF-Katalysatoren.
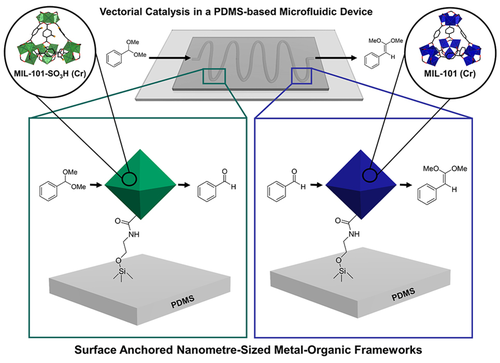
Konzept des mikrofluidischen Reaktors. Zwei oberflächenverankerte metallorganische Gerüste (SA-NMOFs, grüne und blaue Oktaeder) an definierten Kanalabschnitten katalysieren selektiv einen Reaktionsschritt vom Reaktanten (BADMA) über das Zwischenprodukt (BA) zum Produkt (BACN).
Wir haben vier MOF-Katalysatoren ausgewählt, namentlich UiO-66 (Zr6O4(OH)4(bdc)6, bdc=1,4-Benzoldicarboxylat), MIL-101, MIL-101-SO3H, und MIL-101-NH2. Letztere bestehen aus Cr3O(H2O)(OH)6+ Knoten und den funktionalisierten Linkern (bdc-SO3Na)2−/(bdc-SO3H)2−, sowie bdc-(NH2)2−/(bdc-NH3)−(bdc-SO3Na2−=2-Sulfo-1,4-benzoldicarboxylat-Mononatriumsalz; bdc-NH22−=2-Amino-1,4-benzoldicarboxylat). Diese wurden als NMOFs mittels, leicht abgeänderten, in der Literatur beschriebenen Verfahren synthetisiert,14 und durch Rasterelektronenmikroskopie (REM), Pulverröntgendiffraktometrie (PXRD), dynamische Lichtstreuung (DLS) und N2-Adsorption charakterisiert (Abbildungen S1–S3). Die erhaltenen PXRD-Muster bestätigen kristalline, phasenreine NMOF-Proben. Die Linienverbreiterung deutet auf reduzierte Kristallit-Domänengrößen hin, die anhand der Scherrer-Gleichung geschätzt wurden (Tabelle S1).15 Die primären Partikelgrößen der NMOFs und die hydrodynamischen Radien wurden aus REM- bzw. DLS-Messungen ermittelt und lagen zwischen 21–157 nm.
Vor der Integration in mikrofluidische Reaktoren wurde die NMOF-Serie in Batch-Reaktionen für die Hydrolyse von BADMA zu BA und die anschließende Reaktion mit MAN zu BACN getestet (Abbildung 2). Es wurde ein iteratives Optimierungsverfahren durchgeführt, um kompatible Reaktionsbedingungen für jeden Schritt, den NMOF-Katalysator und den PDMS-basierten mikrofluidischen Reaktor zu finden (Abbildungen S4, S5).
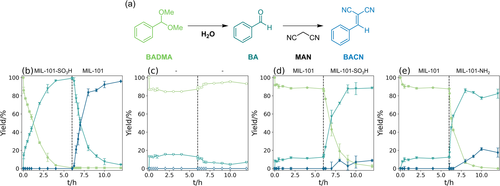
Vor der Integration von SA-NMOFs in mikrofluidischen Reaktoren wurden die Reaktionsbedingungen in Batch-Reaktionen mit NMOF-Kolloiden getestet: a) Gezielte Reaktionsfolge für die vektorielle Katalyse: Hydrolyse von Benzaldehyddimethylacetal (BADMA) zu Benzaldehyd (BA), gefolgt von der Knoevenagel-Kondensation mit Malononitril (MAN) zu 2-Benzylidenmalononitril (BACN). b)–e) Zeit-Ausbeute-Diagramme von BADMA (grün, •), BA (türkis, ▾), und BACN (blau, ⧫) für die Reaktionsfolge in einem Batchreaktor. Die Sequenz wurde durch zwei verschiedene Katalysatoren katalysiert: Katalysator 1 für 6 Stunden und dann entfernt, worauf Katalysator 2 mit 2 Äquivalenten MAN zugegeben wurde. Die verwendeten Katalysatoren sind (b) MIL-101-SO3H/MIL-101; (c) keine/keine; (d) MIL-101/MIL-101-SO3H und (e) MIL-101/ MIL-101-NH2. Reaktionsbedingungen: 0–6 Stunden: 100 μM BADMA in 4 : 1.1 (v%) Dioxan/Wasser (5.1 mL) und 5 mg Katalysator 1, T=50 °C; 6–12 Stunden: 100 μM BADMA und 200 μM (2 Äquiv.) MAN in 4 : 1.1 (v%) Dioxan/Wasser (5.1 mL) und 5 mg Katalysator 2, T=50 °C.
Dabei stellte sich heraus, dass (i) Acetonitril (MeCN) oder Dioxan kompatible organische Lösungsmittel sind, (ii) H2O (≥125 Äquiv.) die Bildung von BA und BACN fördert, (iii) mehr MAN-Äquivalente die BACN-Bildung begünstigen und (iv) eine Erhöhung der Temperatur die Produktbildung steigert, allerdings begrenzt durch den Siedepunkt der Lösungsmittel. Innerhalb dieser Parameter waren MIL-101-SO3H und MIL-101-NH2 die aktivsten Katalysatoren für die BADMA-Hydrolyse, während die Knoevenagel-Kondensation am effektivsten durch MIL-101 katalysiert wurde. Eine entscheidende Voraussetzung für ein integriertes Kaskadenreaktionssystem, bei dem alle Reaktanten gleichzeitig vorhanden sind, ist, dass jeder Katalysator tatsächlich nur einen einzigen Schritt katalysiert und nicht mit anderen interferiert. Mit anderen Worten, es ist ein Satz orthogonaler Katalysatoren erforderlich. Daher überprüften wir, ob dies auf unsere MOF-basierten Lewis-Säure-Katalysatoren zutrifft, indem wir sie Schritt für Schritt in Batch-Experimenten hinzufügten und die Auswirkungen auf die Produktausbeute (BA und BACN) untersuchten.
Wenn die Katalysatoren schrittweise in der richtigen Reihenfolge zugegeben wurden (Abbildung 2b), reagiert BADMA innerhalb von 6 Stunden zu BA, katalysiert durch MIL-101-SO3H. Nach der Entfernung von MIL-101-SO3H durch Filtration werden 2 Äquivalente MAN und 5 mg MIL-101 zugegeben, und es entsteht das Endprodukt BACN. Wenn jedoch kein Katalysator zugegeben wird (Abbildung 2c) oder die Reihenfolge der Katalysatoren umgekehrt wird (Abbildungen 2d, e), entsteht nur 0 % (c), 8.9 % (d) oder 17.5 % (e) BACN nach 12 Stunden. Folglich sind die Katalysatoren ausreichend selektiv, stören die andere Reaktion unter diesen Bedingungen nicht und die sequentielle Umwandlung erfordert eine spezifische Abstimmung zwischen Katalysator und Reagenz.
Die Übertragung dieser Ergebnisse von Batch-Reaktionen auf einen mikrofluidischen Durchflussreaktor erforderte die Verankerung der NMOF-Katalysatoren an den Kanalwänden des Reaktors. Wie bereits beschrieben,8, 9 verwendeten wir Amidbindungen für die kovalente Bindung von NMOFs an das Substrat. Diese Bindungen wurden zwischen terminalen funktionellen Carbonsäuregruppen an der Oberfläche der NMOF-Partikel und den Amin-funktionalisierten Substratoberflächen (d. h. PDMS, aber auch Substratoberflächen aus Glas oder Silizium wurden zum Vergleich getestet) gebildet. Diese Oberflächen wurden dann mittels REM (Abbildung S6) und induktiv gekoppelter Plasmamassenspektrometrie (ICP-MS, Tabelle S2) untersucht. Die REM-Untersuchung zeigt eine relativ dichte Beschichtung und gleichmäßige Verteilung der NMOF-Partikel auf der Si-Oberfläche, die bei UiO-66 und MIL-101 besonders ausgeprägt ist. Die Partikelgrößenverteilung nach der Verankerung der Partikel verringerte sich leicht, wobei die kugelförmige Partikelform erhalten blieb. Wir vermuten, dass der Elektronenstrahl die Probe beschädigt oder dass der Verankerungsprozess kleinere Partikel gegenüber größeren bevorzugt. Die flächenspezifische molare Menge der an den Oberflächen (Si und PDMS) abgelagerten aktiven Metallzentren wurde durch Aufschluss der SA-NMOF-Proben mit H2O2/HNO3 bei 150 °C und ICP-MS-Messung auf 0.66–5.31 nmol cm−2 bestimmt (Tabelle S2). Die erhaltenen Werte sind vergleichbar mit unseren früheren Daten von der SA-NMOF-Methode.9
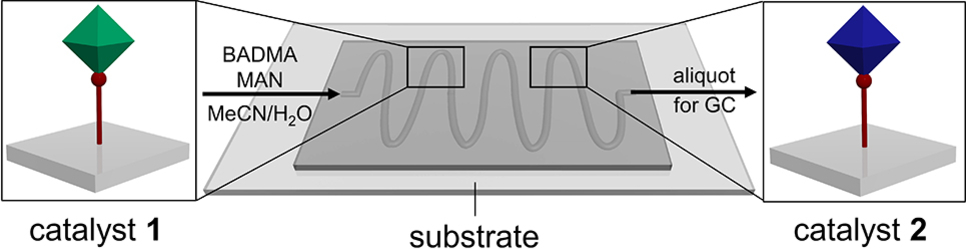
Die mikrofluidischen Reaktoren wurden durch PDMS-basierte Formgebung und Reaktorversiegelung hergestellt. Zunächst wurden SA-NMOF-Substrate (PDMS und Glas) durch Amidbindung hergestellt. Anschließend wurde PDMS mit einer geprägten Kanalstruktur auf das NMOF-funktionalisierte Substrat versiegelt, wodurch der mikrofluidische Reaktor entstand (Abbildungen S7–S9). Auf Grundlage der zuvor beschriebenen Charakterisierung unserer NMOF- und SA-NMOF-Referenzproben untersuchten wir systematisch den Aufbau für die mikrofluidische vektorielle Katalyse und die Auswirkungen auf die Umwandlung, die Selektivität und die TOFs. Eine Lösung von BADMA und MAN in MeCN/H2O oder Dioxan/H2O wurde in den mikrofluidischen Reaktor injiziert. Durch Kapillarkräfte durchlief die Lösung den Mikroreaktor und eluierte am Auslass mit einer Retentionszeit von nur 30 s. Die Umsätze wurden durch Analyse von eluierenden Aliquoten mittels GC nach Verdünnung mit MeCN oder Dioxan bestimmt (Tabelle 1). Zunächst wurden Reaktoren verwendet, die mit nur einem SA-NMOF-Katalysator beladen waren, darunter ein Blindreaktor (Tabelle 1, Eintrag 1), MIL-101-NH2 (Eintrag 2), MIL-101-SO3H (Eintrag 3) und MIL-101 (Eintrag 4). Die Ausbeuten und Umsätze zeigen eine Nullumwandlung für den Blindversuch, und nur der SA-NMOF beladene Reaktor mit MIL-101 (Eintrag 4) lieferte eine beachtliche Umwandlung von 15.5 % BADMA zu BA. Die beiden anderen Katalysatoren, d. h. MIL-101-NH2 (Eintrag 2) und MIL-101-SO3H (Eintrag 3), zeigten eine höhere Umwandlung zum Zwischenprodukt BADMA, aber das gewünschte Endprodukt BACN wurde nicht beobachtet.
|
Katalysator 1 |
Katalysator 2 |
Menge [%] |
||
|---|---|---|---|---|---|
|
|
|
BADMA |
BA |
BACN |
1 |
– |
– |
0.0 |
0.0 |
0.0 |
2 |
MIL-101-NH2 |
MIL-101-NH2 |
41.0 |
59.0 |
0.0 |
3 |
MIL-101-SO3H |
MIL-101-SO3H |
58.7 |
41.3 |
0.0 |
4 |
MIL-101 |
MIL-101 |
84.5 |
15.5 |
0.0 |
5 |
MIL-101-NH2 |
MIL-101 |
14.9 |
12.8 |
72.3 |
6 |
MIL-101-SO3H |
MIL-101 |
9.7 |
7.9 |
82.4 |
7 |
MIL-101 |
MIL-101-SO3H |
74.5 |
25.5 |
0 |
Wir erreichten jedoch Umsätze von 85–90 % für BADMA und 72–82 % des gewünschten Produkts BACN, indem wir die SA-NMOF-Katalysatoren in der optimalen Reihenfolge einsetzten, d. h. mit MIL-101-NH2 (Eintrag 5) oder MIL-101-SO3H (Eintrag 6) an Position 1 für die BADMA-Hydrolyse und mit MIL-101 an Position 2 für die Knoevenagel-Kondensation. Hier ist die Reihenfolge der Katalysatoren entscheidend, da ein Wechsel der Positionen zu 0 % Produktbildung führte (Eintrag 7). Diese Ergebnisse bestätigen unseren Proof-of-Concept mit dem ersten oberflächengebundenen NMOF-basierten mikrofluidischen vektoriellen Reaktor. Weitere Optimierungen der Reaktionsparameter, einschließlich Lösungsmittel, MAN-Äquivalente, Zyklusexperimente und verschiedene Substrate sind in Tabelle S3 aufgeführt.
Die TOFs wurden berechnet und die Eingabedaten, Berechnungsdetails und angewandten Annahmen sind in der Supporting Information gegeben (Kapitel S1/Tabelle S4). Hier waren die TOFs außergewöhnlich hoch und lagen im erwarteten Bereich, basierend auf den zuvor berichteten SA NMOF Referenzproben.9 Für die Hydrolyse von BADMA, haben wir TOFs≈1 000 000 h−1 für MIL-101-NH2 und MIL-101-SO3H erhalten, während für die Knoevenagel Reaktion TOFs ≈400 000 h−1 für MIL-101 berechnet wurden. Einschlägige andere Veröffentlichungen über MOF-basierte Tandemkatalysatoren, die auf eine vollständige Umsetzung der Reaktionssequenz durch einen bifunktionalen MOF-Katalysator abzielen, berichten deutlich niedrigeren TOFs zwischen 0.7–51 h−1.10, 11, 16 Ein umfassender Überblick ist in den Tabellen 2 und S5 zu finden.
Katalysator |
Lösungsmittel |
T [°C] |
t [h] |
ncat [mol %] |
Menge [%] |
TOF [h−1] |
TOF [h−1] |
Ref. |
|
|---|---|---|---|---|---|---|---|---|---|
|
|
|
|
|
BA |
BACN |
Hydrolyse |
Knoevenagel Kondensation |
|
MIL-101-NH2(Cr) |
MeCN, H2O |
RT |
0.008 |
0.008 |
12.8 |
72.3 |
1.13×106 |
– |
+ |
MIL-101(Cr) |
MeCN, H2O |
RT |
0.008 |
0.02 |
12.8 |
72.3 |
– |
4.05×105 |
+ |
PCN-124(Cu) |
DMSO |
50 |
12 |
1.0 |
0 |
100 |
16.8 |
16.8 |
|
MIL-101-NH2(Al) |
dioxane |
90 |
3 |
43 |
6 |
94 |
0.76 |
0.74 |
|
Cr-MIL-101-AB-X |
DMF |
90 |
0.08 |
4.0 |
44 |
17 |
180 |
51 |
|
Zn-MOF 1 |
DMF |
80 |
0.5 |
1.0 |
16 |
10 |
52 |
20 |
|
Cd-MOF 1 |
DMF |
90 |
5 |
0.56 |
0 |
84 |
30 |
30 |
|
Die Untersuchung der Ratenlimitierung in den mikrofluidischen Reaktoren mit der Random-Walk-Gleichung zeigt, dass die Substratdiffusion zu den SA-NMOFs nicht der ratenbestimmende Schritt ist, sondern vielmehr die Diffusion hinein in und innerhalb der SA-NMOFs (siehe Supporting Information, Kapitel S1). Daher können die hohen TOFs durch die kleinen MOF-Partikelgrößen erklärt werden, die die Diffusionsbeschränkungen innerhalb der MOFs verringern. Außerdem verhindern wir durch die Oberflächenverankerung unserer Katalysatoren die Partikelaggregation während der Katalyse, die ihre katalytische Aktivität einschränken würde.9, 17
Die Realisierung der vektoriellen Katalyse durch die Integration räumlich lokalisierter und sequestrierter katalytischer Zentren in mikrofluidischen Reaktoren ist ein visionäres Ziel für die bioinspirierte Katalyseforschung. Wir heben den Proof-of-Principle-Charakter unserer zweistufigen Kaskadenstudie hervor, die als etablierte und vergleichbare Modellreaktion gewählt wurde, um den erfolgreichen Materialaufbau und die kontrollierte Komponentenhierarchie zu validieren. Diese ermöglicht eine vektorielle In-Flow-Katalyse und validiert das vorgestellte Konzept auf der Grundlage von SA-NMOF-Katalysatoren. Die Daten deuten darauf hin, dass diese auch auf andere Reaktionsabläufe übertragen werden können. In weiteren Studien könnten anspruchsvollere MOFs verwendet werden, mehr Katalysatorzentren und einzelne Reaktionsschritte integriert werden und andere Materialien für die Herstellung von Mikroreaktoren, z. B. zyklische Olefin-Copolymere, eingesetzt werden, um eine bessere thermische Stabilität und eine bessere Kompatibilität mit Lösungsmitteln und Reaktionsbedingungen zu erreichen. Unsere Ergebnisse bieten eine Perspektive für die Integration von Mikroreaktoren mit anspruchsvollen Reaktionsabläufen unter Verwendung maßgeschneiderter MOF-basierter Katalysatorsysteme.
Danksagung
A.L.S. und P.M.S. danken dem Fond der Chemischen Industrie für ihre Promotionsstipendien. Diese Arbeit wurde finanziell von dem Deutsche Forschungsgemeinschaft (DFG) Projekt MOFMOX (FI 502/43-1) und DFG Priority Program 1928 “Coordination Networks: Building Blocks for Functional Systems” unterstützt. Open Access Veröffentlichung ermöglicht und organisiert durch Projekt DEAL.
Interessenkonflikt
Die Autoren erklären, dass keine Interessenkonflikte vorliegen.
Open Research
Data Availability Statement
Die Daten, die die Ergebnisse dieser Studie unterstützen, sind in der Supporting Information zu diesem Artikel verfügbar.




