Nanosicherheitsforschung – sind wir auf dem richtigen Weg?
Abstract
Die Zahl der publizierten Studien zum Thema Nanosicherheit spricht für sich. Wir verzeichnen seit ungefähr 15 Jahren einen nahezu exponentiellen Anstieg bei den Publikationen zur “Nanotoxikologie”. Waren es bis zum Jahr 2000 noch wenige Hundert, so sind seit 2001 mehr als 10 000 Publikationen zum Thema “Nanomaterialien: Umwelt und Gesundheit” veröffentlicht worden. Allein, eine Klarheit bei der Aussage zur Sicherheit der Nanomaterialien bleiben die meisten dieser Studien schuldig. Im Gegenteil: Viele der Arbeiten widersprechen einander oder kommen auch zu völlig falschen Schlussfolgerungen. Bereits vor drei Jahren haben wir an gleicher Stelle auf die Missstände bei den Studiendesigns und die Fehlerquellen in den Methoden hingewiesen. Auf der Basis einer umfassenden Literaturstudie und an ausgewählten toxikologischen Endpunkten soll aufgezeigt werden, wo die wesentlichen Schwachpunkte der Studien liegen und was wir in der Zukunft verbessern müssen.
1. Zusammenfassung
Die Studie hatte zum Ziel, die Literatur der letzten 10–15 Jahre daraufhin zu sichten, inwieweit humantoxikologische Bewertungen für synthetisch hergestellte Nanomaterialien (ENMs=engineered nanomaterials) vorgenommen werden können. Auf der Basis bestimmter gesundheitlicher Effekte beim Menschen sowie biologischer Effekte bei Tieren oder in Zellkulturen wurden mehr als 10 000 Publikationen ab dem Jahr 2000 gesichtet.
Für diesen Aufsatz sind die Ergebnisse für vier Kernthemen abschließend ausgewertet worden. Dies sind die Aufnahme von Nanomaterialien über die drei wesentlichen Expositionspfade der Lunge, des Magen-Darm-Traktes und der Haut sowie die Bewertung der Methoden von Lungenexpositionsstudien durch Inhalations- oder Instillationsexperimente.
Die wesentlichen Kernaussagen, die sich nach der Auswertung von mehr als tausend Literaturstellen zu diesen Fragestellungen herauslesen lassen, sind:
- •
Es ist unbestreitbar, dass ENMs die Lunge und den Magen-Darm-Trakt als Eintrittspforte in den Körper nutzen können. Allerdings ist es meist nur ein sehr kleiner Teil der verabreichten Dosis, der in das Blut und nachfolgend zu sekundären Organen transportiert wird. Der größte Anteil der verabreichten Dosis wird in der Lunge von Makrophagen aufgenommen und mit den Reinigungsprozessen aus der Lunge entfernt und/oder aus dem Magen-Darm-Trakt über die Faeces ausgeschieden. Eine systemische Wirkung auf die inneren Organe wurde in nur wenigen der ausgewerteten Studien beobachtet, jedoch nicht nachvollziehbar als spezifische ENM-Wirkung nachgewiesen.
- •
Zum Vergleich von Instillations- zu Inhalationsversuchen: Instillationsstudien werden grundsätzlich mit hohen lokalen Dosen durchgeführt (versuchsbedingt) und liegen damit öfter im Overload-Bereich als Inhalationsstudien. Nach Applikation der Nanomaterialien, sowohl bei Inhalations- als auch bei Instillationsexperimenten, wurden häufig transiente, also vorübergehende Entzündungen beobachtet, die auf eine unspezifische Partikelreaktion schließen lassen, wie diese auch bei Feinstaubbelastungen beobachtet wird. Ausnahmen bilden hier die langen und steifen CNT-Modifikationen (CNT=Kohlenstoff-Nanoröhrchen), die eine schwerwiegendere Reaktion induzieren. Ein “nanospezifischer” Effekt lässt sich für die Lunge anhand der vorliegenden Studien nicht ableiten.
- •
Unbeachtet bleibt häufig bei bestimmten Nanomaterialien die Tatsache, dass sich diese Materialien langsam (z. B. Ag) oder auch relativ rasch (z. B. CuO, ZnO) in Körperflüssigkeiten auflösen können. Dies führt zu einer völlig anderen Situation, und es liegt hier keine “Nanotoxizität” vor, sondern eine allgemeine stofflich bezogene Toxizität, die meist in Lehrbüchern bereits beschrieben worden ist.
- •
Die vorliegende Literaturstudie könnte sicher gute Hinweise auf wichtige biologische Vorgänge geben, die durch Nanomaterialien beeinflusst werden können. Allerdings ist durch die “babylonische Vielfalt” der Methoden in den Studien zum einen keine Vergleichbarkeit gegeben, und zum anderen sind dadurch auch die sich teilweise widersprechenden Ergebnisse in den Publikationen zu erklären.
- •
Im überwiegenden Teil der Arbeiten wurden die eingesetzten Materialien nicht ausreichend charakterisiert, was zu einer erheblichen Minderung der Aussagekraft dieser Arbeiten bis hin zur völligen Bedeutungslosigkeit der Ergebnisse führt. Ohne eine internationale Verständigung zur Verbesserung der Qualitätskriterien toxikologischer Studien zu Nanomaterialien wird sich die Aussagekraft der Resultate auch in Zukunft nicht erhöhen, der Einsatz der finanziellen und materiellen Mittel wäre weiterhin fragwürdig.
Eine wesentliche Erkenntnis dieser Auswertung ist die Tatsache, dass die überwältigende Mehrzahl der Untersuchungen eher “mechanistische” Studien sind, auch wenn über “toxikologisch relevante” Ergebnisse diskutiert wird. Dies führt zur Verwirrung der Leser dieser Publikationen, da dies in den Arbeiten nicht deutlich genug hervorgehoben wird und viele Diskussionen um toxikologische Endpunkte irrelevant sind, da sie in einem mechanistischen Konzentrationsfenster erhalten wurden und damit für eine toxikologisch begründete Gefährdungsabschätzung nicht von Bedeutung sein können.
Auf der Basis der Ergebnisse werden klare Empfehlungen abgegeben, die sich vor allem an die Durchführenden von Förderprogrammen, an Regulierer, aber auch an die Projektleiter von Studien zur Nanotoxikologie richten.
2. Einleitung
Als wir im Januar 2011 unseren Beitrag in der Angewandten Chemie zum Thema “Nanotoxikologie” publiziert haben,1 gab es zu diesem Thema inklusive des gesamten Jahrganges 2010 knapp 5000 Arbeiten.2 In der Zwischenzeit hat sich die Gesamtzahl der zu diesem Thema publizierten Arbeiten weit mehr als verdoppelt! Dies bedeutet, dass in den vergangenen drei Jahren mehr Beiträge erschienen sind als in den 30 Jahren davor (Abbildung 1). Daraus sollte im Grundsatz eine sehr komfortable Situation resultieren, um eine Abschätzung der möglichen negativen Folgen der Einwirkung von synthetischen Nanomaterialien (ENMs) auf Umwelt und Gesundheit ableiten zu können. Ist nicht mit der steigenden Zahl an Beiträgen in internationalen Zeitschriften auch eine deutliche Verbesserung des allgemeinen Wissens verbunden, oder sind wir da auf dem Holzweg?1
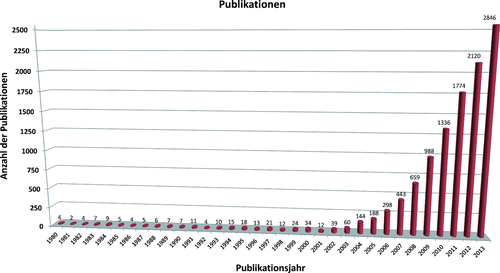
Zahl der publizierten Arbeiten zur Nanotoxikologie in den Jahren 1980 bis 2013.
Ein wenig enttäuschend war das Ergebnis, das 2012 Hristozov et al. in einer Übersicht über die aktuelle Literatur zu Nanomaterialien publizierten, die sie nach bestimmten Kriterien beurteilten.3 Dabei konnte zu den von der Gruppe angewendeten Kriterien und den ausgewählten sechs Materialien nur für die Kohlenstoffnanoröhrchen (CNTs) und die Fullerene ein gutes Ergebnis mit Bezug auf die Charakterisierungen der Materialien und die toxikologischen Informationen als Basis für eine Risikoabschätzung nachgewiesen werden. Für die beiden Nanomaterialien, für die jeweils die meisten Arbeiten gefunden wurden, gab es ein eher enttäuschendes Resultat: Für Titandioxid waren nur 32 % der 302 und für Zinkoxid sogar nur 13 % der 279 Beiträge auswertbar, wenn es um die toxikologischen Daten ging. Natürlich hängt dies auch mit den von der Arbeitsgruppe angelegten Kriterien zusammen. Ganz ähnliche Erfahrungen hat das Projektkonsortium des Projektes DaNa gemacht (Daten und Wissen zu Nanomaterialien – Aufbereitung gesellschaftlich relevanter naturwissenschaftlicher Fakten), das für die Erstellung der Online-Texte nur Originalliteratur verwendet, die einem Kriterienkatalog genügen, der auf der Webseite des Projektes publiziert ist (http://www.nanopartikel.info/files/methodik/Methodik%20zur%20Literaturauswahl.pdf). Durch diese Festlegung auf Minimalkriterien, die erfüllt sein müssen, damit eine Literaturstelle auch berücksichtigt wird, werden je nach Material und Themenstellung bis zu 90 % der publizierten Arbeiten aussortiert, da sie keine genügenden Angaben liefern, die z. B. die Charakterisierung des untersuchten Materials betreffen. Dies wird aber schon seit längerem und von vielen Kollegen gefordert4–11 und ist grundsätzlich ein unerlässliches Merkmal für eine gute Publikation. Es hat sich gezeigt, dass bei ungenügender Charakterisierung (Verwendung “as purchased” und Eigenschaften “as presented by the supplier”) verschiedene Studien erhebliche Fehler gemacht haben, da z. B. schon die Größenverteilung vom Hersteller nicht korrekt angegeben war. Nur wenige Arbeitsgruppen geben außerdem an, ob sie auf Kontaminationen des Materials getestet haben, was bei ENMs ganz besonders wichtig ist, da sie meist nicht unter sterilen Bedingungen hergestellt und verpackt werden. So konnte gezeigt werden, dass Autoren, die entzündliche Prozesse untersucht und die Freisetzung von Entzündungsmediatoren als Endpunkt gemessen haben, falsch-positive Ergebnisse publiziert haben, da das Material mit Endotoxinen kontaminiert war, die genau diese Reaktion im Test hervorgerufen haben.5, 12–17
Weitere Schwachpunkte und Fehlerquellen betreffen das verwendete Lösungs- oder Dispergiermittel, die eingesetzten Konzentrationen oder Dosierungen, die nicht berücksichtigten Interferenzen mit dem Testsystem oder das vollständige Fehlen von Vergleichsmöglichkeiten, da keine Kontrollen durchgeführt worden sind. So konnten meine Kollegen und ich an der Empa beispielsweise zeigen, dass in Tetrahydrofuran aufgenommene Fullerene keinen oxidativen Stress in aquatischen Organismen hervorrufen, sondern die durch den Alterungsprozess im Tetrahydrofuran entstandenen Peroxide diesen Effekt auslösten.18 Weitere Fallstricke beim Dispergieren von Nanopulvern wurden im Projekt NanoCare aufgedeckt.19
Dass viele Fehlinterpretationen in der Literatur zu finden sind, liegt auch an der Tatsache, dass die Konzentrationen, die im Versuch eingesetzt werden, nicht adäquat sind. So hat Wittmaack zeigen können,20 dass bereits eine leichte Überdosierung in der Petrischale bei In-vitro-Experimenten zum totalen Bedecken der Zellen durch agglomerierte Nanopartikel führt, was ihnen die Versorgung mit Nahrungsstoffen und Sauerstoff im Medium erschwert und zum Zelltod führen kann. Eine andere Forschergruppe aus Lausanne hat eine fast 10-fach höhere Konzentration als bei der eben genannten Arbeit eingesetzt, um die Auswirkungen auf die mögliche Induktion des Inflammasoms zu untersuchen.21 Mit dem Wissen, dass die Zellen bei diesen Experimenten unter einer 500 nm dicken Schicht von agglomerierten Nanopartikeln “begraben” worden sind, ist die Interpretation der Ergebnisse in einem völlig anderen Licht zu sehen. Auch im Tierversuch kann eine Überdosierung zu Fehlinterpretationen führen, wenn z. B. durch Instillation eines Bolus in die Lunge die Luftwege verschlossen werden, was zum Erstickungstod des Tieres führt. Auch dies wurde bereits beschrieben.22, 23
Der nächste Punkt betrifft die auftretenden Interferenzen der Nanopartikel mit dem oder den Analyten eines verwendeten Testsystems. Durch ihre hohe Reaktionsbereitschaft als Folge des enorm erhöhten “Oberfläche-zu-Volumen-Verhältnisses” oder durch die besonderen optischen Eigenschaften können die ENMs z. B. Chemikalien an ihrer Oberfläche binden und damit aus dem Testsystem nachhaltig entfernen oder optische Messverfahren direkt beeinflussen. Dies konnten wir schon vor einiger Zeit nachweisen,24 und es wurde in der Zwischenzeit von weiteren Gruppen bestätigt.5, 25–30
Für den Toxikologen häufig noch einigermaßen nachvollziehbar, für den interessierten Laien oder den wissenschaftlichen Nichtexperten auf dem Gebiet der Toxikologie aber nicht ersichtlich, ist die Tatsache, dass fehlende Referenzproben oder Kontrollansätze eine echte Beurteilung eines Effektes praktisch verunmöglichen. Was im medizinischen Bereich Routine ist – ein gemessener Wert wird anhand von Referenzen eingeordnet und lässt erst dann eine Schlussfolgerung auf eine vorliegende Schädigung oder den Gesundheitszustand des Patienten zu – scheint in der Nanotoxikologie völlig verloren gegangen zu sein. Ohne an dieser Stelle einzelne Arbeiten zu zitieren, ist dieser Umstand sicher eine der am häufigsten auftretenden Fehlerquellen bei der Interpretation eines beobachteten Effektes. Da häufig die bloße Tatsache, dass ein Effekt im Vergleich zur unbehandelten Probe auftritt, bereits als toxikologisch relevant angesehen wird, ohne jedoch zu wissen, wie stark der Effekt eigentlich ist und ob er für das jeweilige Gewebe oder die Zellen auch eine biologische Konsequenz hat, werden sehr häufig marginale Effekte als großer Einfluss auf die Zellen “verkauft”.
Alle oben aufgeführten Beispiele, die an dieser Stelle sehr wichtig sind, sollten verdeutlichen, warum zwar eine große Zahl an Publikationen im Titel der Arbeit häufig “toxikologische Effekte” aufführen, was dann aber nicht wirklich durch die Studie belegt wird. Allerdings ist dieser Umstand meist nur Experten des Fachgebiets erkenntlich, und damit ist Spekulationen um die Sicherheit von ENMs Tür und Tor geöffnet.
Mit der Auswertung vieler tausend Publikationen soll daher der Versuch unternommen werden herauszufinden, ob es trotz der qualitativen Unterschiede Gemeinsamkeiten im Hinblick auf die Aufnahmeprozesse und möglichen Wirkungen von ENMs gibt. Außerdem soll sie Wissenslücken deutlich machen, die auch nach mehr als 10 000 publizierten Studien noch vorhanden sind, und eine Diskussion anregen, wie wir in der Zukunft die babylonische Vielfalt der Ergebnisse zusammenführen und auf eine gemeinsame Basis zur Auswertung und Interpretation stellen könnten.2
3. Qualitätskriterien und Ihre Bedeutung
Bereits vor einigen Jahren hat eine Diskussion unter den (Nano-)Toxikologen begonnen, wie die publizierten Studien einzuordnen seien und welche Aussagekraft sie haben. Wie bereits in der Einleitung erwähnt, gibt es Forderungen nach einer ausreichenden Charakterisierung der verwendeten Nanomaterialien, ohne die eine fundierte Aussage gar nicht möglich ist, da allein schon die Beziehung zur Partikelgröße nicht mehr gegeben ist. Solche und ähnliche Mängel in aktuellen Publikationen zur Toxikologie von ENMs führen dazu, dass möglicherweise das Vertrauen in die Abläufe der Prozesse zur Chemikaliensicherheit Stück für Stück verlorengeht. Für herkömmliche Chemikalien gibt es aber bereits entsprechende Konventionen, die internationale Anerkennung gefunden haben.31 Mehr noch, es scheint, dass wir heutzutage die Erkenntnisse, zu denen wir bereits vor mehr als 40 Jahren gekommen waren, nicht mehr respektieren und nur noch in zwei Kategorien denken: Etwas ist giftig oder etwas ist sicher! Henschler hat aber bereits 1973 deutlich gemacht, dass damals genau die gleichen Probleme galten, die wir heute im Zusammenhang mit Nanomaterialien wieder hervorholen und von denen so tun, als wären diese völlig neu!32 Die Frage nach “Wie sicher ist sicher?” kann in der Toxikologie niemals endgültig beantwortet werden, da auch das Theorem von Paracelsus noch immer gilt, demzufolge “allein die Dosis macht, dass eine Substanz giftig ist!” und wir mit dieser Unsicherheit leben müssen. Dennoch ist es die Aufgabe der Toxikologie, auch für die ENMs nachzuweisen, in welchem Dosisbereich und unter welchen Bedingungen sie für Umwelt und Gesundheit kritisch sein können. Eine ausreichende Antwort dazu ist allein mit Tierversuchen nicht zu bekommen, das hat Henschler ebenfalls schon vor 40 Jahren festgestellt. Darüber hinaus hat er damals bereits geschlussfolgert: “Zur besseren Vergleichbarkeit der Resultate sollten toxikologische Laboratorien einer Standardisierung und Qualitätskontrolle unterworfen werden, wie z. B. auf den Gebieten der analytischen und klinischen Chemie. Doppelarbeit und Wiederholungen werden so weitgehend eingeschränkt oder vermieden.” Und: “An Toxizitätsprüfungen sind Mindestanforderungen zu stellen. Detaillierte Regeln des Vorgehens und Auswertens bergen jedoch Gefahren.”32 Wir sind heute im Bereich der Nanotoxikologie leider genauso weit wie eh und je davon entfernt, eine solche Standardisierung der Testverfahren oder eine Qualitätskontrolle der Labore zu haben; Doppelarbeit ist heute vor allem in der EU eher die Regel als eine Ausnahme. Dies führt zu den im weiteren Verlauf noch angesprochenen Problemen bei der Diskussion der Ergebnisse der Studien.
In der vorliegenden Literaturstudie war es ursprünglich angedacht, alle gefundenen Studien daraufhin auszuwerten, inwieweit sie die Kriterien erfüllen, die innerhalb des Projekts DaNa auf der Internetseite zur Qualität der veröffentlichten Arbeiten publiziert wurden (siehe Abschnitt 2). Dies sind sehr strenge Qualitätskriterien, die darauf abzielen, dass nur verlässliche Studien für die Publikation der Texte im Internet Verwendung finden sollen.33 Im Rahmen der hier vorgestellten Ergebnisse konnten diese Kriterien allerdings nicht angewendet werden, da eine solche Arbeit durch die schiere Zahl der zu bewertenden Studien mehrere Jahre in Anspruch nehmen würde. Daher wurde nur eine sehr grobe Qualitätskontrolle vorgenommen, die sich auf die Mindestanforderungen bei der Charakterisierung der Materialien konzentrierte. Arbeiten, die z. B. gar keine Angaben zur Größe der untersuchten Materialien gemacht haben, wurden nicht berücksichtigt. Dennoch sei hier festgestellt, dass wir in Zukunft unbedingt eine Vereinheitlichung der Kriterien sowie eine Standardisierung der Methoden benötigen, damit wir zu vergleichbaren Studien kommen, die uns verlässliche Daten liefern. Mit Bezug auf Mindestanforderungen für eine physikochemische Charakterisierung und die Korrelation zu den biologischen Effekten ist dies jüngst erst wieder von einer internationalen Gruppe gefordert worden.34 Welche Unzulänglichkeiten augenblicklich in den Tests vorhanden sind, macht Tabelle 1 deutlich. Neben der Vielzahl der aufgeführten möglichen Variablen sorgt auch der Umstand, dass viele publizierende Gruppen nicht unmittelbar aus der Toxikologie kommen, dafür, dass die präsentierten Ergebnisse nur schwer interpretierbar sind. Dies macht den Vergleich untereinander nicht einfach, und daher wurden für diese Literaturstudie auch eher forschungsrelevante Hypothesen aufgestellt als solche, die rein toxikologische Kernthesen abfragen.
|
mit dem Nanomaterial assoziierte Variablen |
mit dem Tox-Test assoziierte Variablen |
mit dem biologischen Modell assoziierte Variablen |
|---|---|---|
|
Probenreinigung zur Entfernung biologisch relevanter Spurenstoffe |
Endpunkt-bezogene Auswahl des richtigen Testsystems |
Auswahl des biologischen Systems |
|
Probencharakterisierung des Rohmaterials: Zusammensetzung und Reinheit Größe Form Agglomeration usw. |
verschiedene Testsysteme für den gleichen biologischen Endpunkt |
Zell-Linien: Auswahl der Linie Identifizierung der Linie Alter und Lagerung der Zellen Zahl der Passagen usw. |
|
Probencharakterisierung in Bezug auf biologische Verunreinigungen: Endotoxin usw. |
Kontrollen: angepasste Negativkontrollen angepasste Positivkontrollen Verwendung von Referenzmaterialien |
primäre Zellen/Organsysteme: Spenderabhängigkeit Spendervariabilität Kulturbedingungen |
|
Dispersion in biologischen Medien unter den relevanten Bedingungen: Temperatur Luftfeuchte Gaskonzentrationen (O2, CO2) Salinität usw. |
Testen auf mögliche Interferenzen des ENM mit dem biologischen Testsystem Bindung von Zeigermolekülen Absorption oder Eigenfluoreszenz des Materials usw. |
Kulturbedingungen während des Experiments: Temperatur Luftfeuchte Gaskonzentrationen (O2, CO2) Salinität usw. |
|
Probencharakterisierung in biologischen Medien: Größe und Form Agglomeration Proteincorona usw. |
Messunsicherheit unberücksichtigt: Ringversuche Kalibrierung mit Standards oder Referenzmaterial |
biologische Parameter: Zelldichte Volumen des Mediums Serumgehalt des Mediums Verträglichkeit des Lösungs- oder Dispergiermittels |
Wenn also die Qualität der Studien zur Diskussion steht, dann gibt der vorliegende Aufsatz keinen echten Hinweis darauf, da dies nicht die Zielsetzung gewesen ist, es sei denn, es wird ausdrücklich im jeweiligen Zusammenhang auf die “gute Qualität” einer Studie hingewiesen. Dann genügt diese zitierte Studie entweder dem Kriterienkatalog DaNa (siehe Abschnitt 2), oder der Impact Factor der publizierenden Zeitschrift liegt über 6. Trotz dieser Einschränkung können Fragen, wie eine potenzielle Aufnahme der ENMs in Zellen oder in Organismen, durchaus auch anhand der Fülle der vorliegenden Daten beantwortet werden. Bei widersprüchlichen Daten muss man dann aber genauer hinsehen und nachprüfen, woraus der Widerspruch resultiert und ob dieser eventuell methodisch bedingt ist oder durch die Verwendung eines völlig anderen Materials und völlig anderer Bedingungen hervorgerufen wurde.
4. Die Auswertung der Studien: pro und kontra Standardisierung
Die Auswertung von mehreren tausend Publikationen unter dem Gesichtspunkt der Nanotoxikologie hat grundsätzlich aufgezeigt, dass wir tatsächlich die Vielzahl von Variablen im Studiendesign (Tabelle 1) dort wieder vorfinden und daher ein Vergleich untereinander nur in den seltensten Fällen einen Sinn hat. Wünschenswert wäre es gewesen, wenn sich die Mehrzahl der Studien an die toxikologischen Grundregeln gehalten hätte und Standardvorschriften für die verschiedenen Tests verwendet worden wären. Für epidemiologische Studien gibt es z. B. klare Vorgaben, wie diese angelegt sein sollten. Die Auswahl der Gruppe aus der Bevölkerung oder am Arbeitsplatz soll repräsentativ sein, es muss ein international vergleichbares Studiendesign angewendet werden, und die Parameter, die erfasst werden sollen, müssen klar definiert sein (z. B. Urin, Blut, Verhalten). Weiterhin ist eine Analytik meist nach GLP (Good Laboratory Practice) Voraussetzung, und es müssen erfahrene Wissenschaftler beteiligt sein, die zur Interpretation der erhaltenen Daten nach internationalen Standards befähigt sind. All dies scheint bei der Nanotoxikologie nicht Vorgabe zu sein; weder wird auf die Repräsentativität des biologischen Modells geachtet, noch ist das Studiendesign (experimentelles Set-Up) in irgendeiner Weise international vergleichbar, da meist keine SOPs (Standard Operation Procedures) verwendet werden. Die Parameter, also die biologischen Endpunkte, werden häufig frei festgelegt, und die Analytik folgt keinen standardisierten Prozessen. Weit kritischer ist aber die Tatsache zu bewerten, dass häufig kein toxikologischer Sachverstand in die Studien mit einbezogen wurde, sondern sich alle Naturwissenschaftler gleichermaßen berufen fühlen, zu toxikologischen Problemen Stellung zu nehmen. Dieser Umstand führte gerade in den letzten Jahren dazu, dass verschiedene Arbeitsgruppen diese Tatsache kritisiert haben, auf die Schwachpunkte der meisten Studien eingegangen sind und entsprechende Optimierungen gefordert haben (Tabelle 2).
|
Lit. |
Studienparameter |
Problematik |
|---|---|---|
|
Crist et al., 20125 |
ENM-Charakterisierung |
Sterilität und Endotoxin physikochemische Charakterisierung Verunreinigungen bei der Produktion Biokompatibilität der Komponenten Batch-to-Batch-Konsistenz In-vivo-Stabilität der Nanopartikel |
|
Wittmaack, 201120 |
ENM-Dosierung |
Suspensionskonzentrationen zu hoch; Sedimentation erzeugt Dosierungsverzerrung |
|
Schulze et al., 200819 |
ENM-Dispersion |
Dispersionsvorschrift Agglomeratbildung: Größenverteilung Oberflächenladung Benetzbarkeit der ENMs Adsorption von Mediuminhaltsstoffen (Proteincorona usw.) mit eigenschaftsverändernder Wirkung Sterilität des ENM Endotoxinmessung und -testverlässlichkeit |
|
Wörle-Knirsch et al., 200624 |
Interferenzen |
Dispersion und Lösungsmittel Bindung von Analyten an die ENMs mehrere Methoden für einen Endpunkt Referenzmaterial zum Vergleich |
|
Geys et al., 201028 |
biologische Matrix |
Zelldichte Testmethode Serum (Menge, Herkunft, Spezies) Lösungsmittel (Tween, Polysorbat usw.) |
|
Hirsch et al., 201136 |
Testsystem |
Kalibrierung mit Referenzmaterialien Vergleich mehrerer Methoden Ringversuche mehrerer Labors Abschätzung der Einflussfaktoren Messunsicherheit |
Es wird sicher durch diese Beispiele und die oben gemachten Aussagen deutlich, dass die vorliegende Literaturstudie zwar eine Grundlage zu bestimmten Aussagen zur Verfügung stellen kann, diese aber mit aller Vorsicht betrachtet werden sollten, da die Vergleichbarkeit der publizierten Studien bei weitem nicht gegeben ist. Dennoch kann und soll die Auswertung der Literatur dazu führen, einen Überblick zu bekommen, wenn es um so wichtige Fragen geht wie die Aufnahme von Nanomaterialien in Zellen und Organismen oder die Mechanismen, die durch ENMs in biologischen Systemen beeinflusst oder induziert werden (Mode of Action, MoA). Außerdem kann die Auswertung der Ergebnisse zu einzelnen ganz bestimmten Methoden oder Vorgehensweisen einen guten Eindruck vermitteln, ob diese Methoden in unterschiedlichen Labors zu ähnlichen Ergebnissen führen. In Abschnitt 5 soll dies an zwei Beispielen zu erläutern versucht werden. Zum einen werden die Ergebnisse zur wichtigen Frage präsentiert, ob Nanomaterialien/Nanopartikel von Organismen gleichermaßen gut und ohne Ausnahme aufgenommen werden können, und zum anderen sollen zwei Methoden miteinander verglichen werden – die Inhalation und die Instillation –, die immer wieder als “Goldstandard” herangezogen werden, wobei aber unklar ist, ob sie wirklich beide für die Untersuchung von ENMs gleichermaßen geeignet sind und zu den gleichen Schlussfolgerungen führen.
5. Spezifische Betrachtung zweier Endpunkte (In-vivo-Aufnahmewege und Lungenexpositionsversuche)
In den vergangenen Jahren haben sich bei der Beurteilung von ENMs und ihren biologischen Effekten zwei wesentliche Fragen herauskristallisiert. Eine davon ist, inwieweit ENMs von Zellen (in vitro) oder von Organismen (in vivo) aufgenommen werden können und bei einer In-vivo-Aufnahme auch ein Übertritt durch die jeweilige Gewebsbarriere erfolgt (Lunge: Luft/Blut-Schranke; Magen-Darm-Trakt: Darm/Blut-Schranke; Hautbarriere). Die andere Frage steht im Zusammenhang mit der Annahme, dass gerade der Aufnahmeweg Lunge besonders kritisch gewertet wird: Die beiden experimentellen Methoden, die Instillation und die Inhalation, müssen hier gegeneinander abgewogen werden, und es muss gefragt werden, ob die günstigere und einfachere Methode der Instillation zu verwertbaren Aussagen kommt. In diesem Abschnitt sollen diese beiden Fragen besonders betrachtet werden, und auf der Basis der evaluierten Literatur soll ein Versuch einer Antwort unternommen werden.
5.1. Aufnahme von ENMs in den Körper
Immer wieder werden ENMs im Zusammenhang mit der Exposition sowohl am Arbeitsplatz aber auch während des Gebrauchs von Produkten, die ENMs enthalten, als kritische Größe genannt. Dabei werden häufig alle pulverförmigen Materialien in einen “Nanotopf” gesteckt, wie dies z. B. mit Titandioxid geschieht, das in der Sonnenschutzcreme sicher in Nanogröße seine Wirkung am besten entfaltet,37 in der Zahnpasta oder der Wandfarbe aber als Mikro- oder Millimeterpartikel seine Wirkung tut! Weiterhin ist gerade dieses Material auch als Nahrungsmittelzusatzstoff zugelassen (E 171) und auch dort als Pigment enthalten (daher meist nicht in der Nanoform). Dennoch könnte man auch davon ausgehen, dass nach der aktuellen Definition von “Nanomaterialien” der EU-Kommission prinzipiell alle pulverförmigen Materialien zur Gruppe der Nanomaterialien gehören, denn durch den festgelegten prozentualen Anteil der Nanoobjekte an der Gesamtzahl der Partikel wird es nahezu unmöglich sein, Pulver auf den Markt zu bringen, die nicht unter diese Definition der Nanomaterialien fallen. Aber genauso wäre an dieser Stelle der Umkehrschluss richtig, dass auch alle bisher erzeugten Pulver aufgrund ihres immer vorhandenen hohen Anzahlanteils (wenn auch geringen Masseanteils) an Nanoobjekten bereits schon immer unter diese Definition gefallen wären und daher alle Untersuchungen dieser Pulver auch schon immer die Sicherheit von Nanomaterialien betroffen haben. Daher sei an dieser Stelle nochmals darauf hingewiesen, dass in der vorliegenden Studie ausschließlich Arbeiten berücksichtigt wurden, deren untersuchte Materialien in die ISO-Definition von Nanoobjekten gehören,1 also synthetisch hergestellte Nanopartikel, Nanofasern oder Nanoplättchen sind und hier immer mit ENMs abgekürzt werden.3
Für eine sachliche Diskussion der möglichen toxikologischen Bedeutung von ENMs ist es weiterhin wichtig, die Transportwege in den Körper zu kennen und eine mögliche systemische Verfügbarkeit zu validieren. Aus der Gesamtzahl der Studien sind 153 für den Aufnahmeweg Lunge, 204 für den Magen-Darm-Trakt und 201 für die Haut mit je einer eigenen Stichwortsuche gefunden worden, davon jeweils 151, 116 bzw. 111 ausgewertet und letztlich 116, 67 bzw. 74 als relevant angesehen worden (Abbildung 2). Während die Situation für die Hautbarriere recht eindeutig zu sein scheint – hier ist die absolute Mehrzahl der Studien der Meinung, dass es keine Penetration durch die Haut in tiefere, lebende Zellschichten gibt –, gilt dies nicht für die anderen beiden Barrieren. Es gibt starke Hinweise, dass ENMs diese Barrieren überschreiten können, allerdings gibt es auch hier wieder erhebliche Unterschiede in der Bewertung dieses Effektes. Für die Lunge wurde zwar nur in wenigen Studien, aber dennoch eindeutig nachgewiesen, dass ENMs in das Blut und damit zu sekundären Organen gelangen können.38–43 Dabei handelt es sich jedoch meist nur um sehr kleine Anteile der jeweils verabreichten Dosis. Es gibt außerdem auch Beispiele, dass für bestimmte ENMs kein solcher Transport stattfindet.44 Die überwiegende Mehrzahl der Studien hat jedoch diesen Punkt meist gar nicht berücksichtigt, sondern nur die direkten Effekte in der Lunge beobachtet und analysiert (Abbildung 2, oben). Daher ist zwar eine Evidenz vorhanden, dass ein Transport stattfindet, dieser ist aber wegen der enormen analytischen Probleme nur in Ausnahmefällen tatsächlich quantitativ erfasst worden und wurde als relativ klein bestimmt. Dies bedeutet aber gleichwohl nicht, dass dieser Anteil unbedeutend ist, da eine mögliche Akkumulation über die Lebenszeit in den Sekundärorganen bisher wenig untersucht wurde und nicht ausgeschlossen werden konnte. Knapp 8 % der gesichteten Arbeiten (9/116) beschrieben gar eine systemische Wirkung nach Aufnahme von ENMs über die Lunge. Eine davon war ein Übersichtartikel, der hier nicht genauer betrachtet werden soll. Die Originalarbeiten jedoch wurden auf spezielle Punkte hin angeschaut: Welches Nanomaterial wurde mit welcher Methode appliziert, und welche entscheidenden Punkte gilt es bei der Einordnung der Ergebnisse zu berücksichtigen (Tabelle 3). Ausgenommen eine Arbeit zu Kohlenstoffnanoröhrchen45 haben alle entweder sehr hohe lokale Konzentrationen durch Instillation erzeugt oder gleich im Overload-Bereich gearbeitet, oder die Löslichkeit der Materialien wurde nicht berücksichtigt oder nicht mit analysiert (z. B. bei Silber). Somit liefern die Studien, die nach Aufnahme über die Lunge einen systemischen Effekt beschreiben, mit einer Ausnahme keinen belastbaren Anhaltspunkt zu einer tatsächlich vorhandenen systemisch effektiven Dosis des jeweils applizierten ENM.
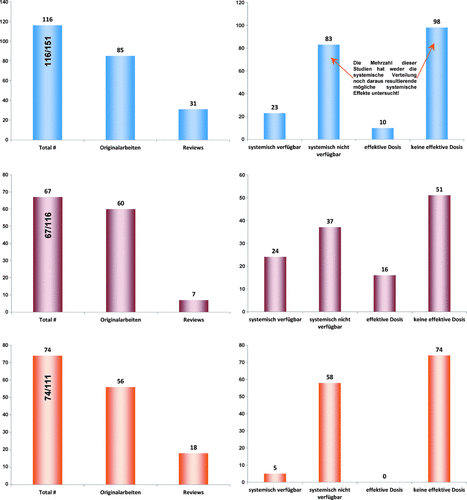
Auswertung der In-vivo-Studien zur Aufnahme von ENMs über die Lunge (oben), den Magen-Darm-Trakt (Mitte) und die Haut (unten). Links sind jeweils die Gesamtzahl der Studien sowie die Aufteilung auf Originalarbeiten und Übersichtsartikel dargestellt. Dabei ist jeweils in der Säule für die Gesamtzahl auch angegeben, wie groß die Zahl der Studien war, nachdem zum Stichwort selektioniert worden war, und wie viele der Studien davon als für diesen Endpunkt relevant angesehen wurden. Auf der rechten Seite ist die Aufteilung der relevanten Studien gezeigt, ob sie systemische Verteilungen und davon abhängige systemische Effekte analysiert haben.
|
Lit. |
ENM/Applikation |
Bemerkungen |
|---|---|---|
|
Li et al., 200746 |
CNT/Instillation |
Wiederholte Instillation, Gewebeschaden nicht auszuschließen! Transfer ins Blut nicht wirklich gezeigt, systemische Effekte auch als “indirekt” diskutiert! |
|
Song et al., 201147 |
SiO2/epidemiologische Studie |
In der Arbeit werden amorphe Kieselsäure und kristalline Formen synonym verwendet; epidemiologische Studie mit wenig Aussagekraft; keine Confounder betrachtet. |
|
Stapleton et al., 201245 |
CNT/Inhalation |
Systemischer Transfer nachgewiesen, aber nur 0.002 % der appl. Dosis! Dennoch endotheliale Schäden nachgewiesen. |
|
Sung et al., 200948 |
Ag/Inhalation |
Kein Nachweis von gelöstem Ag+! Systemische Wirkungen nur mit der höchsten Expositionsgruppe. |
|
Umezawa et al., 201149 |
CB[a]/Instillation |
Lokaler Overload![b] Gewebeschaden nicht auszuschließen; durch induzierte Entzündung auch Folgeeffekte in Föten. |
|
Vesterdal et al., 201050 |
CB[a]/Instillation |
Effekte nur in hohen Dosen, dadurch lokal sehr hohe Konzentrationen. |
|
Zhu et al., 200951 |
Fe2O3/Instillation |
4 mg/Ratte ist Overload-Szenario, daher keine echte Aussage zu einer systemischen Wirkung möglich. |
|
Zhang et al., 201252 |
Cu/intranasale Instillation |
Nur bei 10 und 40 mg kg−1 in Mäusen eine Wirkung! Beides ist jedoch Overload-Szenario. Wirkung wird ENMs und freigesetzten Ionen zugeschrieben. |
- [a] CB=Carbon Black (Industrieruß). [b] Zur Erklärung des Overload siehe Abbildung 5.
Beim zweiten Aufnahmepfad, über den Magen-Darm-Trakt, gibt es ebenfalls einige Besonderheiten (Abbildung 2, Mitte). Verglichen zur Lunge sind hier mit 16 deutlich mehr Arbeiten vorhanden, die sowohl eine Translokation in den Körper als auch eine systemische Wirkung diskutieren. Dies liegt unter anderem auch daran, dass zum einen relativ häufig Materialien eingesetzt wurden, die eine gewisse Löslichkeit haben und möglicherweise über die Freisetzung von Ionen wirken (ZnO, Cu, Ag; 6 Studien); außerdem sind die eingesetzten Mengen in mehr als der Hälfte dieser Studien mit 1–5 g kg−1 Körpergewicht der Versuchstiere sehr hoch gewählt. Zu einem sehr ähnlichen Resultat kommt ein jüngst publizierter Übersichtsartikel, der nur wenige Arbeiten zum Gastrointestinaltrakt aufführt, von denen wiederum nur ein kleiner Teil eine Absorption der ENMs durch das Darmepithel beschrieben hat.53 Aber auch in dieser Übersicht wird die enorme Menge von 5 g kg−1 Körpergewicht an TiO2, wie diese in einer der Studien im Versuch mit Mäusen eingesetzt wurde,54 nicht infrage gestellt, auch wenn selbst bei dieser enorm hohen Menge Titandioxid keine systemischen Effekte gefunden wurden.
Eindeutiger erscheint da das Ergebnis zur Haut. Die dermale Barriere scheint für ENMs wenig durchdringbar zu sein. So hat bisher keine einzige Arbeit beschrieben, dass durch die Aufnahme durch die Haut eine wirksame Körperdosis erreicht würde. Auch haben nur 5 % der Studien überhaupt von einer transdermalen Translokation applizierter ENMs berichtet. Dabei handelt es sich unter anderem um Experimente mit Silber-Nanopartikeln in einer Franz-Zelle mit keiner ausreichenden Studienbeschreibung und auch keiner Analytik für gelöstes Silber55 sowie um eine gute Arbeit aus der Gruppe von Monteiro-Riviere zu Peptid-derivatisierten Fullerenen, die auf Schweinehaut aufgebracht wurden, die wiederum 60 oder 90 min rhythmisch gedehnt wurde.56 Eine hervorragende Zusammenfassung zum Themenkomplex der Haut mit besonderer Betrachtung der beiden wichtigen Nanomaterialien Titandioxid und Zinkoxid, die vornehmlich in Sonnschutzcremes enthalten sind, wurde 2010 publiziert.57 Auch wenn sicher in den letzten drei Jahren noch einige Arbeiten dazugekommen sind, ist die Kernaussage des Artikels aber nach wie vor richtig: “The consistent finding of these different studies is that nano TiO2 or ZnO does not penetrate beyond the stratum corneum of the skin.”
Somit können die ersten Arbeitshypothesen beantwortet werden (Tabelle 4). Es ist unbestreitbar, dass ENMs die Lunge und den Magen-Darm-Trakt als Eintrittspforte in den Körper nutzen können. Allerdings ist es meist nur ein sehr kleiner Teil der verabreichten Dosis, der in das Blut und nachfolgend zu sekundären Organen transportiert wird. Der größte Anteil der verabreichten Dosis wird in der Lunge von Makrophagen aufgenommen und mit den Reinigungsprozessen aus der Lunge entfernt und/oder über die Faeces ausgeschieden. Wegen der sehr aufwändigen Analytik und der Schwierigkeit, Nanopartikel im Organismus wiederzufinden, ist jedoch die Zahl der Studien, die wirklich einen Transport über die Luft-Blut-Schranke untersucht haben, sehr klein. Ähnlich schlecht ist die Datenlage für den Magen-Darm-Trakt. Es gibt, relativ gesehen, weniger Arbeiten zu diesem Thema, die Analytik hat die gleichen großen Probleme und die Varianz in der Verwendung von verschiedenen ENMs und unterschiedlichen Dosisbereichen und Verabreichungsformen ist nochmals um einiges höher, sodass hier kaum einheitliche Aussagen möglich sind.
|
Hypothesen zur Aufnahme in vivo |
Zahl der evaluierten Studien |
ja |
nein |
|---|---|---|---|
|
ENMs[b] können mit der Luft eingeatmet werden und werden dadurch auch systemisch verfügbar. |
151 |
X |
|
|
ENMs können mit der Nahrung aufgenommen werden und werden dadurch systemisch verfügbar. |
116 |
X |
|
|
ENMs können die Haut durchdringen und werden dadurch systemisch verfügbar. |
111 |
X |
|
|
ENMs überschreiten Gewebsbarrieren und erreichen biologisch effektive Dosen (BED) im Körper. |
378 |
o |
o |
|
Alle ENMs können gleichermaßen die Barrieren durchdringen, es gibt keine Ausnahmen. |
378 |
X |
|
|
Die Aufnahme der ENMs ist abhängig von ihrer: |
378 |
||
|
Größe |
o |
o |
|
|
Form (Länge/Breite-Verhältnis) |
X |
||
|
Löslichkeit |
X |
- [a] Ein “X” bedeutet hier, dass die Hypothese entweder durch eine überwältigende Mehrheit oder durch eine Reihe von sehr wichtigen und qualitativ guten Studien befürwortet oder abgelehnt wurde. (Wenn im Zusammenhang mit den evaluierten Studien von “guter Qualität” die Rede ist, so ist entweder damit gemeint, dass die jeweiligen Studien den Kriterienkatalog des Projektes DaNa erfüllen oder der Impact Factor der Zeitschrift, in der diese Studien publiziert wurden, höher als 6 ist.) Ein “o” gibt an, dass es gute Gründe (eine gewissen Zahl von Studien mit guter Qualität) für die Annahme gibt, dass sowohl die Befürwortung als auch die Ablehnung der Hypothese richtig ist, meist abhängig von dem ENM und seinen Eigenschaften. [b] ENMs sind Nanomaterialien im Sinne der ISO-Definition für “Nanoobjekte” (siehe erste Fußnote im Text)
Die Situation stellt sich für die Haut deutlich besser dar. Hier werden nur unter extrem schlechten Bedingungen (die Haut ist verletzt, mechanisch stark gestresst oder mit Lösungsmitteln gängig gemacht) Einwanderungen in tiefere Zellschichten oder gar bis hin zu lebenden Zellen beobachtet.
Zwei wichtige Erkenntnisse sind an dieser Stelle noch erwähnenswert. Das Überschreiten von Barrieren scheint für kleinere Partikel leichter zu sein als für größere, und die Löslichkeit hat einen nicht unerheblichen Einfluss auf das Verhalten und die toxikologischen Effekte. Während die Größenabhängigkeit offensichtlich zu sein scheint, aber dann doch nur sehr wenige Partikel die jeweilige Barriere durchqueren können, ist die Frage nach der Löslichkeit auch gleichbedeutend mit der Frage nach der Nano-Relevanz – denn wenn sich Materialien auflösen, bevor oder während sie eine Gewebsbarriere überqueren, können wir nicht mehr davon ausgehen, dass wir es mit einem so genannten “Nano-Effekt” zu tun haben, was bedeutet, dass der toxikologische Prozess mit anderen Maßstäben als mit denen der Nanotoxikologie gemessen werden muss.
Interessant ist zusätzlich eine Betrachtung, welche Materialien jeweils auf den spezifischen Aufnahmeweg hin untersucht wurden (Abbildung 3). Während die faserartigen CNTs am häufigsten in der Lunge untersucht wurden, nimmt bei der Haut und dem Magen-Darm-Trakt das Titandioxid diese Stelle ein. Es gibt hier ganz offensichtlich sowohl ein produktbezogenes als auch ein sicherheitsrelevantes Auswahlkriterium für die jeweiligen Studienleiter. Für die Haut sind es meist Materialien, die in Kosmetika (ZnO, TiO2) oder in bakteriziden Oberflächen (Ag, TiO2) eine Rolle spielen, im Magen-Darm-Trakt wiederum solche ENMs, die auch in Lebensmitteln oder über die Nahrungskette von Bedeutung sind. Insgesamt werden diejenigen ENMs am häufigsten untersucht, die entweder bereits sehr häufig in Produkten enthalten sind (TiO2, ZnO, Ag) oder von denen eine gewisse kritische Wirkung erwartet werden könnte (Quantenpunkte (QDs), CNTs).
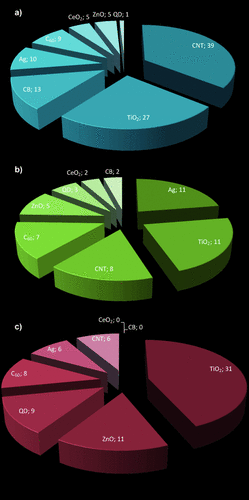
Auswertung der In-vivo-Studien zur Aufnahme von spezifischen ENMs über die a) Lunge, b) den Magen-Darm-Trakt und c) die Haut. Hinter den ENMs ist die Zahl der Studien aufgeführt.
5.2. Lungentoxizität – Instillation versus Inhalation
Die Nanotoxikologie hat ihre natürlichen Wurzeln in der kritischen Diskussion um den Feinstaub in der Luft. Die allerersten Arbeiten zu diesem Thema wurden daher auch weltweit von denjenigen Gruppen durchgeführt, die sich mit den gesundheitlichen Folgen einer Lungenbelastung durch Feinstaub beschäftigt und dann auch die Folgen einer Exposition gegenüber anderen ultrafeinen Partikeln betrachtet haben.58–71 Daher sind die Analogien der Wirkung von ENMs in der Lunge verglichen zu denjenigen von ultrafeinen Stäuben in den meisten Arbeiten und Diskussionen auch ein Thema. Dies bedeutet entsprechend, dass schon frühzeitig Ähnlichkeiten zwischen umweltrelevantem Feinstaub und synthetischen “Modellpartikeln” im Verhalten und bei den biologischen Wirkungen nach Lungenexposition erkannt wurden.70, 72, 73 Solange wie dieses Thema bearbeitet worden ist, gibt es außerdem eine Diskussion um die Methode, mit der die toxikologischen Aspekte erfasst werden sollen. Grundsätzlich gibt es zwei Möglichkeiten, Tierversuche zur Lungentoxizität von Partikeln durchzuführen: die aufwändige, aber realitätsnahe Variante der Inhalation und die einfachere und kostengünstigere Instillation. Ein ausführlicher Vergleich dieser Methoden wurde in der Gruppe von Oberdörster bereits vor über 15 Jahren vorgenommen.74–76 Im Jahr 2000 gab es eine klare Beschreibung der Instillation und ihrer Limitationen im Zusammenhang mit den Untersuchungen von Aerosolen.77 Es sollte angenommen werden können, dass sich diese Erkenntnisse nun auch bei den Experimenten zu den Nanomaterialien durchsetzen und die Durchführung der Studien den vorgegebenen Regeln folgt. Bei der Auswertung der Studien ab dem Jahr 2000 ergibt sich dazu nun folgendes Bild: Generell werden deutlich mehr Instillationsstudien durchgeführt als Inhalationsstudien (Abbildung 4). Dies liegt sicher mit darin begründet, dass die experimentelle Ausstattung und die Durchführung von Inhalationsexperimenten enorm viel analytischen Aufwand bedeuten. Schon allein die kontrollierte Aerosolherstellung über einen längeren Zeitraum (üblich sind 4–6 h Exposition pro Tag über mehrere Tage bis Wochen) ist für viele Arbeitsgruppen nicht möglich. Daher wird sehr häufig auf die Methode der Instillation zurückgegriffen.
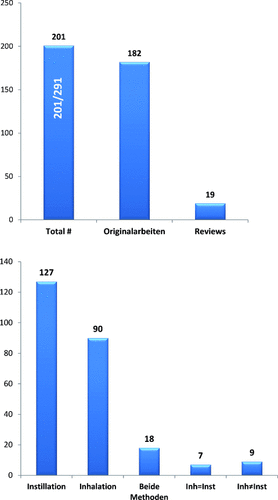
Gesamtzahl und Verteilung der Arbeiten zu den Themen “Inhalationsversuche” und “Instillationsversuche”.
Diese Methode ist sehr viel einfacher und kostengünstiger durchzuführen, weist aber auch einige Fallstricke auf, die bei Nichtbeachtung zu einer Verfälschung der Ergebnisse führen. So kann es durch die Gabe eines Bolus in den Atemtrakt vor allem bei faserigem Material (z. B. CNTs) dazu kommen, dass ganze Lungenbereiche nicht mehr ventiliert werden und die Tiere Mühe haben zu atmen oder sogar daran ersticken.22, 23 Solche Stresssituationen werden in jedem Fall zu Reaktionen der Tiere führen, die aber völlig unabhängig von den verabreichten Partikelsuspensionen sind. Die wesentlichen Punkte, die bei einer Instillation beachtet werden sollten, sind:
- •
die Methode der Intubation
- •
das spezifische Suspensionsmittel für die Partikel
- •
das Gesamtvolumen, das verabreicht wird
- •
die Gesamtdosis des Testmaterials
- •
die Methode der Anästhesie
Zusätzlich sollte als Kontrollversuch immer ein entsprechendes Material mituntersucht werden, zu dem es bereits eine gute Datenbasis gibt. Weiterhin sollte bei Ratten nicht über eine maximale Menge von 100 μg pro Instillation hinausgegangen werden, da die Ergebnisse durch Agglomeration und zu hohe lokale Belastung stark verfälscht werden. Bei einem direkten Vergleich zwischen beiden Methoden durch Gruppen, die innerhalb einer Studie beide Methoden eingesetzt haben, kommt es zu einer Gleichverteilung der Ansichten, dass beide Methoden zum gleichen Ergebnis oder aber zu unterschiedlichen Ergebnissen gelangen (Abbildung 4, unten). Allerdings wird in einer gerade publizierten Studie darauf hingewiesen,78 dass die Instillation im Prinzip immer zu deutlich stärkeren Effekten führt als die Inhalation. Dieser systematische Fehler kann leicht damit erklären werden, dass selbst bei Verabreichung der gleichen Dosis im Fall der Instillation deutlich höhere Dosisraten resultieren.
Ohne an dieser Stelle zu sehr in die Details zu gehen, die bei Driscoll et al. nachgelesen werden können,77 ist bei der Evaluation der Arbeiten zu ENMs sehr auffällig, dass Instillationsstudien erheblich häufiger im Overload-Bereich durchgeführt wurden als entsprechende Inhalationsstudien (Abbildung 5). Der Overload-Bereich, der bereits vor mehr als 20 Jahren definiert wurde,64, 79 ist aus dem Grund kritisch, dass die verabreichte Gesamtdosis die Reinigungsprozesse der Lunge überfordert. Allein der Umstand, dass überladene Makrophagen beginnen, Zytokine zu produzieren, löst einen Entzündungsprozess in der Lunge aus, der in den meisten Fällen unspezifisch ist, also nicht von der Art des applizierten Materials abhängt. Somit kann eine Studie unter solchen Bedingungen zu keinem stoffbezogenen Schluss kommen, was aber bedauerlicherweise doch immer wieder gemacht wird. Weiterhin ist durch die Methode der Instillation bedingt, dass es lokal zu sehr unterschiedlichen Belastungen der Lunge kommen kann. Während also die exponierten Bereiche der Lunge im Overload-Status sein können, gibt es andere Bereiche, die völlig unbelastet sind. Dies macht eine Interpretation der Ergebnisse häufig schwierig und wird in verschiedenen Publikationen in der Diskussion der Ergebnisse nicht entsprechend berücksichtigt. Bei der Bewertung der Inhalations- und Instillationsstudien nach dem Schweregrad der induzierten Effekte sind die Resultate überraschenderweise relativ gut in Übereinstimmung (Abbildung 5, oben). Obwohl die Tendenz bei der Instillation leicht in Richtung intensiverer Schäden (Quarz-ähnliche Wirkung) verschoben ist, liegt für beide Methoden das Maximum der Studien bezüglich der Einschätzung der ENM-Wirkung im Bereich einer Feinstaubexposition. Ausgewertet für die sechs am häufigsten untersuchten ENMs ist das Verhältnis von Inhalation zu Instillation für nahezu alle Materialien gleich, einzig für Silber wurden mehr Inhalations- als Instillationsstudien gefunden (Abbildung 5, Mitte). Aufgeschlüsselt nach den Wirkungskategorien sind die sechs ENMs sehr unterschiedlich zu bewerten. Die CNTs sind abhängig von ihrer Beschaffenheit sicher eine Stoffgruppe, die sehr kritisch bewertet wird. Dies macht auch das Verhältnis zwischen ernsten Wirkungen (Asbest- und Quarz-ähnlich) und leichteren Effekten (Feinstaub-ähnlich oder kein Effekt) deutlich (Abbildung 5, unten). Für alle anderen ENMs überwiegen die weniger schwerwiegenden Effekte; am besten sind sie vergleichbar zu den Wirkungen von Feinstaub mit einer transienten Entzündungsreaktion zwischen dem ersten und dem siebten Tag nach Expositionsbeginn, mit dem völligen Abklingen aller Symptome, sobald keine weitere Exposition stattfindet.
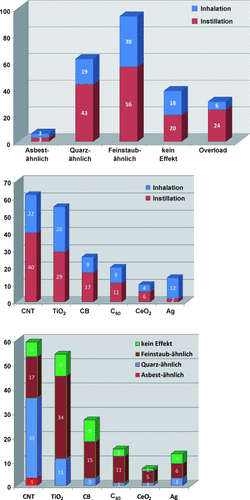
Auswertung aller Experimente mit Lungenexposition mit Hinblick auf die Art der Wirkung der applizierten Nanomaterialien und die angewendete Methode. Oben: Zahl der Studien, die eine spezifische Wirkung der ENMs beobachtet haben, wobei die unterschiedlichen Wirkungen wie folgt kategorisiert wurden: Asbest-ähnlich=Tumorinduktion vergleichbar zu Mesothelioma; Quarz-ähnlich=Entzündung, oxidativer Stress, Fibrose, Granulomabildung; Feinstaub-ähnlich=Wirkung wie bei “normaler ” Staubexposition, transiente Entzündungsprozesse; kein Effekt=unter den gegebenen Umständen (Dosis, Zeit) keine Effekte beobachtet; Overload=Ratte und Hamster: ≥2.5 mg/Tier und Lunge; Maus: ≥0.5 mg/Tier und Lunge. Mitte: Aufschlüsselung der eingesetzten Methoden für die sechs am häufigsten untersuchten ENMs. Unten: Aufschlüsselung der Wirkungskategorien für die sechs am häufigsten untersuchten ENMs.
Nach der detaillierten Betrachtung der Studienergebnisse zu ENMs nach Lungenexposition kann nun versucht werden, die Hypothesen für diesen Bereich zu prüfen (Tabelle 5). Im Falle der eingesetzten Methoden wird deutlich, dass die spezifischen Aspekte sowohl der Instillation als auch der Inhalation häufig nicht in genügendem Maße beachtet werden. Dies führt gerade bei Instillationsversuchen meist zu einer Überbewertung der Ergebnisse. Zusätzlich wird häufig der Aspekt des Overloads nicht genügend abgeklärt oder werden die aus diesen Studien erhaltenen Ergebnisse unkritisch übernommen.
|
Hypothesen zur Lungentoxizität in vivo |
Zahl der evaluierten Studien |
ja |
nein |
|---|---|---|---|
|
Instillation von Nanomaterialien in die Lunge zeigt deren spezifische Wirkung verlässlich an. |
317 |
X |
|
|
Instillationsstudien sind nicht so signifikant wie Inhalationsstudien. |
317 |
X |
|
|
Effekte, die nach Instillationsstudien beobachtet wurden, sind durch Inhalationsstudien immer bestätigt worden. |
317 |
X |
|
|
Die unterschiedlichen Dosierungen, die bei Instillations- und Inhalationsexperimenten verwendet werden, führen auch zu unterschiedlichen Resultaten. |
317 |
X |
|
|
Die Wirkung der ENMs unterscheidet sich grundsätzlich von derjenigen anderer partikulärer Belastungen der Lunge. |
317 |
X |
Abschließend kann festgestellt werden, dass sich Instillationsstudien sehr gut für die Gefährdungsidentifizierung eignen, während für eine umfassende Risikoabschätzung, einschließlich einer Risikocharakterisierung, auch Ergebnisse von Inhalationsstudien benötigt werden.84 Ein sehr wichtiges Ergebnis aus der Beurteilung der Studien ist wohl auch die Erkenntnis, dass sich ENMs in ihrer Wirkung auf die Lunge grundsätzlich nicht von anderen partikulären Belastungen unterscheiden.
Im Kontext der publizierten Ergebnisse wird auch deutlich, dass die bisherigen Studien im Wesentlichen in kurzen Zeiträumen durchgeführt wurden. Da es außerdem noch keine Situation zu geben scheint, in der eine epidemiologische Studie zu ENMs durchgeführt werden könnte, da die Belastungen am Arbeitsplatz bzw. der Allgemeinbevölkerung noch zu gering bzw. die Kollektive zu klein sind, gibt es keine belastbaren Aussagen zu möglichen Langzeitwirkungen. Andererseits werden manche der Materialien auch in Nanogröße seit vielen Jahrzehnten in größeren Mengen hergestellt (Carbon Black seit den 1920er Jahren, Nanosilber seit mehr als hundert Jahren, Titandioxid und Siliciumdioxid seit mehr als 50 Jahren) und seit dieser Zeit haben sich keine besorgniserregenden Resultate in den toxikologischen Studien gezeigt. Dies scheint sich auch grundsätzlich in den ausgewerteten Studien widerzuspiegeln.
6. Was erwarten wir von der Disziplin “Nanotoxikologie”?
Auch wenn es keinen Grund zu erhöhter Besorgnis zu geben scheint, sind dennoch die Prinzipien der Nanotoxikologie, wie diese vor einiger Zeit formuliert wurden,1 zu beachten und sollten bei allen Experimenten berücksichtigt werden, denn die besonderen Eigenschaften der ENMs, die sich aus der Kleinheit, dem besonderen Oberfläche-zu-Volumen-Verhältnis und den Materialunterschieden ergeben, könnten zu einem veränderten Verteilungsschema und einer anderen Biokinetik führen und weitere unterschiedliche Effekte bewirken. Daher sind die Anforderungen an die Nanotoxikologie als Disziplin eigentlich klar, denn sie soll grundsätzlich auf der Basis der spezifischen Nanoeigenschaften eines Materials eine Antwort auf die Frage liefern, ob auf ein ENM auch spezifische und speziell zu berücksichtigende Regulationen anzuwenden sind. Bevor diese Frage allerdings beantwortet werden kann, muss nach den entsprechenden Regeln für die Nanotoxikologie selbst gefragt werden. Wegen der erwähnten Unsicherheiten, der Mängel in der Qualität der Studien und der zu oft zu großen Unterschiede in der Vorgehensweise (Tabelle 1) lassen sich aus den Untersuchungen trotz der enorm steigenden Zahl von Publikationen noch keine allgemeingültigen Regeln ableiten. Aus wissenschaftlicher Sicht sind daher die Forderungen für zukünftige nanotoxikologische Studien klar (vgl. Tabelle 2):
- •
eine grundlegende und ausreichende Charakterisierung des untersuchten Materials
- •
Verwendung der korrekten Methode und eines angepassten Studiendesigns nach den Grundsätzen guter wissenschaftlicher Praxis
- •
Vorgehen nach den Richtlinien der Toxikologie, Einsatz von SOPs
- •
Beachtung der korrekten Dosis/Konzentration; Einschließen einer Dosis-Wirkungs-Beziehung in die Experimente
- •
Kontrolle der Eigenschaften der ENMs unter den jeweiligen Versuchsbedingungen
- •
Korrekte Auswahl des biologischen Modells
- •
Vergleich der Resultate zu parallel durchgeführten Kontrollansätzen
- •
nach Möglichkeit Einsatz eines Referenzmaterials zum besseren Vergleich
Im gesellschaftlichen Bereich sind die Anforderungen und Erwartungen an die Nanotoxikologie jedoch völlig anders. So unterschiedlich wie die Stakeholder der Gesellschaft sind, so verschieden sind die Ansprüche: die regierungsnahen Organisationen (Bundesoberbehörden, Ministerien, Parteien) möchten Antworten darauf haben, ob sich die finanzielle Unterstützung der Technologieentwicklung lohnt, ohne dass es ein Sicherheitsdesaster gibt; die Industrie möchte eindeutige Beweise, dass ENMs biologische Wirkungen haben; solange diese fehlen, wird produziert und werden “Nanoprodukte” auf den Markt gebracht; die Nichtregierungsorganisationen heben den warnenden Finger und wollen “vollkommene Sicherheit” für den Verbraucher und die Gesellschaft; der Verbraucher möchte sichere Produkte und hat ansonsten nur ein geringes Interesse an den Sicherheitsdebatten; die Wissenschaft erwartet Antworten auf die Fragen der biologischen Relevanz und möchte für ihre Untersuchungen gerne eine zusätzliche finanzielle Unterstützung, meist seitens des Staates, bekommen.
Diese unterschiedlichen Anforderungen können von der Nanotoxikologie als Disziplin derzeit kaum erfüllt werden. Zuerst einmal hat es diese relativ neue Disziplin80 versäumt, sich als Unterdisziplin der Toxikologie mit den gleichen Grundsätzen auszustatten, die für die allgemeine Toxikologie gelten (siehe Abschnitt 3). Weiterhin gilt natürlich für die Nanotoxikologie genau das gleiche wie für die allgemeine Toxikologie: Einen nicht vorhandenen Effekt kann man nicht nachweisen, auch wenn noch so lange danach gesucht wird. Ob und unter welchen Bedingungen das jeweilige ENM also keine Wirkung hat und somit unbedenklich ist, wird daher niemals publiziert und entzieht sich der Kenntnis der Allgemeinheit, wird damit auch nicht Gegenstand der Überlegungen zur Sicherheit von ENMs. Im Gegenschluss heißt das, dass unter dem Paradigma, dass die Dosis ein Gift macht, alle Substanzen und somit auch alle ENMs eine Wirkung haben, man muss nur die jeweilige Konzentration hoch genug wählen. Dies entspricht der augenblicklichen Situation in der Nanotoxikologie: Es werden nur “positive” Studien publiziert, also solche, die einen biologischen Befund beschreiben können, und ein solcher ist zumeist ein Effekt auf Zellen oder Gewebe und gibt damit Anlass zur Besorgnis. Wer allerdings die Arbeit der MAK-Kommission der DFG kennt, weiß, dass diese sehr wohl auf der Basis von wissenschaftlichen Erkenntnissen auch Substanzen als “verkehrsfähig” einstuft, die einen biologischen oder gar toxikologischen Effekt auslösen können, denn zur Beurteilung gehört auch die Einschätzung, wie realistisch es ist, dass die betreffende Dosis in der Umwelt oder im Organismus überhaupt erreicht wird.
Gleichermaßen würde ich mir von der Nanotoxikologie als Disziplin in der Zukunft wünschen, dass zusätzlich zu mechanistisch/biologischen Studien, die einfach nur nach den Wirkungsmechanismen suchen, auch wahre toxikologische Studien durchgeführt werden, die auf harmonisierten oder standardisierten Vorschriften zur Erkenntnis kommen, dass ein ENM keine oder eben doch eine toxikologische Relevanz hat und unter bestimmten Umständen mit Vorsicht behandelt werden muss.
Aktuell führt eine globale Betrachtung der bisherigen vielen tausend Publikationen (mit wenigen, meist nicht sehr überraschenden Ausnahmen, wie Cadmium-haltigen Quantenpunkten, löslichen Zinkoxid- und Kupferoxidpartikeln, faserförmigen Kohlenstoffnanoröhrchen inklusive der katalytischen Metalle) zu dem Schluss, dass offensichtlich trotz größter Anstrengungen vieler Arbeitsgruppen keine unerwarteten besorgniserregenden Ergebnisse für technische Nanomaterialien erhalten worden sind.81 Bleibt die Unsicherheit, ob die möglicherweise besorgniserregenden Ergebnisse einfach noch nicht gefunden wurden oder ob es sie tatsächlich für die bisher untersuchten ENMs nicht gibt.
7. Empfehlungen: internationale Harmonisierung und die Regeln der Toxikologie
Seit mehr als zehn Jahren haben wir in den meisten technologisch hochentwickelten Ländern dieser Erde Aktionspläne für Entwicklungen auf dem Gebiet der Nanotechnologie, so auch in der Europäischen Union. In diesen Aktionsplänen ist jeweils ein Paket enthalten, das sich mit sicherheitsrelevanten Fragen beschäftigt und dazu auch entsprechende Forschungs- und Fördermaßnahmen umfasst. Seit dem 6. Rahmenprogramm werden in Europa, aber auch in spezifischen Förderprogrammen der einzelnen Mitgliedsstaaten und weiterer Länder, Aktivitäten zur Nanosicherheit unterstützt. Diese Programme sind grundsätzlich mit dafür verantwortlich, dass wir den jetzt sichtbaren Anstieg der Publikationen zu diesem Thema erleben, aber auch die babylonische Vielfalt in den Studien und Ergebnissen beurteilen müssen. Dabei wird zu wenig darauf hingewiesen, dass sich eine Reihe von Wissenslücken mit diesen neuen Erkenntnissen hat schließen lassen, allerdings einige wichtige Lücken bisher noch nicht in ausreichendem Maße bearbeitet wurden. Folgende Handlungsempfehlungen ergeben sich aus den oben gemachten Überlegungen:
- •
Die politischen Gremien müssen verstehen, dass sie für ENMs keine absolute Sicherheit durch die Forschungsprogramme bekommen werden, da der Nachweis einer nicht vorhandenen Wirkung nicht gegeben werden kann. Wir müssen zurück auf die Ebene der Risikoabschätzung im Kontext der Expositionswahrscheinlichkeiten und Dosisbeziehungen.
- •
In den Förderprogrammen erarbeitete Standardvorschriften und methodische Weiterentwicklungen müssen zur Grundlage neuer Förderprojekte gemacht werden. Wer diese Regeln nicht kennt oder nicht anwendet, sollte keine Fördergelder in toxikologisch ausgerichteten Programmen mehr bekommen.
- •
Zur Harmonisierung der Methoden gehört auch die Förderung zur Verbesserung der Analytik, die gerade für Untersuchungen von ENMs eine besonders anspruchsvolle Aufgabe ist.
- •
Wichtige Entwicklungen in der Toxikologie, wie die internationale Aktivität zur Toxikologie des 21. Jahrhunderts82 und eine entsprechende Nanotoxikologie des 21. Jahrhunderts,83 sind zur Grundlage weiterer Forschungsbemühungen zu machen. Zusammenhänge zwischen In-vitro- und In-vivo-Experimenten ebenso wie Extrapolationen sowie die Vorhersagekraft der In-vitro-Experimente sind dabei stark zu verbessern.
- •
Wissenslücken (z. B. zu bestimmten Expositionspfaden wie dem Magen-Darm-Trakt) sollten in neuen Programmen spezifisch abgedeckt werden.
- •
Langzeitstudien zu einer möglichen Akkumulation sollten in kommende Fördermaßnahmen integriert werden.
- •
Eine bessere Vergleichbarkeit der Studien muss auch darüber erreicht werden, dass die durchführenden Laboratorien eine entsprechende Fachkenntnis vorweisen können. Eine Qualitätskontrolle in den methodischen Vorgehensweisen wäre wünschenswert. Dazu gehört obligatorisch die ausreichende und kompetente physikochemische Charakterisierung der ENMs, ohne die es keine Förderung von Projekten mehr geben darf.
- •
Entscheidungen zur Regulation von ENMs sollten von Experten getroffen werden, die sich im Umfeld toxikologischer Wirkprinzipien auskennen, da sie eine entsprechende Ausbildung haben.
Im internationalen Kontext ist es natürlich beliebig schwierig, alle Forderungen überall in gleichem Umfang zu erfüllen, aber wir sollten in jedem Fall versuchen, die internationale Harmonisierung zu verbessern. Ohne den Abgleich in den Methoden und ohne übereinstimmende Vorgehensweisen bei den Dosierungen in den Experimenten und Studiendesigns werden weiter Resultate mit teilweise erschreckenden Meldungen generiert, die aber keine vernünftige Grundlage haben und die wiederum mit neuen Studien widerlegt werden müssen.
8. Quo vadis Nanotoxikologie? Ein kritischer Ausblick zur Disziplin
Vor 40 Jahren schrieb Henschler in seinem Beitrag in der Angewandten Chemie: “Die aufgezeigten Grenzen der Aussagekraft epidemiologischer und tierexperimenteller Methoden machen deutlich, dass eine absolut sichere Voraussage darüber, ob für bestimmte Stoffe eine toxische Wirkung beim Menschen erwartet werden muss oder ausgeschlossen werden kann, nicht möglich ist. Die Öffentlichkeit aber erwartet, der Journalist fordert und mancher Produzent verspricht ‘Sicherheit’ vor Gesundheitsschäden durch Umweltgifte.”32 Durch den Austausch des Wortes “Umweltgifte” gegen “ENMs” trifft dieser Satz heute genauso zu wie damals. Ohne die Anerkennung dieser Tatsache und die Publikation von Studien, die genau solche “Negativeffekte”, d. h. fehlende Wirkungen, beschreiben, werden wir für ENMs keine vernünftigen Aussagen machen können. Wenige Studien, die ohne toxikologischen Sachverstand durchgeführt wurden und ohne echte wissenschaftliche Grundlage von einem “enormen toxikologischen Potenzial” bei ENMs sprechen, haben mehr Wirkung in der Gesellschaft als die vielen guten Studien, die mit Dosis-Wirkungs-Beziehungen aufzeigen, dass wir uns in einem sicheren Umfeld bewegen, da weder durch die gefundenen Effekte noch durch die prognostizierten Umweltkonzentrationen eine Wirkung in Mensch und Umwelt erwartet werden kann.
Dies erfordert von uns allen allerdings ein klares Bekenntnis zu den Grundsätzen der Toxikologie. Ohne die Einhaltung und Respektierung der fundamentalen Regeln von toxikologischen Studiendesigns und ohne die Harmonisierung der Vorgehensweisen, z. B. durch Anwendung von SOPs oder anderen standardisierten Vorschriften, werden auch die zukünftigen Förderprogramme, national wie international, wirkungslos verpuffen und nur weiter zur babylonischen Vielfalt der Ergebnisse beitragen.
Acknowledgements
Ich bedanke mich bei A. Fischer für die Durchführung der Literatursuche und die Zusammenfassung der Publikationen in einer Datenbank. Weiterhin möchte ich mich besonders bei K. Krug bedanken, ohne deren Hilfe die Auswertung der Flut von Daten nicht in der kurzen Zeit funktioniert hätte. Ganz besonders bedanke ich mich beim Bundesministerium für Bildung und Forschung für die finanzielle Unterstützung des Projektes DaNa (BMBF; FKZ 03X0075A), bei dem Förderprogramm CCMX und den Schweizer Bundesämtern für Umwelt und für Gesundheit für die Unterstützung des Projektes VIGO sowie beim deutschen VCI für die direkte Finanzierung der Auswertung der Literaturdatenbank.
Biographical Information
Harald F. Krug ist in der Geschäftsleitung der Empa in der Schweiz für die internationalen wissenschaftlichen Beziehungen zuständig und ist im Rahmen einer Titularprofessur an der Universität Bern in der Lehre tätig. Er ist Mitglied im Lenkungsgremium des DECHEMA-AK zum verantwortungsvollen Umgang mit Nanomaterialien und in vielen weiteren Expertengruppen zu diesem Thema und berät Bundesministerien in Deutschland wie auch Bundesämter der Schweiz zur Nanotechnologie. 2006 erhielt er den cwi-Award der Deutschen Keramischen Gesellschaft und 2007 den Forschungspreis des Landes Baden-Württemberg zu “Ersatz- und Ergänzungsmethoden zum Tierversuch”.
- 1 Unter “Nanomaterial” wird in diesem Artikel die Gesamtheit der so genannten “Nanoobjekte” verstanden (siehe Lit. 1 für eine Definition). Bei allen Studien wird daher als Größe der Wert für das Primärpartikel berücksichtigt und nicht derjenige für die Agglomerate oder Aggregate. Vergleiche dazu auch die Definition der EU in der dritten Fußnote dieses Textes.
- 2 Informationen zu den Suchbegriffen, der Datenbank, den Kriterien und den aufgestellten Hypothesen sowie einige statistische Auswertungen einschließlich alle Zitate der ausgewählten und bewerteten Arbeiten zu den Themen dieses Aufsatzes finden sich in den Hintergrundinformationen.
- 3 “Nanomaterial” ist ein natürliches, bei Prozessen anfallendes oder hergestelltes Material, das Partikel in ungebundenem Zustand, als Aggregat oder als Agglomerat enthält und bei dem mindestens 50 % der Partikel in der Anzahlgrößenverteilung ein oder mehrere Außenmaße im Bereich von 1 nm bis 100 nm haben (Amtsblatt der Europäischen Union, L 275/38, 2011/696/EU).





