Enantioselektive intramolekulare [2+2]-Photocycloadditionen in Lösung
Thorsten Bach Prof. Dr.
Fachbereich Chemie der Philipps-Universität Hans-Meerwein-Straße, 35032 Marburg, Deutschland
Search for more papers by this authorHermann Bergmann Dipl.-Chem.
Fachbereich Chemie der Philipps-Universität Hans-Meerwein-Straße, 35032 Marburg, Deutschland
Search for more papers by this authorKlaus Harms Dr.
Fachbereich Chemie der Philipps-Universität Hans-Meerwein-Straße, 35032 Marburg, Deutschland
Search for more papers by this authorThorsten Bach Prof. Dr.
Fachbereich Chemie der Philipps-Universität Hans-Meerwein-Straße, 35032 Marburg, Deutschland
Search for more papers by this authorHermann Bergmann Dipl.-Chem.
Fachbereich Chemie der Philipps-Universität Hans-Meerwein-Straße, 35032 Marburg, Deutschland
Search for more papers by this authorKlaus Harms Dr.
Fachbereich Chemie der Philipps-Universität Hans-Meerwein-Straße, 35032 Marburg, Deutschland
Search for more papers by this authorDieses Projekt wurde von der Deutschen Forschungsgemeinschaft (Ba 1372-4/1 und -4/2) und dem Fonds der Chemischen Industrie gefördert. Wir danken Herrn Stefan Sieber (Forschungspraktikum) für tatkräftige experimentelle Unterstützung.
Kristallstrukturanalyse
Abstract
Wasserstoffbrücken ermöglichen es, dass prochirale 2-Chinolone wie 1 an den chiralen Wirt 2 gebunden werden, sodass in einer enantioselektiven, intramolekularen [2+2]-Photocycloaddition Cyclobutane wie 3 mit hohen ee-Werten (bis zu 93 % ee) gebildet werden können. Der Wirt lässt sich vom Produkt trennen und wird nahezu quantitativ zurückgewonnen.
References
- 1Übersichten: (a) S. R. L. Everitt, Y. Inoue in Molecular and Supramolecular Photochemistry: Organic Molecular Photochemistry, Vol. 3 (Hrsg.: V. Ramamurthy, K. S. Schanze), Marcel Dekker, New York, 1999, S. 71–130; (b) Y. Inoue, Chem. Rev. 1992, 92, 741–770; (c) H. Rau, Chem. Rev. 1983, 83, 535–547.
- 2(a) Übersichten zu Auxiliar-kontrollierten stereoselektiven Photoreaktionen: T. Bach, Synthesis 1998, 683–703; (b) S. A. Fleming, C. L. Bradford, J. J. Gao in Molecular and Supramolecular Photochemistry: Organic Photochemistry, Vol. 1 (Hrsg.: V. Ramamurthy, K. S. Schanze), Marcel Dekker, New York, 1997, S. 187–243; (c) J.-P. Pete, Adv. Photochem. 1996, 21, 135–216; (d) J. Mattay, R. Conrads, R. Hoffmann, Methoden Org. Chem. (Houben-Weyl) 4th ed. 1952–, Vol. E 21c, 1995, S. 3085–3178; (e) M. Demuth, G. Mikhail, Synthesis 1989, 145–162.
- 3 Einige ausgewählte Beispiele aus dem Bereich der [2+2]-Photocycloadditionen: (a) L. M. Tolbert, M. B. Ali, J. Am. Chem. Soc. 1982, 104, 1742–1744; (b) H. Koch, J. Runsink, H.-D. Scharf, Tetrahedron Lett. 1983, 24, 3217–3220; (c) A. I. Meyers, S. A. Fleming, J. Am. Chem. Soc. 1986, 108, 306–307; (d) M. Demuth, A. Palomer, H.-D. Sluma, A. K. Dey, C. Krüger, Y.-H. Tsay, Angew. Chem. 1986, 98, 1093–1095; Angew. Chem. Int. Ed. Engl. 1986, 25, 1117–1119.
- 4 Photopinakolisierung: (a) D. Seebach, H.-A. Oei, H. Daum, Chem. Ber. 1977, 110, 2316–2333; (b) L. Horner, J. Klaus, Liebigs Ann. Chem. 1979, 1232–1257.
- 5 Photocyclisierung: T. Naito, Y. Tada, I. Ninomiya, Heterocycles 1984, 22, 237–240.
- 6 Photochemische Umlagerung: D. R. Boyd, R. M. Campbell, P. B. Coulter, J. Grimshaw, D. C. Neill, W. B. Jennings, J. Chem. Soc. Perkin Trans. 1 1985, 849–855.
- 7 Photoabbau: N. Levi-Minzi, M. Zandomeneghi, J. Am. Chem. Soc. 1992, 114, 9300–9304.
- 8(a) Photooxygenierung: L. Weber, I. Imiolczyk, G. Haufe, D. Rehorek, H. Hennig, J. Chem. Soc. Chem. Commun. 1992, 301–303; (b) A. Sakai, H. Tani, T. Aoyama, T. Shioiri, Synlett 1998, 257–258, zit. Lit.
- 9Übersichten: (a) F. Toda, Acc. Chem. Res. 1995, 28, 480–486; (b) Y. Ito, Synthesis 1998, 1–32.
- 10 A. Joy, S. Uppili, M. R. Netherton, J. R. Scheffer, V. Ramamurthy, J. Am. Chem. Soc. 2000, 122, 728–729, zit. Lit.
- 11 T. Bach, H. Bergmann, K. Harms, J. Am. Chem. Soc. 1999, 121, 10650–10651.
- 12 C. Kaneko, T. Suzuki, M. Sato, T. Naito, Chem. Pharm. Bull. 1987, 35, 112–123.
- 13 J. G. Stack, D. P. Curran, S. V. Geib, J. Rebek, Jr., P. Ballester, J. Am. Chem. Soc. 1992, 114, 7007–7018.
- 14 M. Kajino, Y. Shibouta, K. Nishikawa, K. Meguro, Chem. Pharm. Bull. 1991, 39, 2896–2905.
- 15
Die Absolutkonfiguration des Tetrahydronaphthalinoxazolderivats (+)-5 wurde zum einen über den Drehwertvergleich ([α]
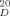 = + 7.4; c = 1 in CHCl3) mit dem analogen, bekannten Benzoxazolderivat[13] ([α]
= + 7.4; c = 1 in CHCl3) mit dem analogen, bekannten Benzoxazolderivat[13] ([α]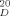 = + 7.4; c = 2 in CHCl3) als auch durch die Absolutkonfiguration des Bestrahlungsprodukts 2 eindeutig bewiesen.
= + 7.4; c = 2 in CHCl3) als auch durch die Absolutkonfiguration des Bestrahlungsprodukts 2 eindeutig bewiesen.
- 16 Die Reaktionen wurden in Toluol als Lösungsmittel (0.15 M Lösung von 1) bei der angegebenen Temperatur durchgeführt. Weitere Angaben zur Bestrahlungsvorschrift finden sich in: T. Bach, J. Schröder, J. Org. Chem. 1999, 64, 1265–1273. Die ee-Werte (ee=[(−)-2–(+)-2)]/[(−)-2 + (+)-2]) wurden durch HPLC-Analyse des Rohprodukts bestimmt (Säule: Chiracel OD; Eluent: Hexan/Isopropanol 92:8). Die Trennung von Wirt und Produkt ist durch Flashchromatographie möglich (Pentan/tert-Butylmethylether 1:2). Beide Enantiomere des Wirts 5 wurden verwendet. Naturgemäß ändert sich die Richtung der Seitendifferenzierung, wenn (+)-5 durch (−)-5 ersetzt wurde.
- 17 Kristallstrukturanalyse von (−)-4 (C22H37NO3·CH2Cl2, Mr = 448.45): Kristallgröße 0.3 × 0.3 × 0.15 mm3, orthorhombisch, Raumgruppe P212121, a = 852.0(1), b = 1212.3(1), c = 2410.5(1) pm, V = 2489.9(4) Å3, ρber. = 1.196 gcm−3, Z = 4, F(000) = 968, μ = 2.516 mm−1, Enraf-Nonius-CAD4-Diffraktometer, Λ = 1.54178 Å, ω-Scans, 4875 gemessene Reflexe (−h,+k, ±l), Θmax = 65°, 4245 unabhängige und 3575 beobachtete Reflexe [F±4σ(F)], 272 verfeinerte Parameter, R = 0.0608, wR2 = 0.2080, max. Restelektronendichte 0.22 eÅ−3, Direkte Methoden, C-gebundene H-Atome berechnet, N-H verfeinert. Die kristallographischen Daten (ohne Strukturfaktoren) der in dieser Veröffentlichung beschriebenen Struktur wurden als „supplementary publication no. CCDC-142268”︁ beim Cambridge Crystallographic Data Centre hinterlegt. Kopien der Daten können kostenlos bei folgender Adresse in Großbritannien angefordert werden: CCDC, 12 Union Road, Cambridge CB21EZ (Fax: (+44) 1223-336-033; E-mail: [email protected]).
- 18 T. Bach, H. Bergmann, K. Harms, unveröffentlichte Ergebnisse.
Citing Literature
This is the
German version
of Angewandte Chemie.
Note for articles published since 1962:
Do not cite this version alone.
Take me to the International Edition version with citable page numbers, DOI, and citation export.
We apologize for the inconvenience.



112:13<>1.0.co;2-v.cover.gif)
